Clear Sky Science · nl
MerTK-geactiveerd TGFβ1-autocriene signaal reguleert microgliale reactie op neurodegeneratie
Hoe het schoonmaakteam van de hersenen ziekte vormt
Wanneer zenuwcellen in de hersenen en de oogzenuw afsterven, laten ze een spoor van puin achter. Gespecialiseerde immuuncellen, microglia genoemd, fungeren als het schoonmaakteam van de hersenen en ruimen dit afval op. Maar microglia doen meer dan alleen opruimen: hun reactie kan zenuwnetwerken beschermen of ziekten zoals Alzheimer verergeren. Deze studie onthult een verborgen zelfcommunicatiemechanisme binnen microglia dat wordt geactiveerd door afval van afstervende zenuwvezels en mede bepaalt hoe sterk deze cellen op schade reageren.
Een trigger verborgen in afstervende zenuwvezels
Om dit proces te onderzoeken gebruikten de onderzoekers een muismodel waarbij de oogzenuw wordt gekneusd, waardoor de lange uitlopers van oogneuronen degenereren zonder de cellichamen te doden. Dit isoleert op nette wijze de nasleep van axonafbraak. Op het oppervlak van deze degenererende vezels draait een vetmolecuul naar buiten, en fungeert als een “eet mij”-signaal voor nabijgelegen microglia. Die signalen worden waargenomen door een receptor op microglia genaamd MerTK, behorend tot een kleine familie van eiwitten die puin herkennen. Door MerTK selectief in microglia te verwijderen, toonde het team aan dat microglia zonder deze receptor hun gebruikelijke reactie op letsel niet konden uitvoeren: ze deelden minder, bewogen minder en schakelden minder genen in die met schadebestrijding en ontsteking samenhangen.
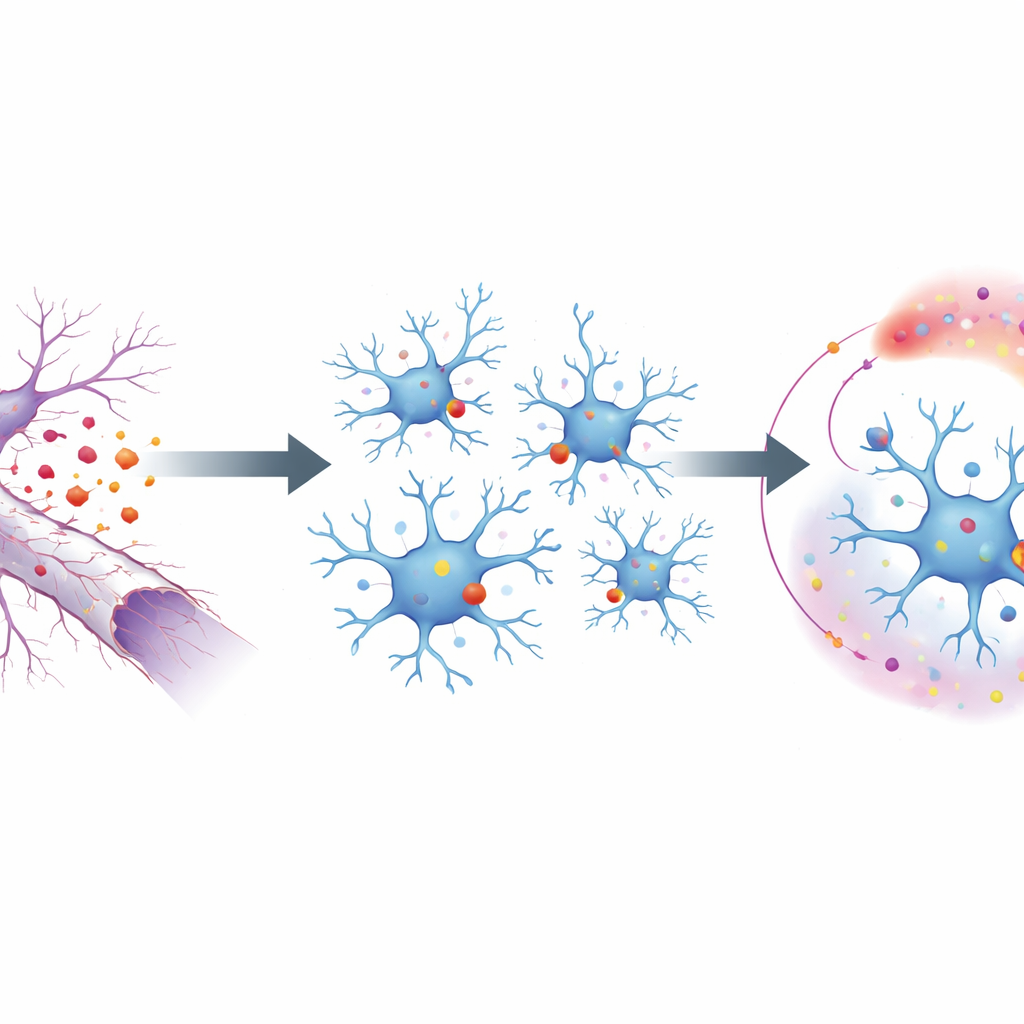
Van oppervlaktesignaal naar genetische herprogrammering
Door in microglia te kijken, volgden de wetenschappers hoe het MerTK-oppervlaktesignaal wordt omgezet in veranderingen in genactiviteit. Ze ontdekten dat MerTK een moleculaire relais activeert, fosfolipase C genaamd, dat op zijn beurt twee hoofdregelproteïnen in de kern versterkt: PU.1 en IRF8. Deze factoren functioneren als voormannen op de microgliale assemblagelijn en schakelen veel genen in die nodig zijn voor een geactiveerde toestand. Met DNA-bindingskaarten vond het team dat PU.1 en IRF8 rechtstreeks binden aan een specifieke plaats in het gen dat TGFβ1 codeert, een krachtig signaalproteïne. Wanneer deze bindingsplaats zo werd gemuteerd dat de voormannen er niet meer konden binden, konden microglia in beschadigde zenuwen geen verhoogde TGFβ1-productie opwekken, hoewel andere basisfuncties intact bleven.
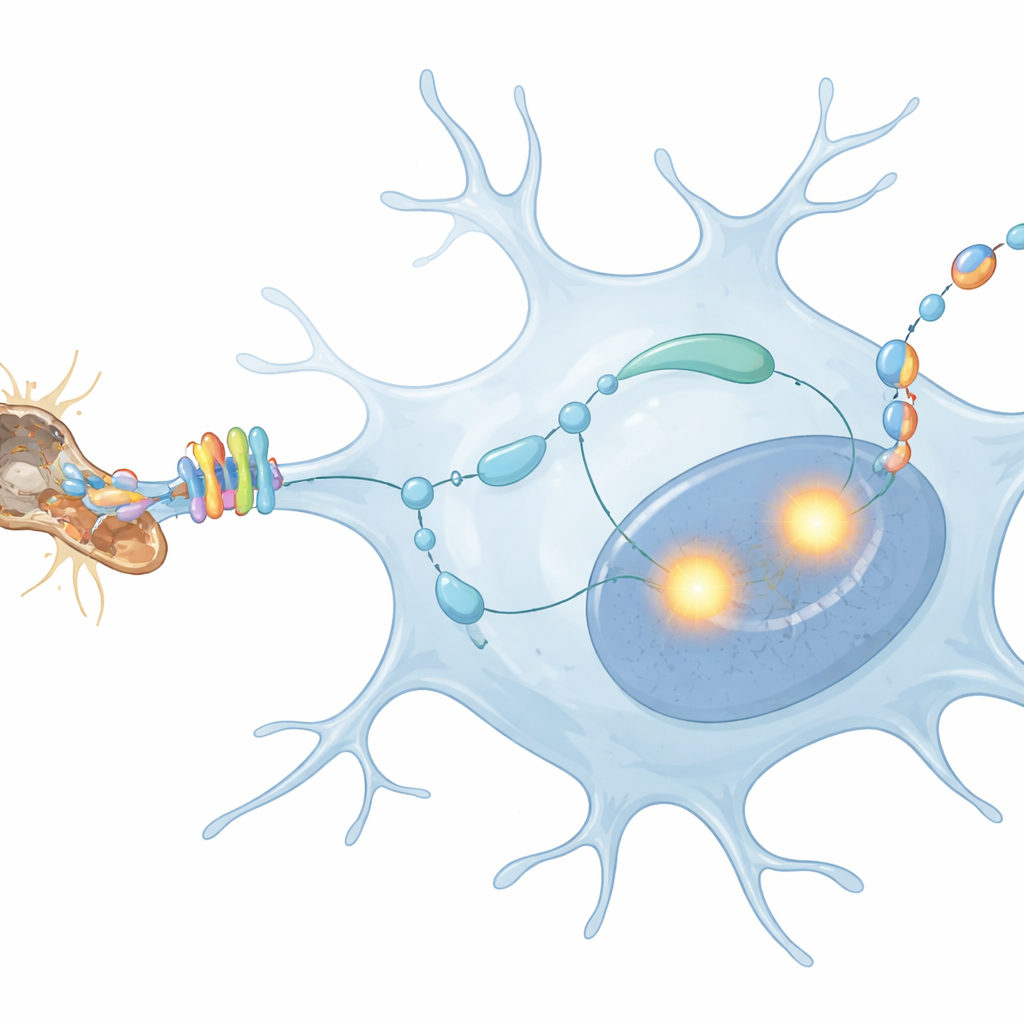
Een zelfterugkoppelingslus in microglia
De volgende vraag was wat TGFβ1 in deze context precies doet. De studie toont aan dat microglia TGFβ1 produceren en er vervolgens zelf op reageren, waardoor een autocriene, oftewel zelfterugkoppelingslus ontstaat. Wanneer TGFβ1 of de receptoren ervan genetisch alleen in microglia werden verwijderd, veroorzaakte het letsel nog steeds axondegeneratie, maar lieten microglia hun volledige activatieprogramma niet meer zien. Ze vermenigvuldigden zich minder en drukten minder schade-respons- en ontstekingsgenen uit, hoewel veel homeostatische identiteitskenmerken door andere signalen nog steeds werden onderdrukt. Een belangrijke downstream-molecule van TGFβ-signaling, gefosforyleerd SMAD2, verscheen specifiek in microgliale kernen na letsel en verdween grotendeels wanneer TGFβ1 of de receptoren werden uitgeschakeld, wat bevestigt dat de zelfterugkoppeling was doorbroken.
Van muis-oogzenuw naar Alzheimerhersen
Om te testen of deze route verder reikt dan een kunstmatig letselmodel, onderzochten de auteurs een veelgebruikt muismodel van de ziekte van Alzheimer. Bij deze dieren vertoonden microglia die zich rond amyloïdeplaque clusterden hoge niveaus van PU.1, IRF8, TGFβ1 en geactiveerde TGFβ-signaleringspatronen, in overeenstemming met de bevindingen in de oogzenuw. Het team keek vervolgens naar menselijke gegevens uit single-nucleus RNA-sequencing van hersenweefsel van Alzheimerpatiënten. Daar vielen microglia op als de belangrijkste cellen die de menselijke tegenhangers van MerTK, PU.1, IRF8 en TGFB1 tot expressie brachten. In postmortem hersensecties van patiënten lieten microglia ook sterke tekenen zien van actieve TGFβ-signalisering, in tegenstelling tot weefsel van controles. Samen pleiten deze observaties ervoor dat dezelfde zelfcommunicatielus ook in menselijke ziekte een rol speelt.
Waarom dit zelfgesprek belangrijk is voor hersengezondheid
Dit onderzoek onthult een keten van gebeurtenissen waarbij puin van degenererende zenuwvezels MerTK op microglia activeert, wat vervolgens PU.1 en IRF8 versterkt, die op hun beurt microglia aanzetten tot het produceren van TGFβ1 dat weer op henzelf terugwerkt. Dit zelfgesprek scherpt en bestendigt hun reactie op neurodegeneratie. Voor de niet-specialist is de kernboodschap dat de schoonmakers van de hersenen niet slechts passieve opruimers zijn; ze luisteren actief naar hun eigen signalen, en deze terugkoppelingslus kan bepalen of hun handelen neuronen beschermt of ziektes zoals Alzheimer vooruit helpt. Inzicht in en mogelijke bijsturing van dit circuit kan nieuwe wegen openen om schadelijke ontsteking te matigen terwijl de nuttige opruimfunctie van microglia behouden blijft.
Bronvermelding: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
Trefwoorden: microglia, neurodegeneratie, Ziekte van Alzheimer, hersenontsteking, TGF-beta signalering