Clear Sky Science · nl
Het redoxgestuurde Na+-pompmecanisme in Vibrio cholerae NADH-quinone oxidoreductase berust op dynamische conformationele veranderingen
Hoe het energiecentrum van cholera een geneesmiddeldoelwit werd
Bacterie die cholera veroorzaakt, Vibrio cholerae, overleeft en vermeerdert door een kleine moleculaire energiecentrale in zijn celmembraan te laten draaien. Deze studie onthult, met ongekende details, hoe een van zijn sleutelmotoren — een enzym genaamd Na⁺-NQR — van vorm verandert terwijl het natriumionen uit de cel pompt. Inzicht in deze moleculaire machine bevredigt niet alleen de fundamentele nieuwsgierigheid naar hoe leven voedsel omzet in bruikbare energie, maar wijst ook op nieuwe manieren om antibiotica te ontwerpen die schadelijke bacteriën uitschakelen zonder menselijke cellen te beïnvloeden.
Een door natrium aangedreven motor in bacteriën
Veel mariene en ziekteverwekkende bacteriën vertrouwen op Na⁺-NQR als de eerste stap in hun respiratoire keten, de reeks reacties die energie uit nutriënten wint. Na⁺-NQR zit in het binnenmembraan en neemt elektronen van een brandstofmolecuul genaamd NADH, en geeft die door een keten van gekleurde "hulp"moleculen (cofactoren genoemd) aan quinon, een ander klein molecuul ingebed in het membraan. Terwijl elektronen stromen, gebruikt het enzym die energie om natriumionen (Na⁺) van binnen naar buiten te duwen, waardoor een natriumgradiënt ontstaat. Deze gradiënt is als een opgeladen batterij: hij drijft de bacteriële flagellaire motor voor beweging aan, helpt bij het maken van ATP (de energievaluta van de cel) en stuurt opname van voedingsstoffen en het wegpompen van medicijnen. Omdat Na⁺-NQR alleen in bacteriën voorkomt en sterk verschilt van het verwante enzym in onze mitochondriën, is het een aantrekkelijk doelwit voor zeer selectieve antibiotica.
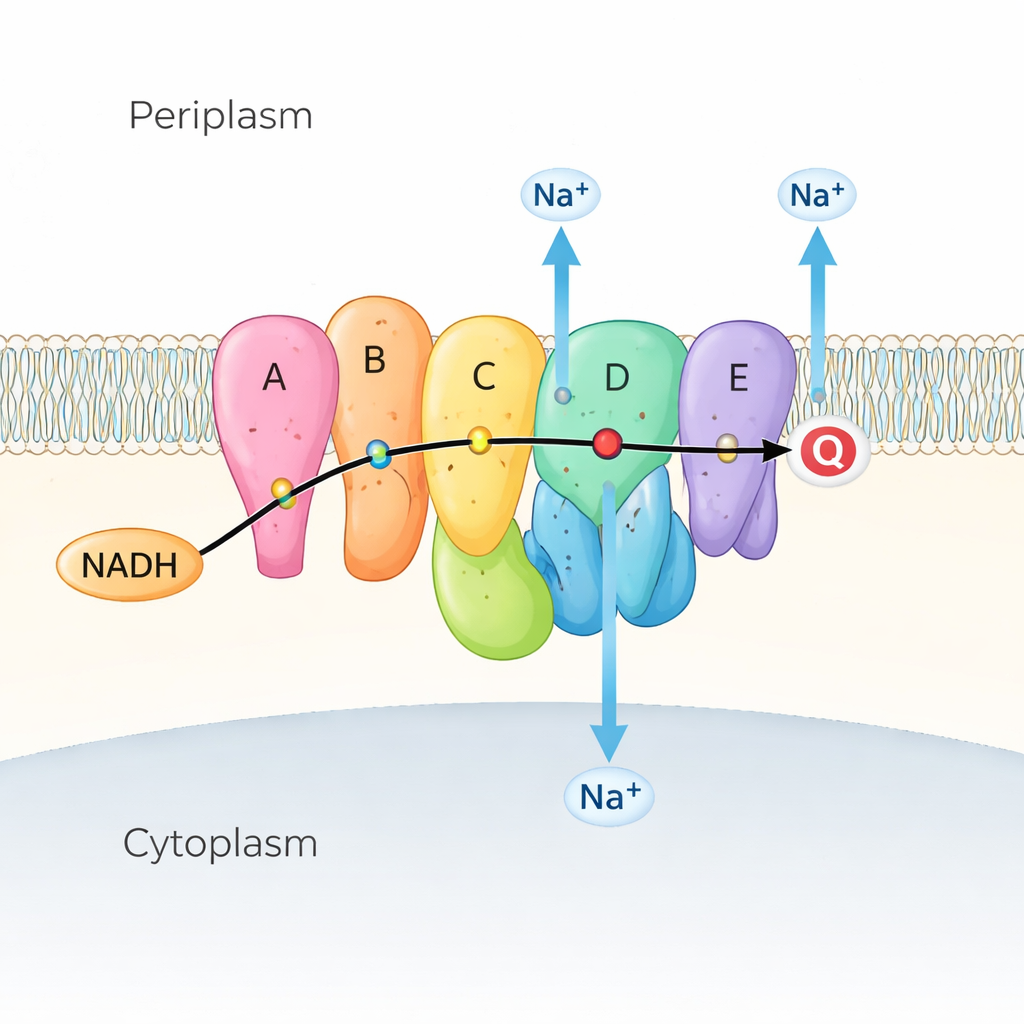
De machine in beweging zien
Eerdere röntgen- en cryo-elektronenmicroscopie-opnames toonden waar de subunits en cofactoren van Na⁺-NQR zitten, maar onthulden ook een raadsel: sommige kritieke elektronische overspringen waren te ver van elkaar verwijderd om efficiënt te kunnen verlopen tenzij het eiwit van vorm veranderde. De auteurs pakten dit aan door Na⁺-NQR in veel licht verschillende omstandigheden vast te leggen. Ze gebruikten mutanten die specifieke cofactoren wegnemen, medicijnen die de reactie in bepaalde stadia stilzetten, en oplossingen met en zonder natrium. Met hogeresolutie cryo-EM en geavanceerde beeldanalyse konden ze meerdere conformaties van hetzelfde enzym scheiden en reconstrueren, en zo statische opnames feitelijk omzetten in een film van zijn werkcyclus.
Een flexibele arm en een scharnierende klem
Een belangrijke bevinding betreft een flexibele cytoplasmatische subunit, NqrF, die twee elektrondragende cofactoren draagt. Het team identificeerde drie posities voor zijn "ferredoxine-achtige" domein — bijgenaamd de "omhoog", "midden" en "omlaag" toestanden. In de zeldzame maar cruciale "omlaag"-toestand zwaait dit kleine domein in een pocket gevormd door twee membraansubunits, NqrD en NqrE, waardoor zijn ijzer-zwavelcluster dichtbij genoeg komt om een elektron door te geven. Ondertussen gedraagt een periplasmatische (buiten) subunit, NqrC, zich als een beweegbare klem. In de ene conformatie ("stabiel") nestelt het zich tegen een andere membraansubunit, NqrB, gepositioneerd om elektronen naar de uiteindelijke quinonacceptor te sturen. In een tweede ("verplaatst") conformatie beweegt NqrC naar NqrD/E, waardoor zijn flavin-cofactor dichterbij komt om een elektron van hun ijzer-zwavelcentrum te accepteren. Deze bewegingen laten zien dat NqrF en NqrC fungeren als dynamische koeriers, die grote kloven in de cofactorketen overbruggen.
Hoe vormveranderingen natrium pompen
Het hart van de natriumpomp ligt in de gepaarde NqrD- en NqrE-subunits, die een centrale bundel van membraanoverspannende helixen vormen. Met behulp van zowel structuren als atomaire moleculaire dynamicasimulaties tonen de auteurs aan dat wanneer het ijzer-zwavelcluster in NqrD/E gereduceerd wordt (een elektron opneemt), er een negatief geladen plaats ontstaat die een Na⁺-ion en een paar watermoleculen van de cytoplasmatische kant aantrekt, en zo een tijdelijke bindingspocket vormt. Hydrofobe aminozuren boven en onder deze pocket werken als binnen- en buitengrenzen, die de toegang tot het ion regelen. Wanneer NqrD/E overschakelen van een "inwaarts-open" naar een "uitwaarts-open" vorm, beweegt de Na⁺ richting de periplasmatische zijde en wordt uiteindelijk losgelaten wanneer het ijzer-zwavelcluster weer geoxideerd wordt. Simulaties laten zien dat Na⁺ gedeeltelijk gehydrateerd blijft maar nooit een continue watergevulde tunnel ziet, wat suggereert dat het enzym stevig is afgesloten tegen ongewenst protonlekkage.
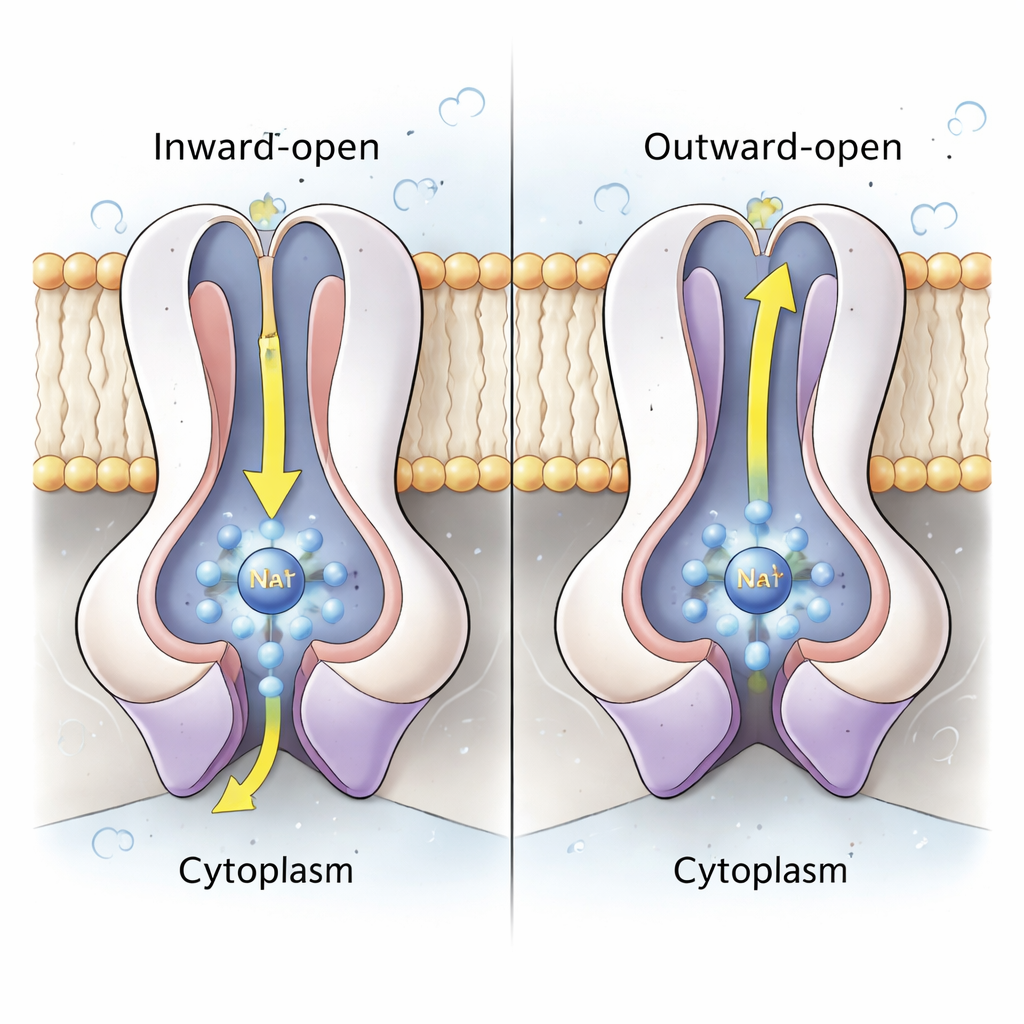
Een gecoördineerde cyclus die richting afdwingt
Door al hun structurele toestanden en simulaties te combineren, stellen de onderzoekers een zesstappen cyclus voor. NADH bindt eerst en doneert elektronen aan NqrF, dat vervolgens één elektron naar NqrD/E doorgeeft, waardoor Na⁺ uit het cytoplasma wordt opgenomen en de centrale pocket wordt geladen. De resulterende conformationele omschakeling van NqrD/E naar de uitwaarts-open vorm stoot zowel Na⁺ naar de periplasmale ruimte uit als stimuleert NqrC om in positie te komen om het elektron te accepteren. Vervolgens worden elektronen verder overgedragen naar de uiteindelijke flavine- en riboflavinecofactoren en tenslotte naar quinon, dat twee elektronen moet ontvangen om quinol te worden. Belangrijk is dat dezelfde vormveranderingen die Na⁺ verplaatsen, ook om de beurt NqrF en NqrC losser en stijver maken, waardoor voorwaartse elektronenstroom waarschijnlijker wordt alleen wanneer Na⁺ naar buiten wordt gepompt en terugslag wordt ontmoedigd. Deze koppeling helpt het enzym om Na⁺ tegen een bestaande gradiënt in te pompen, waardoor de bacteriële "batterij" opgeladen blijft.
Waarom dit van belang is voor geneeskunde en biologie
Voor niet-specialisten toont dit werk hoe het leven uiterst gechoreografeerde machines uit eiwitten bouwt, waarbij kleine ladingveranderingen grote, nuttige bewegingen veroorzaken. Voor onderzoek naar infectieziekten verduidelijkt het dat Na⁺-translocatie in Na⁺-NQR voornamelijk plaatsvindt via de NqrD/E-kern, en niet via de eerder verdachte NqrB-subunit. Dat inzicht verfijnt waar toekomstige medicijnen het beste kunnen binden om de motor die Vibrio cholerae en andere pathogenen aandrijft te verstoren, terwijl menselijke enzymen gespaard blijven. Breder gezien biedt de studie een structureel stappenplan voor hoe redoxreacties kunnen worden gekoppeld aan ionenpompen — een ontwerpprincipe dat de natuur in veel vormen van bioenergetische machines hergebruikt.
Bronvermelding: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Trefwoorden: zoutpompen, bacteriële ademhaling, Na+-NQR, cryo-EM, antibiotische doelwitten