Clear Sky Science · nl
Een synthetisch systeem voor RNA‑responsieve pyroptose gebaseerd op type III‑E CRISPR nuclease‑protease
Gevaarlijke celontploffingen omzetten in gerichte instrumenten
Ons lichaam verdedigt zich soms door geïnfecteerde of beschadigde cellen te laten exploderen in een felle vorm van zelfvernietiging, bekend als inflammatoire celdood. Deze explosie verwijdert niet alleen gevaarlijke cellen maar lokt ook het immuunsysteem. De nieuwe studie introduceert een synthetisch gen‑circuit, DAMAGE genoemd, dat de RNA‑boodschappen binnen een cel kan aflezen en beslist of die cel moet worden vernietigd. Door een microbieel verdedigingssysteem op ons eigen celdoodmachinerie aan te sluiten, tonen de onderzoekers een manier om selectief virus‑geïnfecteerde, kankercellen of verouderde cellen uit te schakelen terwijl gezonde buren gespaard blijven. 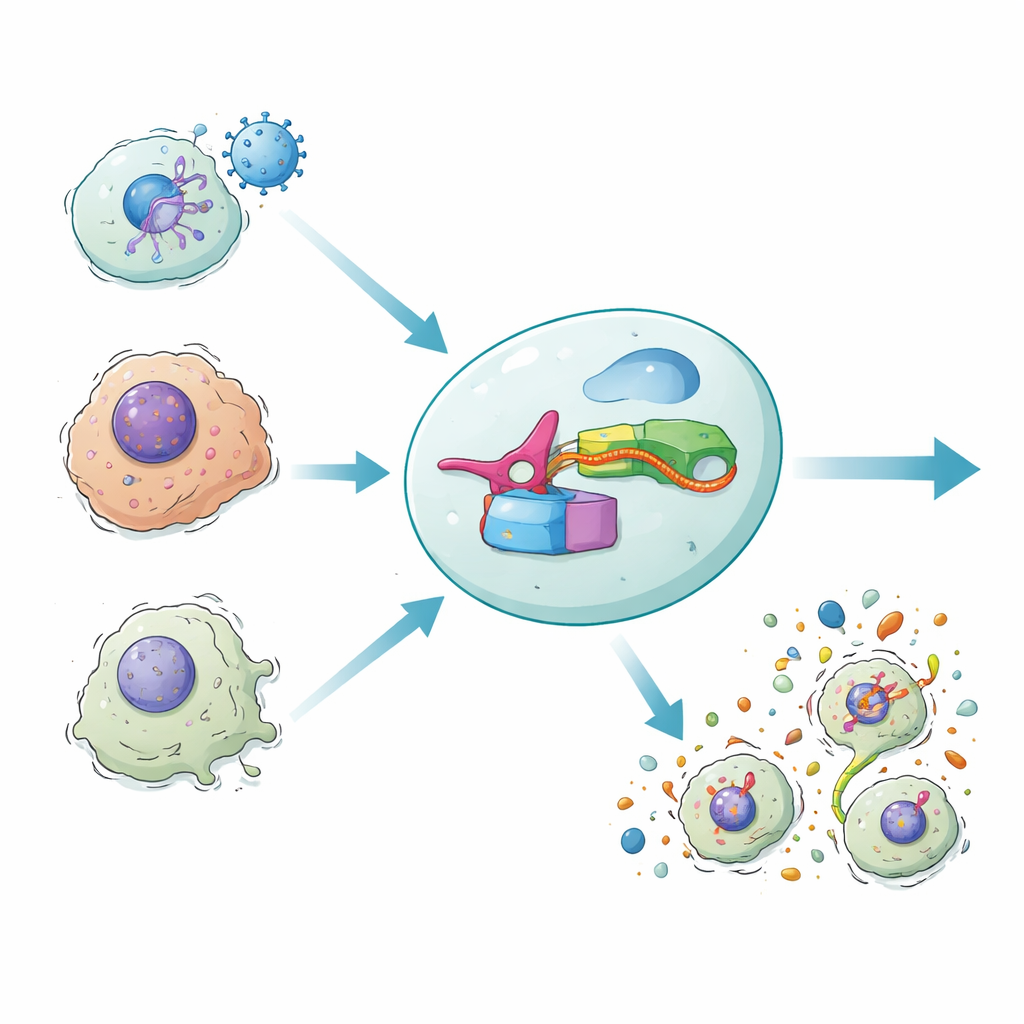
Hoe cellen normaal gesproken zichzelf opblazen
Bij inflammatoire celdood zit een familie eiwitten, bekend als gasderminen, in cellen als geladen ladingen. Elke gasdermine heeft een ‘‘dodelijk’’ voorste helft die gaten in celmembranen kan slaan, en een ‘‘veiligheidskap’’ achterste helft die de dader in bedwang houdt. Wanneer immuunsensoren gevaar detecteren, knippen enzymen gasderminen doormidden en laten de voorste helft vrij om poriën in het buitenste membraan te vormen. De cel zwelt op, barst en spuwt alarmstoffen uit die immuuncellen mobiliseren. Deze krachtige respons helpt bij de bestrijding van infecties en tumoren, maar het natuurlijke controlesysteem is complex en lastig te herprogrammeren voor therapie.
Bacteriële verdedigingen lenen om RNA te lezen
Bacteriën hebben compacte verdedigingsmodules ontwikkeld die we inmiddels kennen via CRISPR‑technologie. Eén daarvan, het type III‑E systeem, gebruikt een eiwit genaamd Cas7‑11 dat zich met behulp van een korte gids‑RNA aan specifieke RNA‑sequenties kan vastklampen. Wanneer Cas7‑11 een overeenkomend doel‑RNA vindt, schakelt het een hulpenzym, Csx29, aan dat een partnerproteïne, Csx30, knipt. De auteurs realiseerden zich dat Csx30 als een aanpasbare ‘‘scharnier’’ tussen twee eiwitdelen kon fungeren. Ze verbonden dit scharnier tussen de dodelijke en de veiligheidshelften van menselijke gasderminen, en creëerden kunstmatige uitvoerders die alleen uit elkaar worden gehaald wanneer de CRISPR‑achtige sensor hun gekozen RNA binnen een cel detecteert.
Een programmeerbare doodsschakelaar voor zieke cellen
Dit ontwerp, DAMAGE (Death Manipulation Gene) genoemd, bestaat uit vijf onderdelen: de Cas7‑11 sensor, de Csx29‑knipper, een gasdermine–Csx30 fusie, een gids‑RNA en het doel‑RNA in de cel. Wanneer het juiste RNA‑bericht verschijnt, bindt Cas7‑11 eraan, activeert Csx29 en knipt Csx29 het Csx30‑scharnier in het fusieproteïne. De dodelijke helft van gasdermine wordt vrijgelaten, boort poriën in het membraan en de cel sterft met een inflammatoire explosie. Door alleen het gids‑RNA te veranderen, stuurde het team DAMAGE naar verschillende cellulaire doelen. Ze toonden aan dat het RNA van respiratoir syncytieel virus, hoogrisico humaan papillomavirus in baarmoederhalskankercellen en meerdere kanker‑producerende KRAS‑mutaties kon herkennen die slechts op één letter van normaal RNA verschilden. In elk geval werden cellen met het verdachte RNA selectief uitgeschakeld, terwijl nabijgelegen controlecellen intact bleven. 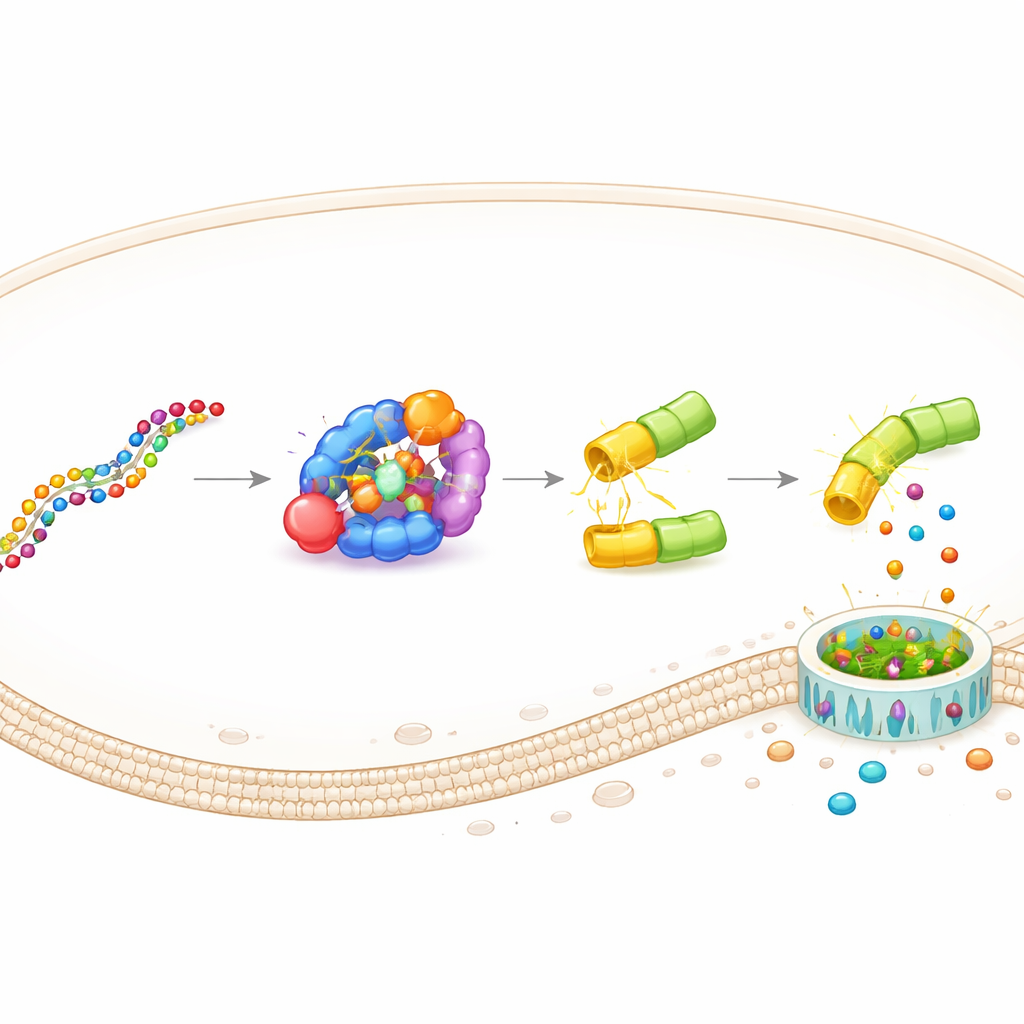
Richten op verouderde cellen
De onderzoekers vroegen zich ook af of DAMAGE senescente cellen—verouderde of gestreste cellen die stoppen met delen maar zich ophopen in weefsels en bijdragen aan kwetsbaarheid en chronische ziekte—kon opsporen. Zulke cellen verhogen vaak de productie van twee poortwachter‑eiwitten, p16 en p21. Door gidsen tegen de RNA’s voor p16 en p21 te programmeren, creëerde het team een versie genaamd DAMAGE‑Aging. Dit circuit doodde cellen met hoge niveaus van deze boodschappen, terwijl cellen waarin p16 genetisch was verwijderd gespaard bleven, wat bevestigt dat het systeem realtime RNA‑hoeveelheid leest in plaats van vaste DNA‑veranderingen. Medicamenteuze behandelingen die p16 of p21 verhoogden, maakten cellen gevoeliger voor deze gerichte zelfvernietiging.
Het systeem verpakken voor toekomstige therapieën
Om dichter bij praktisch gebruik te komen, codeerden de auteurs de vele DNA‑onderdelen van DAMAGE in een gestroomlijnd construct, DAMAGE‑Plus, en lieten zien dat het nog steeds betrouwbaar functioneerde. Daarna transcribeerden ze dit construct naar synthetisch mRNA, verpakte het in lipide‑nanodeeltjes vergelijkbaar met die in COVID‑19‑vaccins, en leverden het af in cellen in kweek. De mRNA‑versie assembleerde het circuit succesvol en veroorzaakte gerichte inflammatoire celdood in cellen met virale of kankergerelateerde RNA’s. Hoewel het geheel nog omvangrijk is en alleen in cellijnen is getest, wijzen deze resultaten erop dat programmeerbare, RNA‑geleid celdoden ooit via injecteerbare mRNA‑formuleringen zou kunnen worden ingezet.
Een nieuwe manier om cellulaire boodschappen te lezen en erop te reageren
In eenvoudige bewoordingen is DAMAGE een moleculaire portier die het interne RNA‑“ID” van elke cel controleert en alleen die eruit gooit die gevaarlijk lijken—virus‑geïnfecteerd, mutatie‑dragend of senescent—door ze in een explosieve vorm van zelfvernietiging te dwingen. Het werk toont aan dat bacteriële RNA‑sensoren met hoge precisie gekoppeld kunnen worden aan menselijke celdoodmachinerie, zelfs met onderscheid tot op één letters verschil in genetische boodschappen. Hoewel er veel engineering nodig is voordat zo’n systeem veilig in dieren of mensen gebruikt kan worden, schetst het een krachtige nieuwe strategie: de live RNA‑ruis binnen cellen aflezen en die direct vertalen naar beslissingen over leven of dood.
Bronvermelding: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
Trefwoorden: pyroptose, CRISPR, RNA‑gerichte therapie, kankerimmunotherapie, cellulaire veroudering