Clear Sky Science · nl
hnRNPM werkt samen met BCAS2 om alternatieve splicing te moduleren tijdens eicelontwikkeling
Waarom eicelkwaliteit ertoe doet
Elk menselijk leven begint met één enkele eicel, maar wetenschappers ontdekken nog steeds hoe deze uitzonderlijk grote cellen zich voorbereiden op het moment van bevruchting. Lang voordat zaadcellen arriveren, stapelen groeiende eicellen duizenden RNA-boodschappen op die hun rijping en de eerste dagen van embryo-ontwikkeling zullen aansturen. Deze studie onthult hoe een weinig bekend eiwit, samen met een partner, die boodschappen nauwkeurig bewerkt in muizeicellen — en wat er gebeurt wanneer dat bewerksysteem faalt.
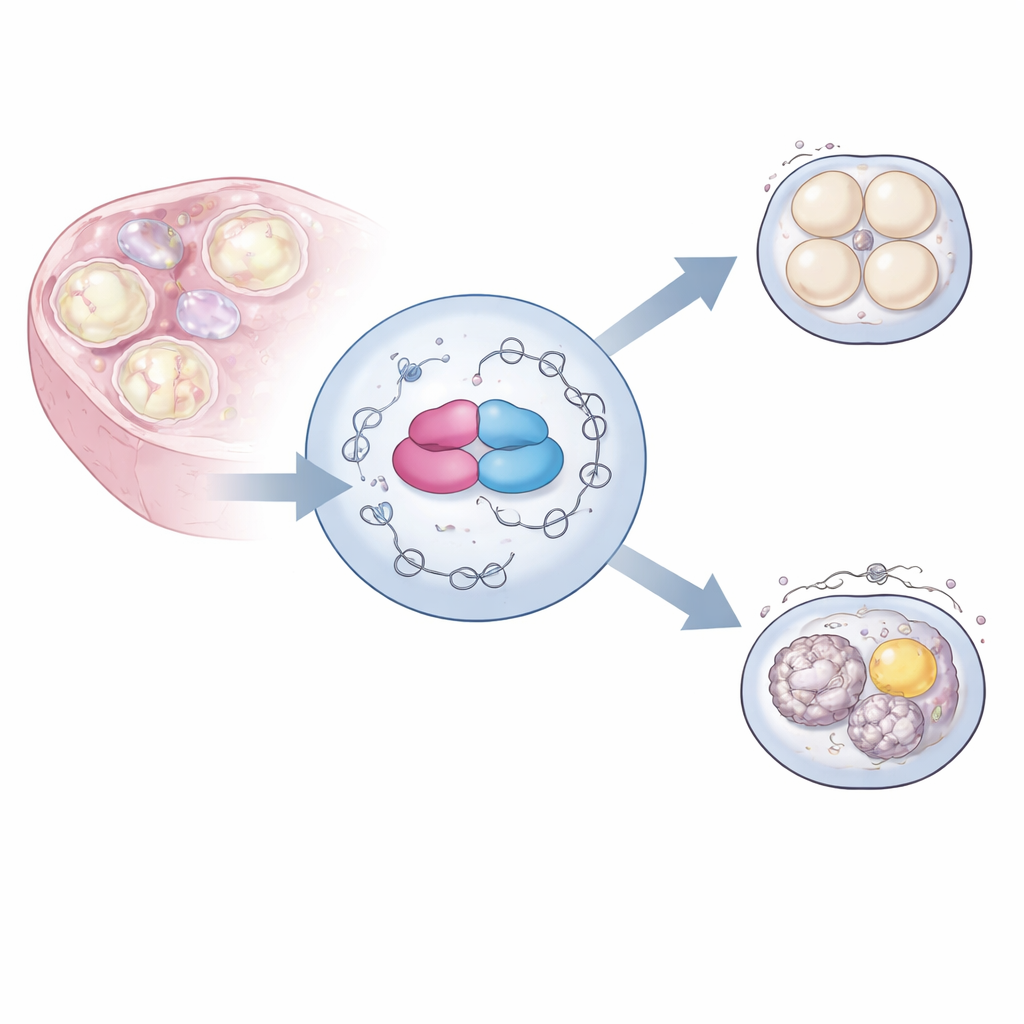
Poortwachters van genetische boodschappen
Eicellen groeien wekenlang in de eierstok terwijl hun DNA grotendeels stil blijft. In die periode bouwen ze een enorme bibliotheek van maternale RNA-boodschappen op die eerder van het genoom gekopieerd zijn. Deze boodschappen moeten op verschillende manieren worden bijgesneden en aan elkaar gezet, een proces dat alternatieve splicing wordt genoemd, om op precies het juiste moment de juiste mix van eiwitvarianten te produceren. De auteurs richtten zich op een eiwit genaamd hnRNPM, deel van een grote familie die RNA bindt, en op diens partner BCAS2, die beiden veel voorkomen in het vrouwelijke voortplantingssysteem. Eerder werk suggereerde dat deze eiwitten veel RNA’s in eicellen binden, maar hun precieze rol bij het bepalen van vruchtbaarheid bleef onduidelijk.
Wat er misgaat zonder deze redacteur
Om de functie van hnRNPM te onderzoeken, verwijderde het team met genetische manipulatie het Hnrnpm-gen specifiek uit muizeicelvoorlopers. De eierstokken van deze vrouwtjes zagen er normaal uit en produceerden vergelijkbare aantallen eicellen vergeleken met controles. Toen deze eicellen echter in het laboratorium werden bevrucht, ontwikkelden ze bijna nooit verder dan de eerste delingen, waardoor de vrouwtjes volledig onvruchtbaar waren. Nauwkeuriger onderzoek van de onrijpe eicellen toonde donkere klonten in het normaal heldere cytoplasma. Elektronenmicroscopie liet zien dat een fijn intern skelet, het cytoplasmatisch lattice, grotendeels ontbrak, en dat belangrijke organellen zoals mitochondriën en vetdruppels abnormaal geclusterd waren in plaats van gelijkmatig verdeeld. Deze veranderingen wezen op een diepgaand probleem met de interne organisatie van de eicel.
Gebroken celindelingsmachinerie
Dezelfde gemuteerde eicellen slaagden er ook niet goed in om meiose te voltooien, de speciale celdeling die het aantal chromosomen halveert. Wanneer onderzoekers de eicellen in cultuur lieten rijpen, konden ze de meiose starten, maar meestal stokte het proces voordat het voltooid was. Onder de microscoop waren de structuren die de chromosomen uit elkaar trekken — de spoelen — gedraaid, multipolair of slecht verankerd. Een eiwit genaamd pericentrin, dat helpt bij het organiseren van de spoelpolen, verscheen laat en op de verkeerde plekken. Samen betekenden deze defecten dat de eicellen chromosomen niet betrouwbaar konden opstellen en scheiden, wat waarschijnlijk de oorzaak is van het volledige ontwikkelingsfalen na bevruchting.
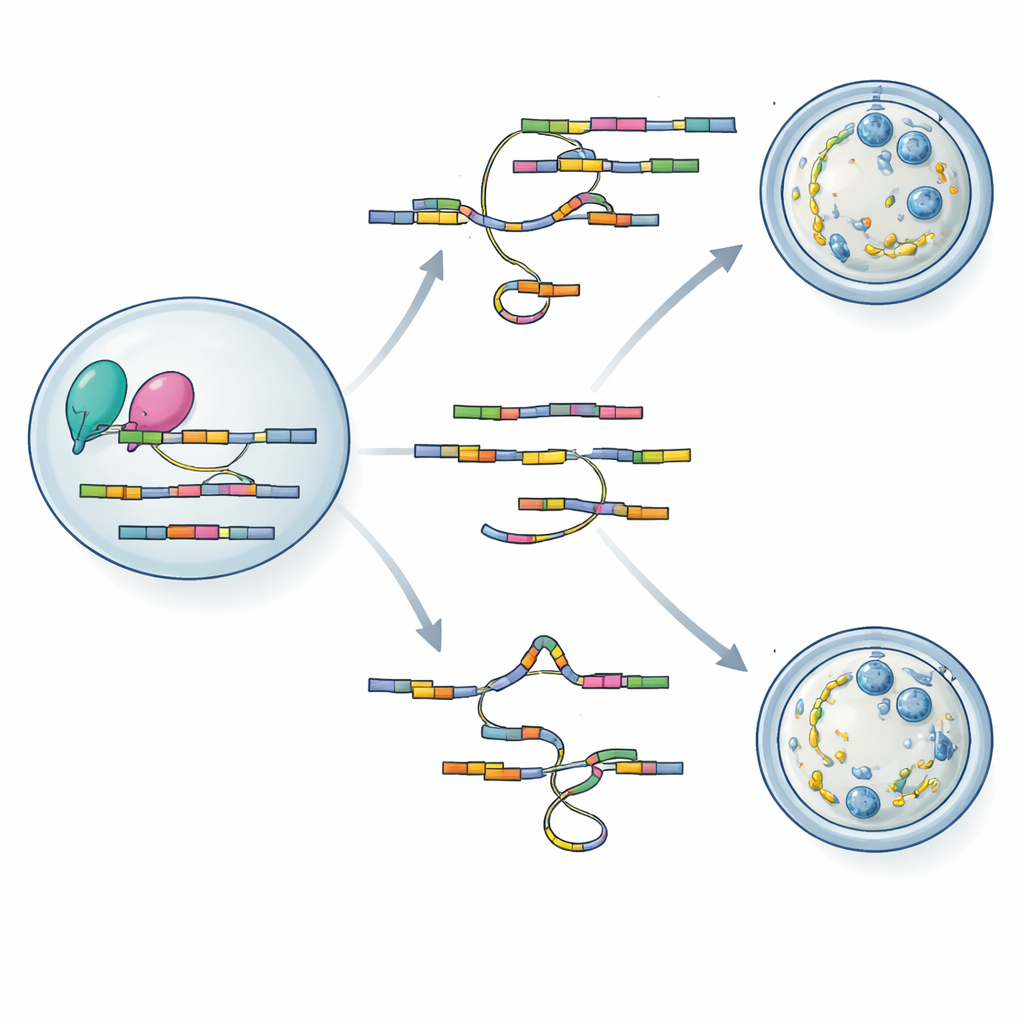
RNA-instructies lezen en herschrijven
Om te begrijpen hoe verlies van hnRNPM tot zulke ingrijpende defecten leidt, gebruikte het team twee krachtige sequencing-technieken aangepast voor kleine eicelmonsters. Met SCAN-seq, dat volledige RNA-moleculen van individuele oöcyten leest, ontdekten ze meer dan duizend splicing-veranderingen in gemuteerde eicellen, inclusief veel eerder onbekende RNA-varianten. Genen betrokken bij de opbouw van het cytoplasmatisch lattice, het beheersen van spoelgedrag en het reguleren van de meiotische celcyclus waren bijzonder getroffen. Een tweede methode, LACE-seq, bracht exact in kaart waar hnRNPM op RNA’s bindt en toonde een voorkeur voor GU-rijke reeksen binnen exonen. Door de twee datasets te combineren, lieten de auteurs zien dat hnRNPM direct op veel van de boodschappen zit waarvan de splicing verandert wanneer het eiwit ontbreekt, waarmee zijn bindingsactiviteit aan splicingnauwkeurigheid wordt gekoppeld.
Een samenwerkingsmodel voor eicelbeheersing
Proteïne-interactieonderzoek toonde aan dat hnRNPM fysiek geassocieerd is met BCAS2 en met kerncomponenten van het splicingmachinerie. De twee partners binden veel van dezelfde RNA-doelen en veranderen die vaak op vergelijkbare wijze wanneer een van beide eiwitten verstoord is. Intrigerend genoeg verminderde het verlies van hnRNPM de BCAS2-eiwitniveaus en verzwakte het de binding van BCAS2 aan gedeelde RNA-doelen, wat suggereert dat hnRNPM niet alleen boodschappen bewerkt maar ook helpt zijn partner op die boodschappen te stabiliseren. De auteurs stellen een model voor waarin hnRNPM en BCAS2 een coöperatief complex vormen dat tijdens de groei van de oöcyt sleutel-maternale RNA’s nauwkeurig afstemt, zodat het cytoplasmatisch lattice goed wordt opgebouwd en de meiotische deling betrouwbaar verloopt.
Wat dit betekent voor vruchtbaarheid
Kort gezegd laat dit werk zien dat een moleculair redactieteam — hnRNPM en BCAS2 — achter de schermen werkt om eicellen voor te bereiden op het leven na bevruchting. Wanneer dit team ontbreekt, stort het interne skelet van de eicel in, werkt het chromosoomscheidingsmechanisme niet goed meer en, ook al wordt de eicel in normale aantallen geproduceerd, kan zij de embryo-ontwikkeling niet ondersteunen. Omdat hnRNPM sterk vergelijkbaar is tussen muizen en mensen, wijzen deze bevindingen op een geconserveerd kwaliteitscontrolesysteem dat ten grondslag kan liggen aan bepaalde vormen van onverklaarde vrouwelijke onvruchtbaarheid en nieuwe aanknopingspunten kan bieden voor diagnose of behandeling.
Bronvermelding: Zhou, S., Liu, D., Gan, S. et al. hnRNPM cooperates with BCAS2 to modulate alternative splicing during oocyte development. Nat Commun 17, 2681 (2026). https://doi.org/10.1038/s41467-026-69176-8
Trefwoorden: eicelontwikkeling, alternatieve splicing, vrouwenonvruchtbaarheid, RNA-bindende eiwitten, cytoplasmatisch lattice