Clear Sky Science · nl
Ensembles op atomaire resolutie van intrinsiek ongeordende eiwitten met AlphaFold
Waarom ‘vormveranderende’ eiwitten ertoe doen
Onze cellen bevatten veel eiwitten die nooit in één vaste, stijve vorm blijven. Deze "intrinsiek ongeordende" eiwitten gedragen zich meer als slappe slierten dan als netjes gevouwen machines, en toch spelen ze een centrale rol in processen variërend van celsignalering tot neurodegeneratieve ziekten. Omdat ze voortdurend bewegen en buigen, is het vastleggen van hun volledige scala aan vormen op atomaire schaal uiterst moeilijk en vereist het meestal jaren van experimenten en zware berekeningen. Dit artikel presenteert een nieuwe manier om kunstmatige intelligentie en natuurkundige principes te combineren om deze rusteloze moleculen veel efficiënter in kaart te brengen.
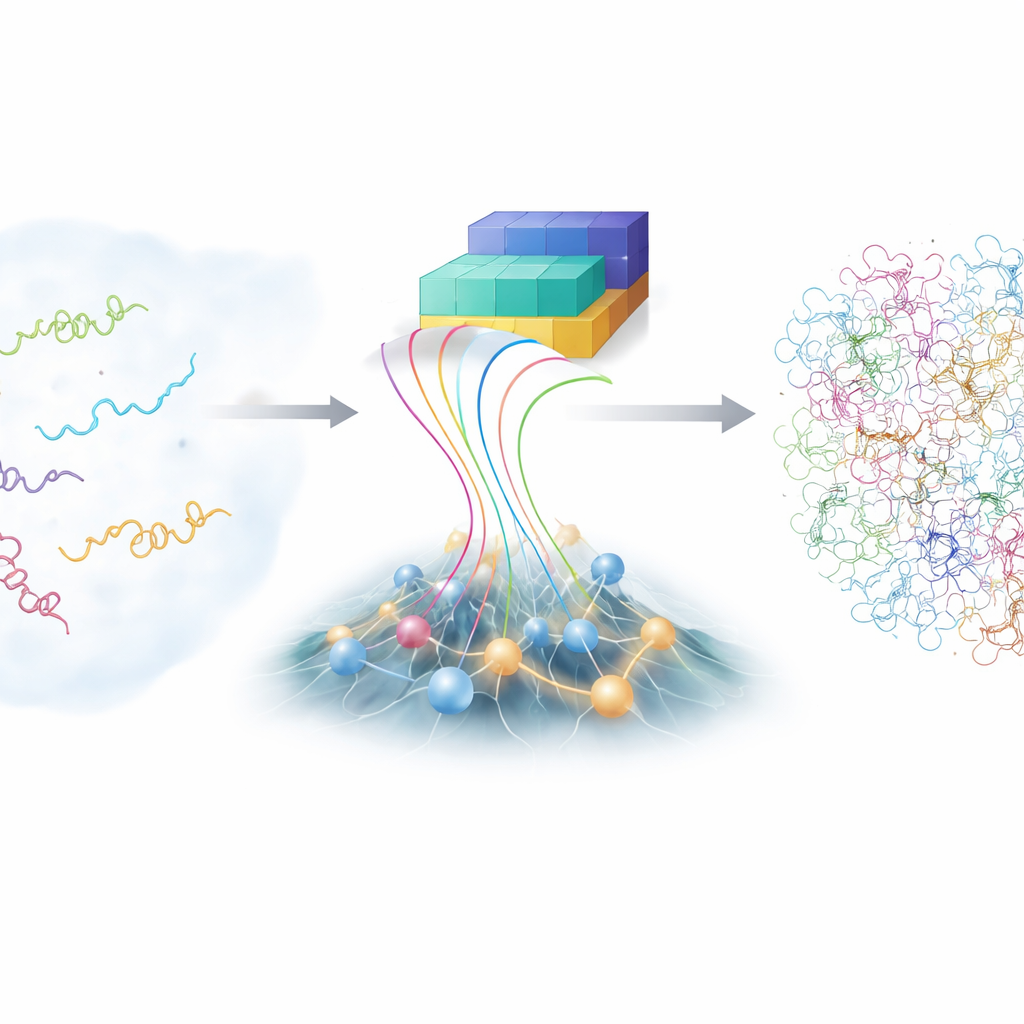
De uitdaging van rusteloze moleculen
In tegenstelling tot leerboekmodellen van eiwitten die één keurig structuur tonen, dwalen intrinsiek ongeordende eiwitten (IDP’s) door een uitgestrekt landschap van mogelijke vormen. Die flexibiliteit helpt hen om vele verschillende partners te herkennen, maar maakt ze ook berucht lastig te bestuderen. Traditionele laboratoriumtechnieken, zoals geavanceerde nucleaire magnetische resonantie en röntgenschittering, geven vaak informatie over gemiddelden over veel vormen, maar niet over elke afzonderlijke configuratie. Computersimulaties met volledige atomaire detail kunnen in principe elk atoom volgen terwijl een IDP kronkelt, maar ze zijn extreem duur en afhankelijk van fijn afgestelde fysische modellen. Daardoor beschikt de wetenschappelijke gemeenschap slechts over een beperkte verzameling nauwkeurige, gedetailleerde IDP-ensembles om van te leren.
Slimme gissingen combineren met fysische regels
In de afgelopen jaren heeft de AlphaFold-familie van deep-learningtools de biologie verrast door eiwitstructuren te voorspellen op basis van hun aminozuursequenties. Voor ongeordende eiwitten is AlphaFold’s gebruikelijke kracht—het raden van één beste vorm—echter minder behulpzaam, omdat IDP’s niet slechts één vorm hebben. Wat AlphaFold wél levert, is rijke informatie over hoe waarschijnlijk het is dat verschillende delen van de keten dicht bij of ver van elkaar zijn. De auteurs bouwden een nieuw kader, bAIes, dat deze door AI afgeleide informatie behandelt als zachte aanwijzingen en mengt met een snel, op fysica gebaseerd model dat bewust begint vanuit een "random coil"-perspectief, waarin de keten alle mogelijke buigingen en twists verkent zonder een specifieke structuur te bevoordelen.
Van willekeurige kluwens naar realistische ensembles
Eerst construeerden de onderzoekers een efficiënt fysisch model dat reproduceert hoe een volledig ongestructureerde eiwitketen zich gedraagt, gebaseerd op statistieken afgeleid uit duizenden bekende eiwitstructuren. Dit model dient als de "prior"—de basisverwachting van hoe een IDP beweegt als we niets anders weten. Vervolgens leest bAIes AlphaFold’s voorspellingen over welke residuparen de neiging hebben dicht bij elkaar te komen. In plaats van het eiwit in één patroon te dwingen, zet het die hints om in zachte afstandsrestricties met ingebouwde onzekerheid, waardoor de keten de AI-suggesties alleen volgt wanneer ze consistent zijn met het bredere fysische beeld.
Testen tegen echte experimenten
Om te beoordelen of deze aanpak werkt, pasten de onderzoekers bAIes toe op een set van 21 eiwitten die varieerden van vrijwel volledig random coils tot complexere systemen met tijdelijke helices en meerdere domeinen. Voor elk eiwit vergeleken ze de resulterende computergegenereerde ensembles met een breed scala aan experimentele metingen die zowel lokale details als globale grootte en vorm onderzoeken. Voor zeer slappe eiwitten zoals het aan Alzheimer gelinkte peptide Aβ40 was het eenvoudige random-coil-model al dicht bij de werkelijkheid, en bAIes handhaafde deze goede overeenkomst. Voor gedeeltelijk gestructureerde eiwitten verbeterde bAIes de overeenkomst met experimenten door correct vast te leggen waar korte helicale segmenten en compacte patches verschijnen en verdwijnen. Cruciaal is dat de methode robuust bleef, zelfs wanneer AlphaFold te veel vertrouwen toonde en ten onrechte stabiele vouwen voorspelde terwijl oplossingsexperimenten disorder lieten zien, omdat bAIes expliciet fouten in de AI-invoer toestaat.
Betere of gelijkwaardige prestaties ten opzichte van bestaande methoden
De auteurs zetten bAIes vervolgens af tegen zware all-atom-simulaties uitgevoerd op gespecialiseerde supercomputers, leidende coarse-grained modellen die eiwitten vereenvoudigen tot kralen, en nieuwe deep-learninggeneratoren getraind op simulatiedata. Over meerdere tests heen evenaarde of overtrof bAIes consequent deze benaderingen in het reproduceren van experimentele data, terwijl het veel minder rekenkundig veeleisend was dan grootschalige simulaties. Het werkte ook buiten eenvoudige IDP’s, door eiwitten met meerdere stijve domeinen verbonden door flexibele schakels aan te kunnen en hun algemene vormen in oplossing te herstellen. Wanneer de onderzoekers de bAIes-ensembles verder verfijnden met experimentele data, verbeterde de overeenkomst nog meer, wat aantoont dat de methode kan dienen als een krachtig uitgangspunt voor integratieve modellering.
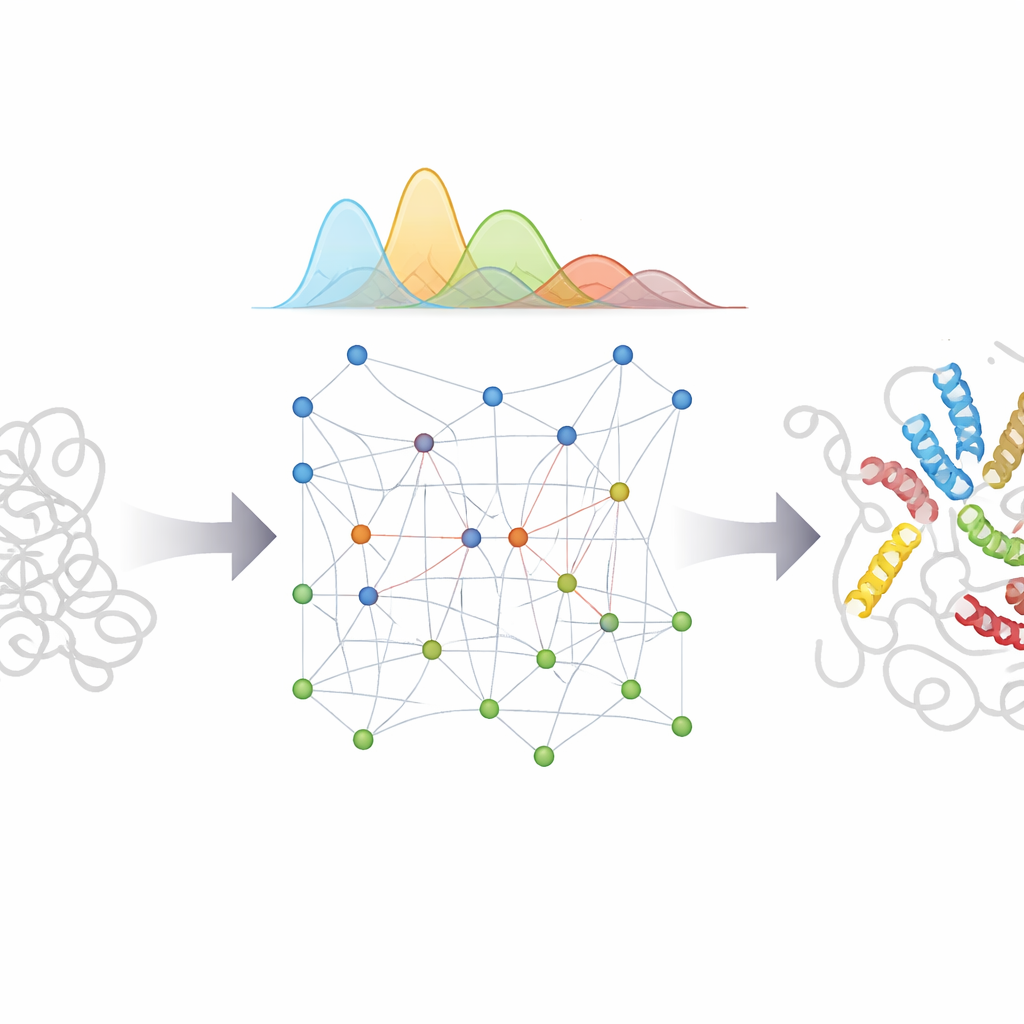
Wat dit betekent voor biologie en geneeskunde
Door AlphaFold’s patroonherkenningskracht te combineren met een zorgvuldig ontworpen fysisch model en een Bayesiaanse behandeling van onzekerheid, biedt bAIes een praktische route naar gedetailleerde "films" van ongeordende eiwitten in plaats van enkele momentopnames. Deze ensembles met atomaire detaillering kunnen wetenschappers helpen begrijpen hoe flexibele regio’s partners herkennen, hoe misvouwing en aggregatie beginnen bij ziekten zoals Parkinson en Alzheimer, en hoe kleine moleculen zich mogelijk binden aan ongrijpbare, veranderlijke doelen. Omdat de methode efficiënt is en is ingebouwd in open-sourcesoftware, kan ze breed worden toegepast om realistische ensembles voor vele ongeordende eiwitten te genereren, experimenten te sturen en toekomstige AI-systemen te ondersteunen die niet slechts één structuur willen voorspellen, maar het volledige scala aan vormen dat de meest flexibele moleculen van het leven kunnen aannemen.
Bronvermelding: Schnapka, V., Morozova, T.I., Sen, S. et al. Atomic resolution ensembles of intrinsically disordered proteins with Alphafold. Nat Commun 17, 2399 (2026). https://doi.org/10.1038/s41467-026-69172-y
Trefwoorden: intrinsiek ongeordende eiwitten, AlphaFold, Bayesiaanse modellering, eiwittenensembles, structurele biologie