Clear Sky Science · nl
Een multivalente adaptormechanisme stuurt de kernimport van proteasomen
Hoe cellen hun controlekamers schoon houden
In elke cel fungeert de kern als een commandocentrum, vol met DNA en de eiwitten die bepalen welke genen aan of uit staan. Om deze controlekamer goed te laten functioneren, vertrouwen cellen op krachtige moleculaire "versnippers" genaamd proteasomen die versleten of foutieve eiwitten afbreken. Dit artikel onthult hoe cellen de verrassend lastige taak klaren om deze forse proteasomen op het juiste moment door de smalle doorgangen naar de kern te krijgen.
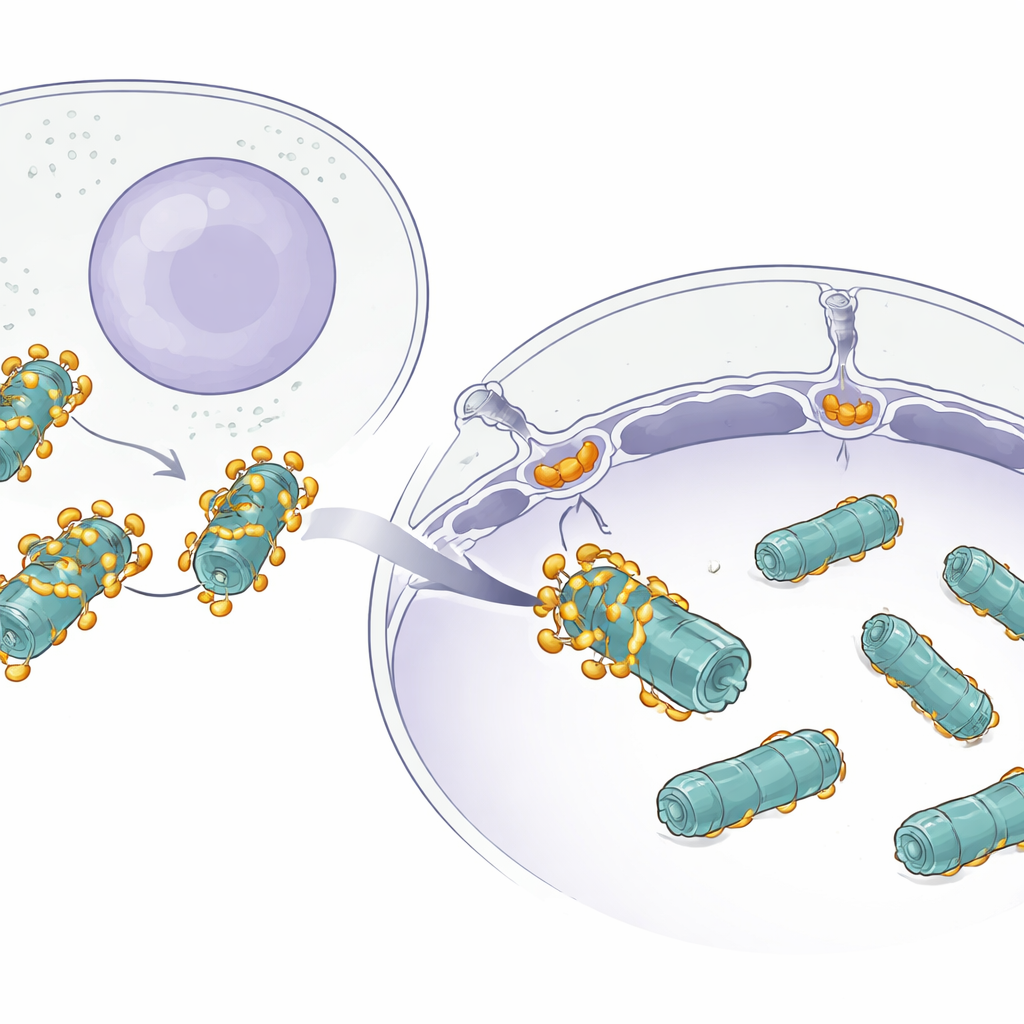
De uitdaging van het verplaatsen van grote machines
Veel eiwitten pendelen geruisloos tussen het hoofddeel van de cel en de kern via enorme deuropeningen in het kernmembraan, bekend als kernporiën. Kleine eiwitten kunnen makkelijk doorheen glippen, maar grote machines zoals proteasomen zijn anders: het zijn massieve, tonvormige complexen opgebouwd uit vele onderdelen. Terwijl al bekend was dat kleine ladingen hulp-eiwitten genaamd importines gebruiken om de kern binnen te komen, was onduidelijk hoe iets zo groots als een proteasoom efficiënt doorheen kan zonder vast te lopen of te verdwalen.
Een van vorm veranderende helper komt in zicht
Het team richtte zich op een klein, flexibeler eiwit genaamd AKIRIN2, waarvan eerder werk had aangetoond dat het absoluut noodzakelijk is voor proteasomen om de kern te betreden. Cellen die delen zonder AKIRIN2 kunnen proteasomen niet naar de kern brengen en sterven snel omdat beschadigde kern-eiwitten zich ophopen. Met een combinatie van methoden — waaronder een enorme mutatiescan die bijna elk aminozuur in AKIRIN2 veranderde, hoogresolutie cryo-elektronenmicroscopie om het complex in 3D te zien, en zorgvuldige biochemische testen — brachten de onderzoekers in kaart welke delen van AKIRIN2 belangrijk zijn en wat ze doen. Ze ontdekten een eerder onderschatte „vleugelachtige" segment en een gevlochten (coiled) regio die AKIRIN2 in staat stelt dimers (paren) te vormen, beide essentieel voor het grijpen van proteasomen en andere partners.
Bouwen van een meerhandig transporthandvat
De structurele beelden toonden dat meerdere kopieën van AKIRIN2 zich verzamelen aan één zijde van het proteasoom als vele handen die hetzelfde voorwerp vasthouden. Elk AKIRIN2-paar bindt aan specifieke plekken op het buitenoppervlak van het proteasoom terwijl het ook met verschillende importines interacteert. Eén importine, IPO9, houdt AKIRIN2 op een ongebruikelijke manier vast, wikkelt eromheen en verandert van vorm terwijl het complex assembleert. Andere importines, die zelf in paren werken, herkennen korte kerninvoersignalen die AKIRIN2 draagt. Omdat meerdere AKIRIN2-moleculen op hetzelfde proteasoom zitten, tonen ze collectief veel van deze signalen tegelijk. Dit multivalente "handvat" maakt het mogelijk dat een menigte importines zich gelijktijdig vastklampt, waardoor het enorme proteasoom genoeg trekkracht krijgt om door de kernporie te bewegen.
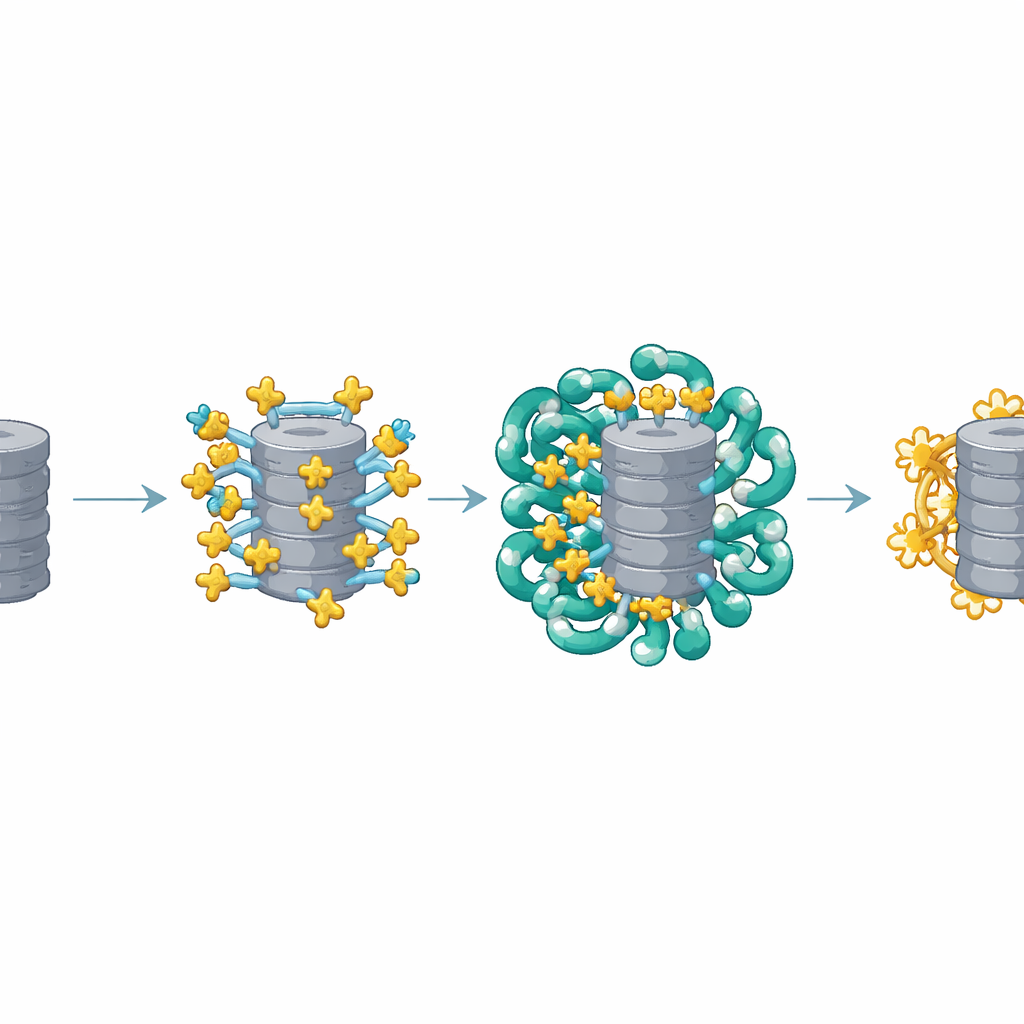
Een slimme assemblage- en loslaatcyclus
Hergebouwde experimenten in een vereenvoudigd reageerbuis-systeem lieten zien dat proteasomen alleen efficiënt de kern binnengaan wanneer zowel AKIRIN2 als importines samen aanwezig zijn. Hoe meer AKIRIN2, hoe sterker en sneller de import. Eenmaal binnenin de kern moet het transportapparaat worden opgeruimd zodat proteasomen kunnen werken. De cel gebruikt hier een tweestaps release. Een klein schakeleiwit genaamd Ran, in zijn GTP-gebonden vorm, trekt de meeste importines van hun lading af. AKIRIN2 en sommige IPO9 houden echter koppiger vast, maar de kern heeft een reserve: kernproteasomen zelf breken AKIRIN2 direct af, zonder de gebruikelijke ubiquitine-tag. Metingen gedurende de celdeling tonen dat AKIRIN2 piekt tijdens de celdeling, wanneer nieuwe kernen zich vormen, en vervolgens daalt in vroeg G1, in overeenstemming met deze gerichte opruiming.
Waarom dit verder belangrijk is dan één eiwit
Samen tonen deze bevindingen aan dat AKIRIN2 fungeert als een flexibel geraamte dat veel importines op een enkel proteasoom bijeenbrengt, waardoor een lastige transportopgave verandert in een gecoördineerde groepsinspanning. Door kerninvoersignalen op een adaptor te clusteren in plaats van op het proteasoom zelf, kunnen cellen regelen wanneer en hoe sterk grote machines de kern binnengaan zonder die machines te moeten herontwerpen. Vergelijkbare adaptor-gebaseerde strategieën blijken te worden gebruikt voor andere grote eiwitassemblages, en zelfs virussen benutten verwante trucs om de kern binnen te dringen. Het begrijpen van deze algemene transportlogica verdiept ons beeld van hoe cellen het eiwit-evenwicht in hun meest gevoelige compartiment behouden en kan uiteindelijk wijzen op nieuwe manieren om in te grijpen wanneer eiwitafbraak of kernfuncties ontsporen.
Bronvermelding: Brunner, H.L., Kalis, R.W., Grundmann, L. et al. A multivalent adaptor mechanism drives the nuclear import of proteasomes. Nat Commun 17, 2359 (2026). https://doi.org/10.1038/s41467-026-69162-0
Trefwoorden: nucleair transport, proteasoom, AKIRIN2, importine, eiwitafbraak