Clear Sky Science · nl
Een integratieve structurele-biologieaanpak onthult de dynamische organisatie van het R2SP quaternaire chaperoncomplex
Hoe cellen complexe moleculaire machines bouwen
In elke cel werken veel eiwitten niet alleen—ze moeten zich in elkaar klikken tot ingewikkelde machines voordat ze hun taken kunnen uitvoeren. Het goed laten verlopen van deze assemblage is essentieel voor gezond ademen, beweging en zelfs vruchtbaarheid. Dit artikel onderzoekt een van die assemblagehulpen, een moleculaire "bouwploeg" genaamd het R2SP-complex, en toont hoe het is georganiseerd en hoe het werkt. Inzicht in R2SP is belangrijk omdat wanneer de onderdelen falen, microscopisch kleine haarachtige structuren op cellen, cilia genoemd, niet goed bewegen, wat leidt tot chronische luchtwegklachten en andere ziekten.
De cellulaire bouwploegen R2TP en R2SP
Cellen vertrouwen op teams van hulpeiwitten, bekend als chaperoncomplexen, om andere eiwitten naar de juiste meerdelige vormen te begeleiden. Een lang bestudeerd team, R2TP genoemd, komt in veel weefsels voor en helpt bij de assemblage van grote machines zoals RNA‑producerende fabriekjes en DNA‑schadezoekers. R2SP is een nauwe verwant van R2TP: beide zijn opgebouwd rond dezelfde ringvormige motor, bestaande uit twee partnereiwitten, RUVBL1 en RUVBL2, die de energiemolecule ATP gebruiken. Wat verschilt, zijn de hulpadapters die klanten op deze motor aansluiten. R2TP gebruikt adapters RPAP3 en PIH1D1, terwijl R2SP SPAG1 en PIH1D2 inzet. Deze kleine verschillen in onderdelen geven de twee complexen verschillende klantenlijsten en koppelen R2SP specifiek aan de bouw van bewegende cilia die slijm en vloeistoffen over weefsels voortstuwen.
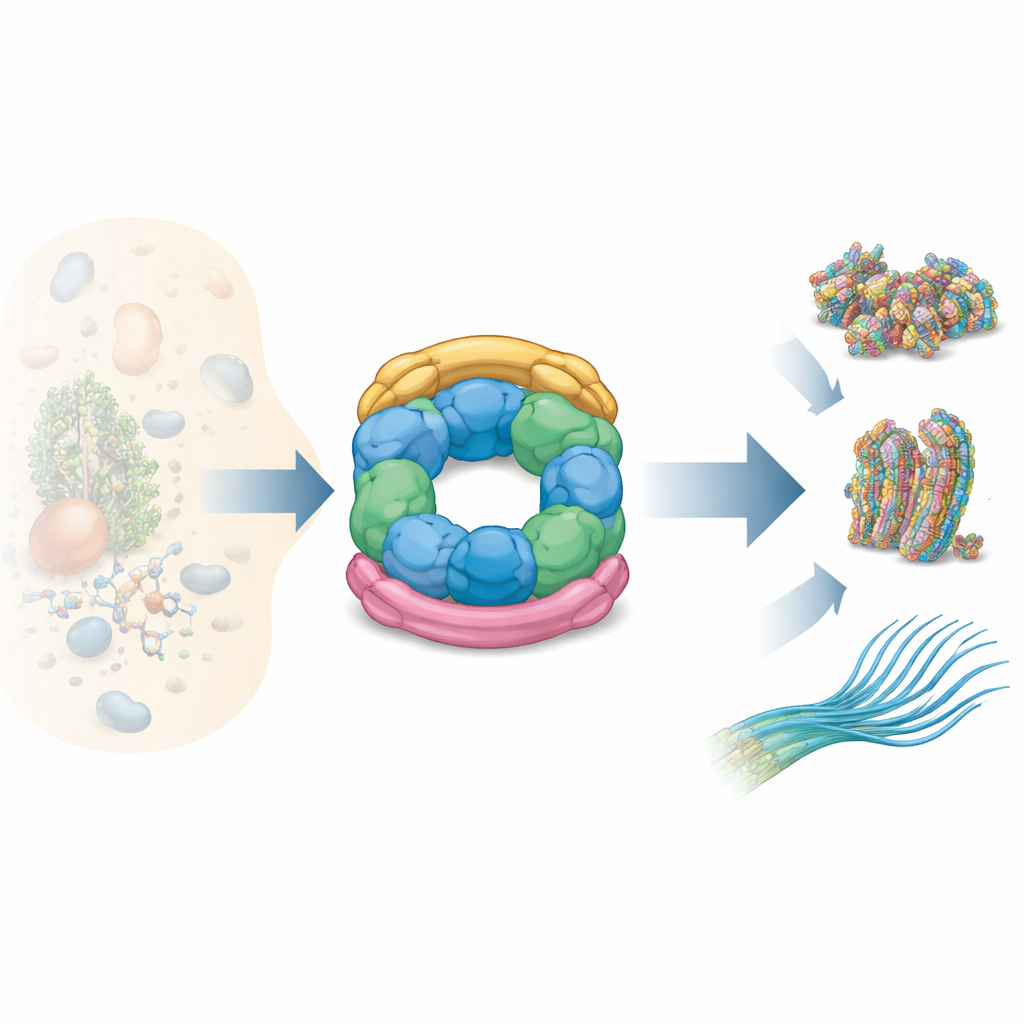
Hoe de R2SP‑onderdelen in elkaar passen
De auteurs combineerden meerdere structurele technieken—nucleaire magnetische resonantie, cryo‑elektronenmicroscopie en crosslinking‑massaspectrometrie—met biochemische tests om in kaart te brengen hoe R2SP is opgebouwd. Ze toonden aan dat het staartuiteinde van SPAG1 de RUVBL1/RUVBL2‑ring vastgrijpt op een manier die lijkt op hoe RPAP3 bindt in R2TP, maar met belangrijke aanpassingen in vorm en contactpunten. Een tweede adapter, PIH1D2, nestelt zich onder de ring en reikt ook omhoog om flexibele zijdomains van de motor aan te raken. Deze zijdomains werken als scharnierende armen die bewegingen van de ATP‑verbruikende kern naar gebonden klanten helpen overbrengen. De gegevens laten zien dat SPAG1 en PIH1D2 zich niet onafhankelijk hechten: ze werken samen, vormen een gekoppelde eenheid die de ring van boven en onder klemt en een karakteristieke driedimensionale architectuur stabiliseert.
Een dynamische ring die van versnelling verandert
Naast statische beelden vroeg het team hoe R2SP zich gedraagt. Met interactiemetingen vonden ze dat de RUVBL1/RUVBL2‑motor zowel als enkele ring als als gestapelde dubbelring kan voorkomen. Wanneer SPAG1 en PIH1D2 binden, verschuift dit evenwicht sterk naar de enkele‑ringvorm en kunnen er tot drie adapterparen op geplaatst worden. Tegelijkertijd verhogen de adapters de ATP‑verbrandingsactiviteit van de motor aanzienlijk en veranderen ze hoe snel ATP‑achtige moleculen aan de en van de actieve centra binden. In vergelijking met het R2TP‑systeem bevorderen SPAG1 en PIH1D2 andere stappen in het loslaten van nucleotiden, wat suggereert dat R2SP de energiefiets van de kernmotor op een eigen wijze afstemt. Dit fijn gecontroleerde energiegebruik wordt verondersteld de stapsgewijze assemblage van klantcomplexen aan te drijven die nodig zijn voor beweeglijke cilia.
Een flexibele platform voor het bouwen van ciliaonderdelen
Door al hun structurele beperkingen in één model te integreren, stellen de auteurs voor dat R2SP fungeert als een flexibel, veelarmig platform. De staart van SPAG1 verankert stevig bovenop de ring, terwijl andere delen ervan en de twee domeinen van PIH1D2 uitsteken naar de meer open, arm‑achtige zijde van de motor. Deze zijde is waar klanteiwitten en helper‑chaperonnes zoals HSP70 en HSP90 waarschijnlijk aanmeren. Omdat tot drie SPAG1–PIH1D2‑eenheden aan één ring kunnen hechten en de flexibele armen constant bewegen, lijkt het hele complex op een octopus waarvan de tentakels meerdere klantdelen tegelijk kunnen grijpen, coördineren en doorgeven om in grotere cilia‑structuren te worden ingebouwd.
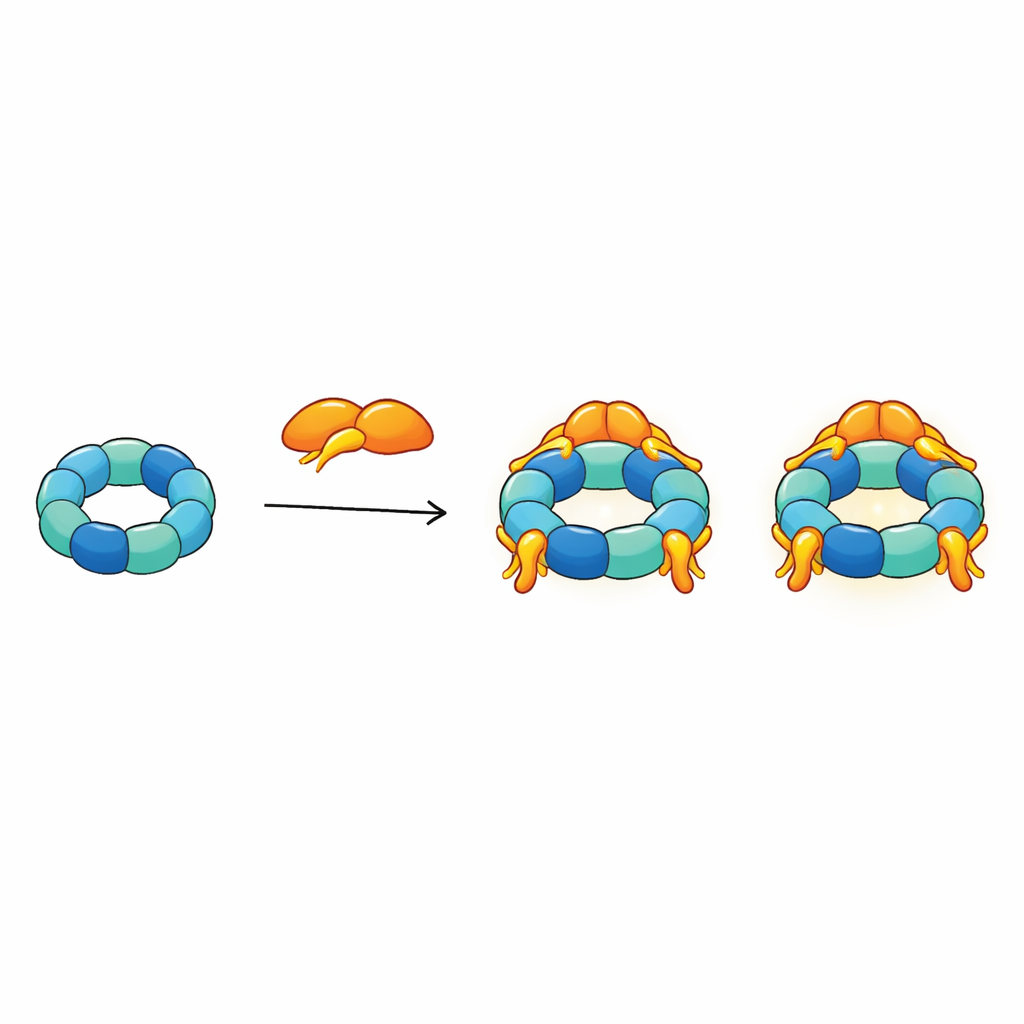
Wat dit betekent voor gezondheid en ziekte
Voor niet‑specialisten is de kernboodschap dat R2SP een gespecialiseerde versie is van een algemeen cellullair bouwmachien, herbedraad door het wisselen van slechts twee adaptereiwitten. Deze wissel verandert zowel hoe de centrale motor wordt aangestuurd als hoe klanten worden gepositioneerd, wat verklaart waarom R2SP zich richt op het bouwen van onderdelen voor beweeglijke cilia terwijl R2TP andere cellulaire fabrieken bedient. Defecten in SPAG1 zijn al bekend als oorzaak van primaire ciliaire dyskinesie, een aandoening gekenmerkt door chronische infecties en vruchtbaarheidsproblemen. Door R2SP’s gedetailleerde opbouw en werkingsprincipes te onthullen, legt deze studie de basis voor het begrijpen hoe specifieke mutaties de ciliaassemblage verstoren en kan ze uiteindelijk leiden tot gerichte behandelingen die deze cruciale moleculaire bouwploeg herstellen of moduleren.
Bronvermelding: Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
Trefwoorden: moleculaire chaperonnes, eiwitcomplexassemblage, bewegende trilharen, structurele biologie, RUVBL1 RUVBL2