Clear Sky Science · nl
Structurele basis van door TACO1 gefaciliteerde efficiënte mitochondriale translatie
De energiecentrales van de cel soepel laten draaien
Mitochondriën worden vaak de energiecentrales van onze cellen genoemd omdat ze het energiemolecuul ATP produceren. Hiervoor moeten ze een kleine maar cruciale set eiwitten bouwen met behulp van hun eigen gespecialiseerde eiwitfabrieken, de zogenoemde mitoribosomen. Deze studie onthult hoe een weinig bekend hulpstofje, TACO1, deze fabrieken fijn afstelt zodat ze soepel blijven draaien, vooral wanneer ze op bijzonder “lastige” reeksen in de eiwitketen stuiten die de machinerie doen vastlopen.
Energie‑fabrieken met eigen hardware
In tegenstelling tot de meeste eiwitsynthese, die plaatsvindt in het waterige binnenste van de cel, vindt mitochondriale eiwitproductie plaats op mitoribosomen die verankerd zijn aan het binnenmembraan van het mitochondrion—datzelfde membraan dat veel energieproducerende enzymen huisvest. Met behulp van geavanceerde cryo-elektronenmicroscopie op intacte menselijke mitochondriën verkregen de auteurs bijna-atomische momentopnamen van deze mitoribosomen in hun natuurlijke omgeving. Ze zagen dat alle vastgelegde mitoribosomen aan het binnenmembraan vastzaten en zo gepositioneerd waren dat pasgevormde eiwitketens rechtstreeks in een membraaninsertase konden worden geleid, een soort moleculaire opening die verse eiwitten in het membraan prikt waar ze nodig zijn voor energieproductie. 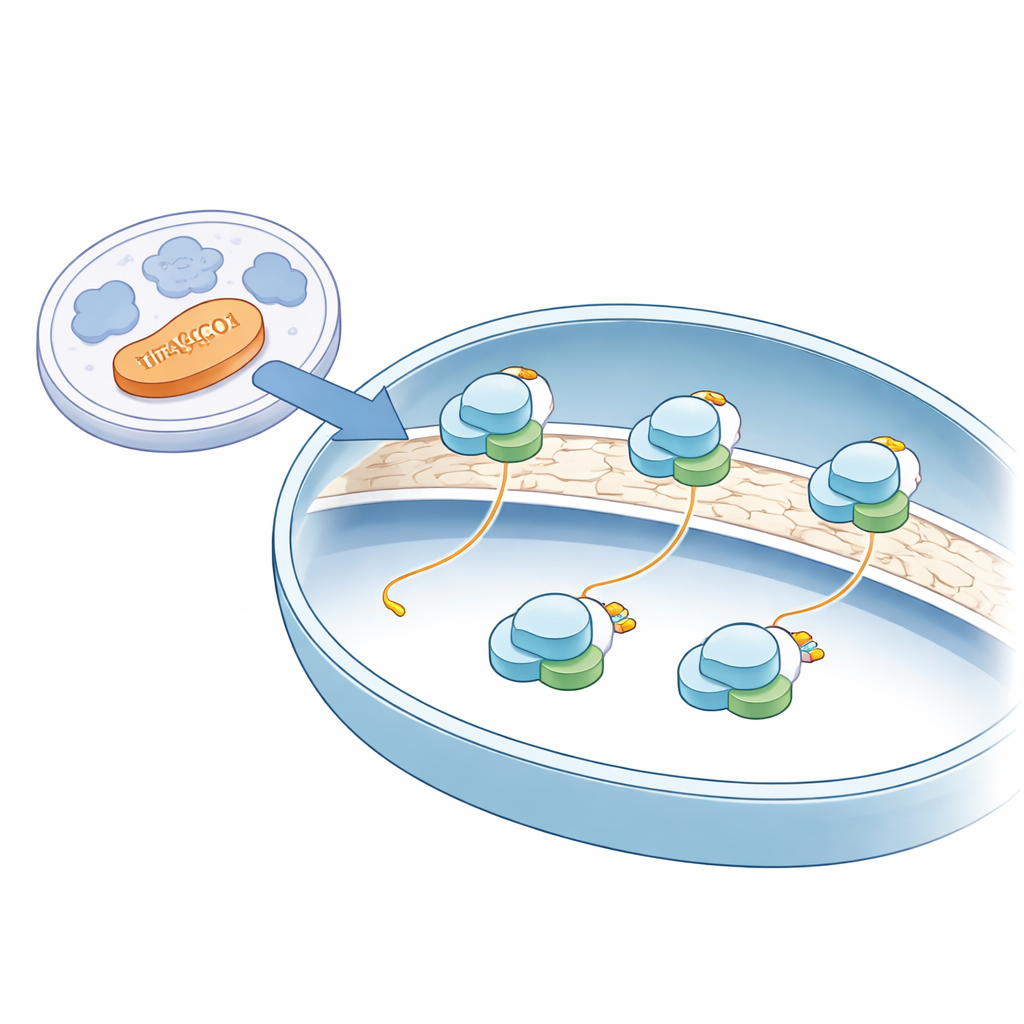
Een verborgen helper komt scherp in beeld
Tussen de ribosomale componenten, RNA-strengen en groeiende eiwitketens merkten de onderzoekers een extra dichtheidsveld op dat in eerdere, meer kunstmatige preparaten nooit was gezien. Door hun kaarten zorgvuldig te verfijnen en vormen te vergelijken met voorspelde eiwitstructuren, identificeerden ze dit mysteriecomponent als TACO1, een eiwit dat al aan menselijke mitochondriale ziekten was gekoppeld maar waarvan de fysieke rol onduidelijk bleef. De beelden toonden dat TACO1 zich genesteld heeft naast het deel van het ribosoom waar het volgende aminozuur‑dragende RNA (de A‑plaats tRNA) arriveert, waarbij het contact maakt met zowel ribosomaal RNA als verschillende ribosomale eiwitten. Deze plaatsing stelt TACO1 in staat bijna als een steun te fungeren, die het binnenkomende tRNA ondersteunt terwijl het ribosoom een nieuwe binding vormt om de eiwitketen te verlengen.
Verkeersopstoppingen op de eiwitproductielijn voorkomen
Eiwitopbouw verloopt cyclisch: een elongatiefactor (mtEF‑Tu) levert een geladen tRNA, het ribosoom controleert en gebruikt het, en de factor vertrekt zodat de volgende stap kan plaatsvinden. De auteurs vonden dat TACO1 zich bindt in grofweg hetzelfde gebied dat mtEF‑Tu gebruikt, en dat de twee factoren niet gelijktijdig op het ribosoom kunnen zitten. In normale cellen verkeerden veel mitoribosomen in een toestand waarin het nieuwe tRNA volledig op zijn plaats zit en de elongatie vordert. Wanneer het team mitochondriën van cellen zonder TACO1 onderzocht, zagen ze daarentegen een opeenhoping van ribosomen die vastzaten in een vroegere toestand waarin mtEF‑Tu nog vastzat en het nieuwe tRNA zich niet volledig had gezet. Biochemische experimenten bevestigden dat, zonder TACO1, mtEF‑Tu langer blijft hangen op actief vertalende ribosomen, en dat de grote en kleine subeenheden eerder uit elkaar drijven—tekens van vastgelopen of mislukte translatie. 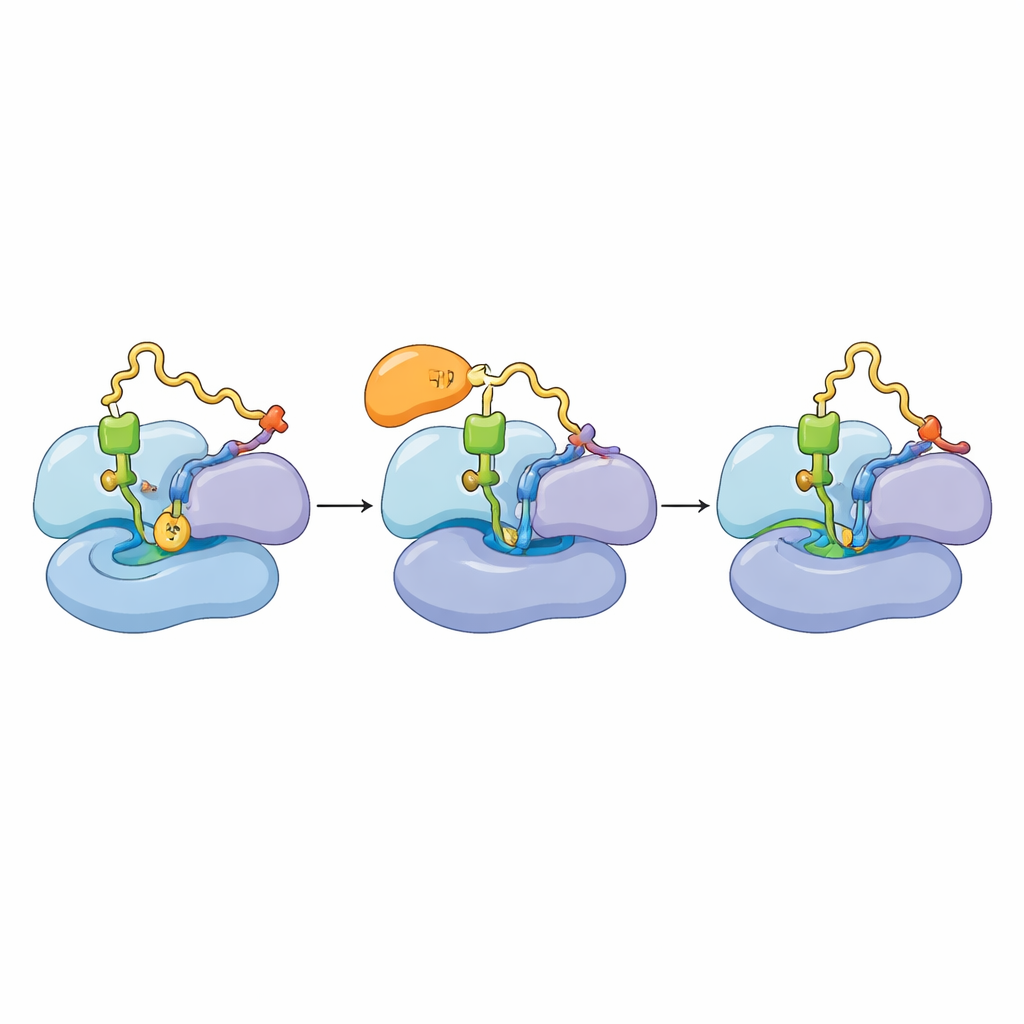
Waarom bepaalde eiwitreeksen zo problematisch zijn
Een van TACO1’s belangrijkste taken lijkt te zijn het helpen van het ribosoom bij het verwerken van reeksen van het aminozuur proline, die van nature de bindingsvorming vertragen vanwege de starre ringstructuur van proline. Eerder werk toonde aan dat TACO1 cruciaal is voor de productie van cytochroom c‑oxidase subeenheid 1, een kerncomponent van de energieketen die een zeldzame drievoudige‑proline‑motief bevat, en dat het verlies ervan een ineenstorting van dit energiecomplex en een menselijke hersenaandoening genaamd Leigh‑syndroom veroorzaakt. In bacteriën en in het belangrijkste cytoplasmatische systeem van de cel vervullen andere hulpfactoren een vergelijkbare anti‑stolfunctie, maar mitochondriën missen die conventionele factoren. Dit nieuwe structurele werk toont dat TACO1 zich heeft ontwikkeld als een mitochondriumspecifieke oplossing: door mtEF‑Tu opzij te duwen, het binnenkomende tRNA te stabiliseren en de bindingsvorming te ondersteunen, helpt het het mitoribosoom om deze lastige sequentiepatches voorbij te duwen in plaats van tot stilstand te komen.
Een oude strategie met moderne gezondheidsimplicaties
Buiten menselijke cellen worden aan TACO1 verwante eiwitten in veel bacteriën en andere organismen aangetroffen, en sommige van deze bacteriële varianten blijken nu ook ribosoom‑stagnatie te verlichten. Deze conservatie suggereert dat het gebruik van een TACO1‑achtig factor om trage of vastgelopen ribosomen te redden een oude strategie is om eiwitsynthese efficiënt te houden. Voor mensen biedt het werk een concreet, visueel verklaringsmodel waarom mutaties in TACO1 de energieproductie en het zenuwstelsel zo ernstig kunnen beschadigen, en het hint dat het manipuleren van TACO1 of diens verwanten ooit manieren kan bieden om mitochondriale translatie bij te sturen—of dat nu om mitochondriale ziekten te behandelen is of om schadelijke bacteriën te richten die op vergelijkbare stalling‑verlichtingssystemen vertrouwen.
Bronvermelding: Wang, S., Brischigliaro, M., Zhang, Y. et al. Structural basis of TACO1-mediated efficient mitochondrial translation. Nat Commun 17, 2521 (2026). https://doi.org/10.1038/s41467-026-69156-y
Trefwoorden: mitochondriale translatie, TACO1, mitoribosoom, ribosoom‑stagnatie, Leigh‑syndroom