Clear Sky Science · nl
Gecombineerde bacteriofaag- en antibioticatherapie bij therapieresistente peritoneale dialyse-gerelateerde peritonitis veroorzaakt door Klebsiella pneumoniae
Waarom dit infectieverhaal ertoe doet
Mensen bij wie de nieren het begeven vertrouwen vaak op peritoneale dialyse, een thuistoepassing die het bloed zacht reinigt met behulp van het buikvlies. Een ernstige complicatie van deze behandeling is peritonitis—een infectie in de buik—die pijnlijk, moeilijk te behandelen en zelfs levensbedreigend kan zijn. Nu sommige bacteriën minder goed reageren op standaardmedicijnen, zoeken artsen naar nieuwe manieren om deze kwetsbare patiënten te beschermen. Dit artikel beschrijft hoe een team van clinici en wetenschappers een virus dat bacteriën aanvalt, samen met antibiotica, gebruikte om een hardnekkige infectie bij een man met peritoneale dialyse succesvol te behandelen, en wat ze leerden door zijn reactie nauwgezet te volgen.
Een moeilijk te behandelen buikinfectie
De patiënt was een 71-jarige man met nierfalen die werd behandeld met continue ambulante peritoneale dialyse. Gedurende meerdere jaren had hij herhaaldelijk peritonitis, aanvankelijk veroorzaakt door veelvoorkomende huidbacteriën die zich aan de plastic katheter hechten en een slijmlaag of biofilm kunnen vormen. Om deze cyclus te doorbreken vervingen artsen zijn peritoneale dialysekatheter in één ingreep zodra de vloeistof helder werd, een strategie die simultane kathetervervanging wordt genoemd. Kort daarna ontwikkelde hij echter een nieuwe en ernstiger infectie: de dialysaatvloeistof werd opnieuw troebel en testen toonden Klebsiella pneumoniae aan, een Gram-negatieve bacterie die geassocieerd wordt met ernstiger ziekte, grotere kans op verlies van de katheter en verhoogd sterfterisico bij dialysepatiënten.
Wanneer antibiotica niet voldoende zijn
Laboratoriumtesten toonden aan dat deze Klebsiella-stam gevoelig bleef voor een paar krachtige antibiotica, waaronder amikacine en imipenem. Artsen gaven deze middelen rechtstreeks in de buikholte gedurende twee weken, naast andere ondersteunende medicijnen en een pil ter voorkoming van schimmelinfecties. Desondanks bleef de vloeistof troebel en bleven witte bloedcellen—immuuncellen die tijdens een infectie sterk toenemen—zeer hoog. Bacteriën bleven groeien in kweek, waarmee werd voldaan aan de definitie van therapieresistente peritonitis, waarvoor richtlijnen meestal aanraden de katheter te verwijderen en de patiënt over te zetten op hemodialyse. Omdat regelmatig reizen voor hemodialyse extreem belastend zou zijn geweest, onderzocht het team een experimenteel alternatief: bacteriofaagtherapie gericht op zijn eigen Klebsiella.
Virussen inzetten die op bacteriën jagen
Bacteriofagen, of faag, zijn virussen die bacteriën infecteren en doden maar geen menselijke cellen aanvallen. Uit een grote faagbibliotheek selecteerden de onderzoekers twee faag die de Klebsiella-stam van de patiënt herkenden. Genetische sequencing bevestigde dat deze faag puur lytisch waren—gebouwd om hun bacteriële gastheer te vernietigen, niet in stilte samen te leven—en dat ze geen genen droegen die gekoppeld zijn aan toxines of antibioticaresistentie. In het laboratorium doodde één faag de bacteriën snel, maar liet binnen enkele uren resistente overlevenden ontstaan. De tweede faag kon deze ontsnappers verwijderen. Gezamenlijk gebruikt als cocktail onderdrukten ze de bacteriegroei gedurende een volle dag of langer. In combinatie met lage doses imipenem ruimde de faagcocktail de bacteriën sterker op dan een van beide behandelingen afzonderlijk, wat een duidelijke synergie tussen het virusmengsel en het antibioticum aantoonde.
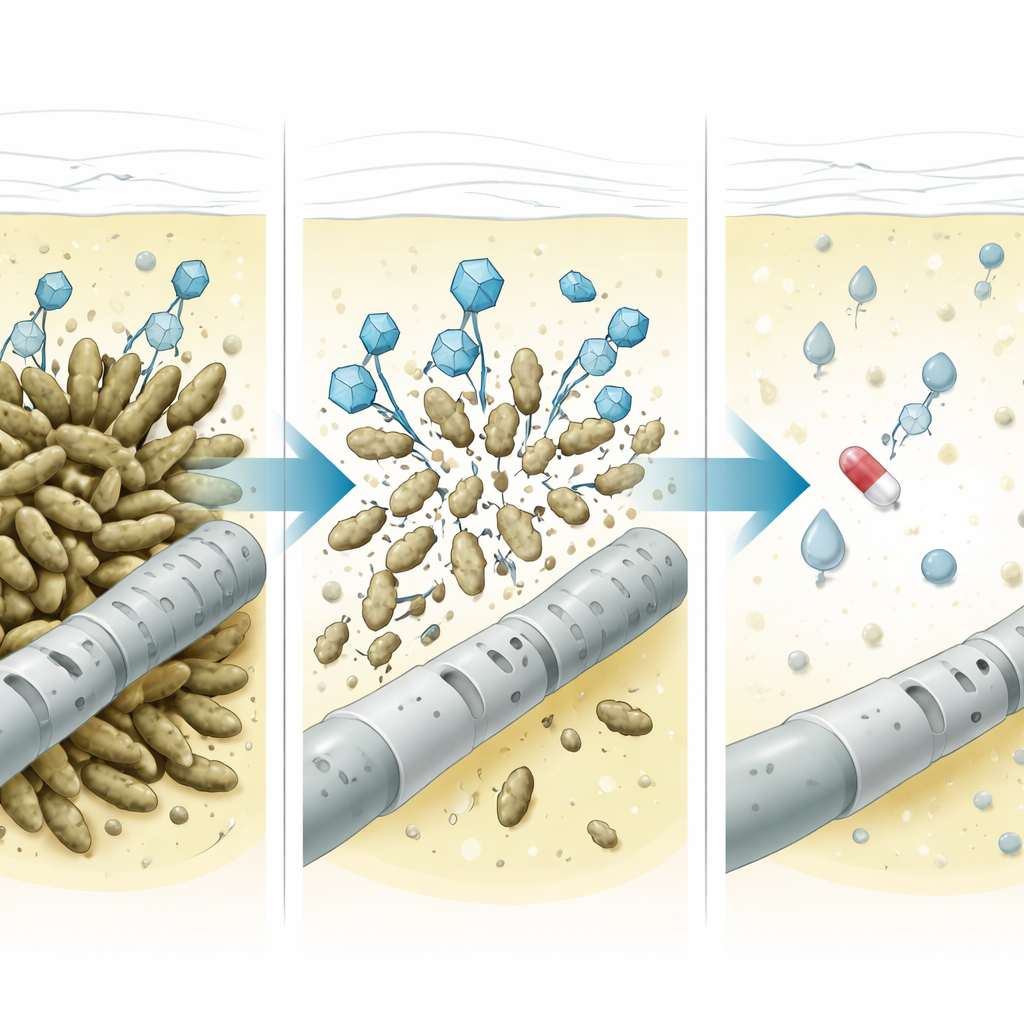
Wat er in de buik gebeurde
Artsen infuseerden de faagcocktail twee keer per dag gedurende drie dagen in de peritoneale holte, terwijl ze intraperitoneaal imipenem en orale fluconazol bleven toedienen. Daarna volgden ze zorgvuldig verschillende signalen in de afvloeiingsvloeistof. De tellingen witte bloedcellen schommelden aanvankelijk maar daalden al snel sterk, en Klebsiella stopte met groeien in kweek. Interleukine-6, een eiwit dat lokale ontsteking weerspiegelt, begon zeer hoog, piekte kort tijdens de faagbehandeling—waarschijnlijk doordat bacteriën uiteenbarstten en hun inhoud vrijgaven—en daalde vervolgens gestaag naar lage niveaus. Lipopolysaccharide, een onderdeel van de buitenmantel van Gram-negatieve bacteriën en een sterke trigger van immuunreacties, liet een vergelijkbaar patroon zien: hoog vóór therapie, een kleine verhoging tijdens bacteriële afbraak, waarna het daalde tot ondetecteerbare niveaus. Het team zocht ook naar neutraliserende antilichamen—immuunmoleculen die de faag zouden kunnen blokkeren—en vond geen significante toename in de peritoneale vloeistof. Faagniveaus zelf daalden ongeveer tienduizendvoudig binnen een dag en werden binnen 48 uur ondetecteerbaar, wat past bij het beeld van virussen die hun werk doen en daarna verdwijnen.
Inzichten uit andere patiënten
Om dit verhaal in context te plaatsen, bekeken de auteurs alle gepubliceerde gevallen van humane infecties veroorzaakt door Klebsiella pneumoniae die met faag werden behandeld. Ze vonden 14 patiënten wereldwijd, met infecties van de urinewegen, longen, botten, gewrichten en hersenvliezen. Bij 13 hiervan verbeterden de symptomen of raakte de infectie opgeruimd, en slechts één geval reageerde niet. De meeste patiënten kregen faag samen met antibiotica, hoewel enkelen uitsluitend met faag werden behandeld. In deze rapporten waren ernstige bijwerkingen zeldzaam, wat ondersteunt dat zorgvuldig bereide faagtherapieën veilig kunnen zijn wanneer ze nauwlettend worden gemonitord.
Wat dit kan betekenen voor toekomstige zorg
Na drie weken gecombineerde faag- en antibioticabehandeling was de buikinfectie van de patiënt verdwenen, normaliseerden zijn ontstekingsmarkers en werd hij ontslagen zonder verdere antibiotica. Bij controle na een maand was er geen aanwijzing voor terugkeer en kon hij op peritoneale dialyse blijven. Dit enkele geval kan niet bewijzen dat faagtherapie bij elke dialysepatiënt met therapieresistente peritonitis zal werken, en de auteurs benadrukken de noodzaak van grotere studies, betere detectiemethoden voor ziekteverwekkers en diepgaander onderzoek naar hoe faag met het immuunsysteem interageren. Desondanks laat hun ervaring zien dat gepersonaliseerde faagcocktails, weloverwogen gecombineerd met effectieve antibiotica, een waardevolle reddingsoptie kunnen bieden wanneer standaardbehandelingen falen en het verwijderen van de katheter desastreuze gevolgen zou hebben voor iemands kwaliteit van leven.
Bronvermelding: Yang, X., Wu, N., Jiang, X. et al. Combined bacteriophage and antibiotic therapy for refractory peritoneal dialysis-related peritonitis caused by Klebsiella pneumoniae. Nat Commun 17, 2468 (2026). https://doi.org/10.1038/s41467-026-69154-0
Trefwoorden: faagtherapie, peritoneale dialyse, Klebsiella pneumoniae, antibioticaresistentie, peritonitis