Clear Sky Science · nl
Moleculair mechanisme van fosfaatimport door de bacteriële PstSCAB-transporter
Waarom kleine voedingsstoffen ertoe doen
Elke levende cel, van menselijke neuronen tot bodem-bacteriën, draait op fosfor. Dit element helpt bij het opslaan van energie, het bouwen van DNA en het behouden van celmembranen. In de omgeving is bruikbaar fosfaat—de vorm van fosfor die cellen daadwerkelijk kunnen opnemen—echter vaak schaars. Veel ziekteverwekkende bacteriën zijn afhankelijk van een extreem efficiënt moleculair apparaat, de PstSCAB-transporter, om fosfaat te verzamelen wanneer het ontbreekt. Begrijpen hoe dit apparaat precies werkt is niet alleen een fundamentele wetenschappelijke vraag; het kan ook nieuwe wegen openen om infecties te verzwakken door bacteriën van deze essentiële voedingsstof te beroven.
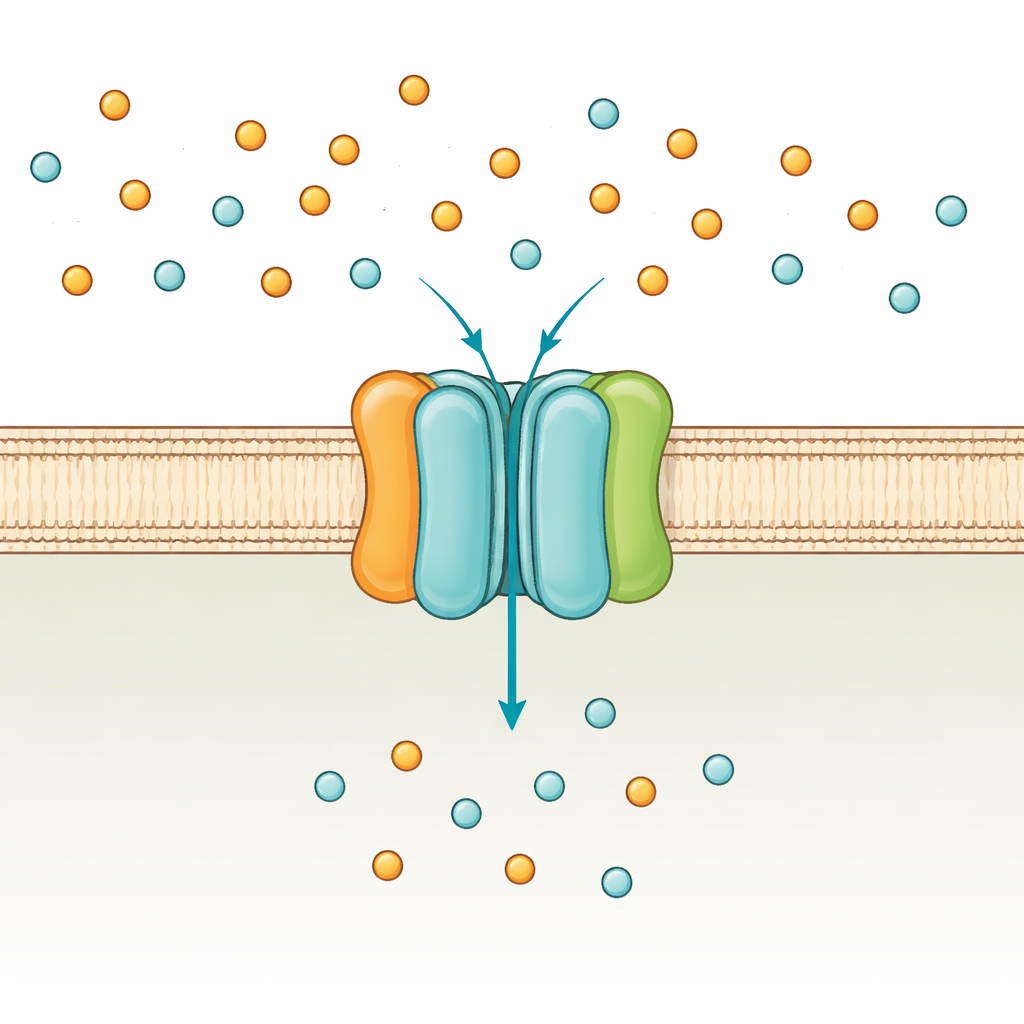
De fosfaatpoortwachter van de cel
Bacteriën zoals Escherichia coli gebruiken twee hoofdroutes om fosfaat op te nemen: een laag-affiniteitssysteem dat werkt wanneer fosfaat in overvloed is, en het hoog-affiniteitssysteem PstSCAB dat actief wordt bij schaarste. PstSCAB zit in het celmembraan en wordt aangedreven door ATP, de universele energievaluta van de cel. Het bestaat uit vijf onderdelen: twee membraangebonden subunits (PstA en PstC) die het doorgangsporto vormen, een oplosbaar ‘vanger’-eiwit buiten het membraan (PstS) dat fosfaat grijpt, en een paar interne subunits (PstB) die ATP verbranden om transport aan te drijven. Omdat dit systeem ook veel genen regelt die samenhangen met bacteriële virulentie, kunnen mutaties in PstSCAB ziekteverwekkers verzwakken die urineweginfecties, sepsis bij vee en tuberculose veroorzaken.
Het apparaat in actie vastleggen
Tot nu toe hadden wetenschappers slechts gedeeltelijke beelden van PstSCAB, grotendeels van het vanger-eiwit PstS afzonderlijk. In deze studie gebruikten de onderzoekers cryo-elektronenmicroscopie met hoge resolutie om de volledige transporter in verschillende sleutelstappen van zijn werkcyclus te visualiseren. Ze herbouwden de bacteriële eiwitten in kunstmatige membraan-„nanodiscs” en vroren ze zo snel in dat de moleculen in beweging gevangen raakten. Door de eiwitten zorgvuldig te manipuleren en ATP toe te voegen of weg te laten, verkregen ze structuren van drie hoofdtoestanden: een rustende inwaarts gerichte vorm zonder de vanger, een pretranslocatiestaat waarin fosfaat-beladen PstS op het membraankomplex aanlegt, en een ATP-gebonden katalytisch intermediair waarin fosfaat binnenin de transporter wordt vastgehouden.
Hoe vormveranderingen fosfaat verplaatsen
De beelden tonen hoe gecoördineerde vormveranderingen fosfaat van buiten naar binnen verplaatsen. In de rusttoestand opent het kanaal gevormd door PstA en PstC alleen naar het celinterieur; de buitenzijde is afgesloten door een set ‘‘poort’’-residuen, waardoor fosfaat nog niet van buiten kan binnenkomen. Wanneer fosfaat-beladen PstS in de pretranslocatiestaat aanlegt, nestelt het zich tussen flexibele lussen van PstA en PstC maar, opvallend genoeg, veranderen de membraansubunits nauwelijks van vorm. De echte verschuiving treedt op wanneer PstS zijn twee lobben begint te openen om fosfaat los te laten en tegelijkertijd de twee PstB-subunits naar elkaar zwaaien om ATP te binden. Deze ATP-binding klemmt PstB in een dimer en trekt aan verbindingshelixen in PstA en PstC, waardoor de hele porie omslaat naar een naar buiten gerichte conformatie die een specifiek fosfaatbindend pocket aan de buitenzijde blootlegt.
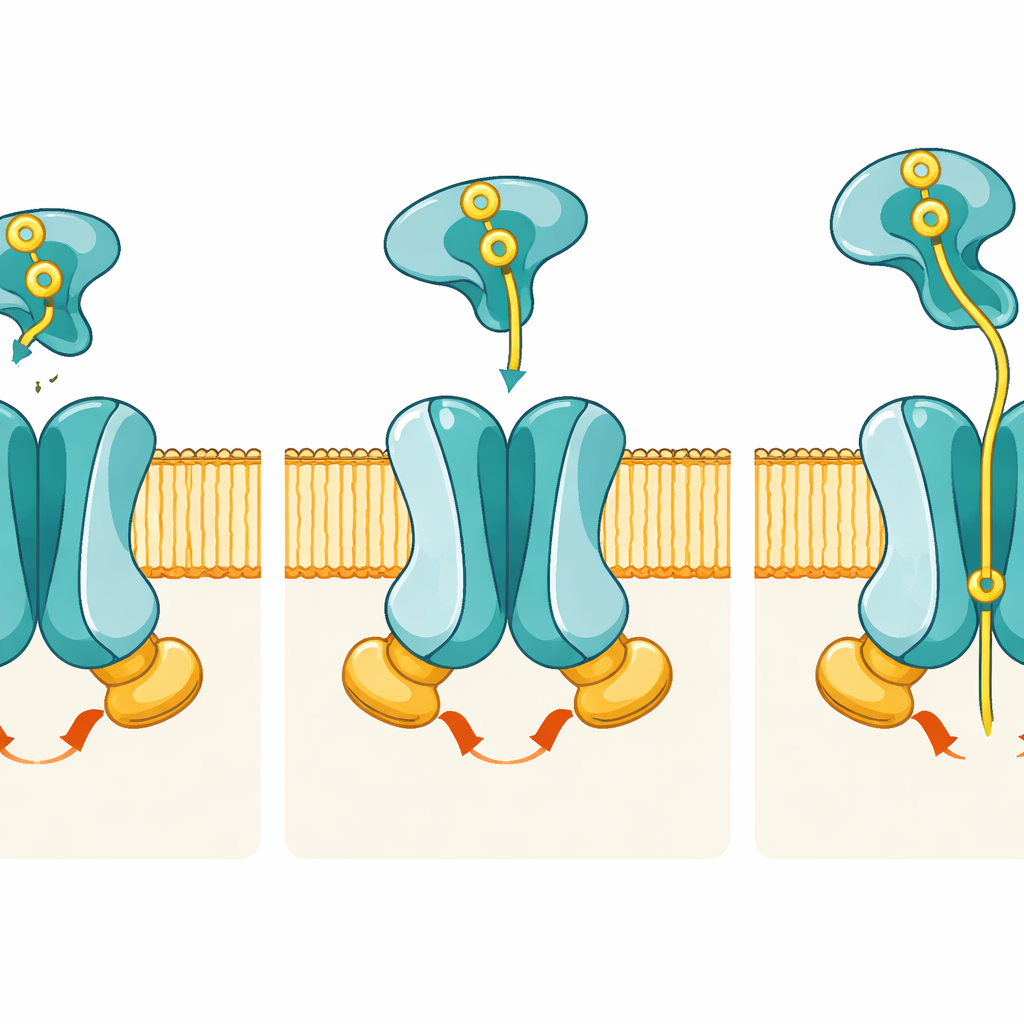
Een op maat gemaakt pocket voor fosfaat
In de naar buiten gerichte, ATP-gebonden structuur vinden de auteurs een dichtheid in het midden van het membraangebied die overeenkomt met een fosfaation. Dit ion wordt ondersteund door positief geladen aminozuren—met name twee arginines, één van PstA en één van PstC—die als moleculaire vingertoppen het negatief geladen fosfaat klemmen. Computersimulaties laten zien dat fosfaat stabiel in dit pocket gebonden blijft over microseconden, en genetische experimenten bevestigen het belang ervan: wanneer deze sleutelresiduen worden gemuteerd, verbrandt de transporter nog steeds ATP maar importeert hij fosfaat zeer slecht. Deze scheiding van ‘‘waar energie wordt verbruikt’’ en ‘‘waar lading wordt herkend’’ benadrukt hoe precies het apparaat is afgestemd op fosfaat.
Van structurele snapshots naar medische belofte
Gezamenlijk schetsen de structuren en ondersteunende biochemische tests een volledige cyclus: PstS vangt fosfaat buitenop, legt aan bij de naar binnen gerichte transporter, en veroorzaakt—gekoppeld aan ATP-binding en -afbraak door PstB—een omslag die fosfaat in het membraanpocket en tenslotte in het celinterieur overbrengt. Nadat ATP gehydrolyseerd is, ontspant het apparaat terug naar de rusttoestand, klaar voor een nieuwe ronde. Voor een niet-specialist is de kernboodschap dat we nu een blauwdruk op atomaire schaal hebben voor hoe veel bacteriën overleven in fosfaatarme omgevingen en hun virulentie reguleren. Deze gedetailleerde kaart kan het ontwerp sturen van geneesmiddelen, antilichamen of peptiden die de transporter blokkeren of zijn vanger-eiwit afschermen, en zo een essentiële voedingspoort in een kwetsbaar therapeutisch doel veranderen.
Bronvermelding: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
Trefwoorden: fosfaattransport, opname van voedingsstoffen door bacteriën, ABC-transporter, PstSCAB, antibacteriële doelwitten