Clear Sky Science · nl
Moleculaire inzichten in de capsulaire polysacharide-transporter Wza-Wzc-complex
Hoe bacteriën onzichtbare pantser dragen
Bacteriën die ons ziek maken beschermen zichzelf vaak met een suikerachtige laag, of capsule, die hen helpt ons immuunsysteem te ontwijken en bestand te zijn tegen vijandige omstandigheden. Deze studie onthult, op atomaire detailgraad, hoe een belangrijk onderdeel van de machinerie bij veel voorkomende darmbacteriën dat suikerachtige pantser bouwt en exporteert. Begrip van dit proces kan de weg wijzen naar nieuwe antibiotica en vaccins die ziekteverwekkers hun beschermende schild ontnemen in plaats van ze alleen te doden.
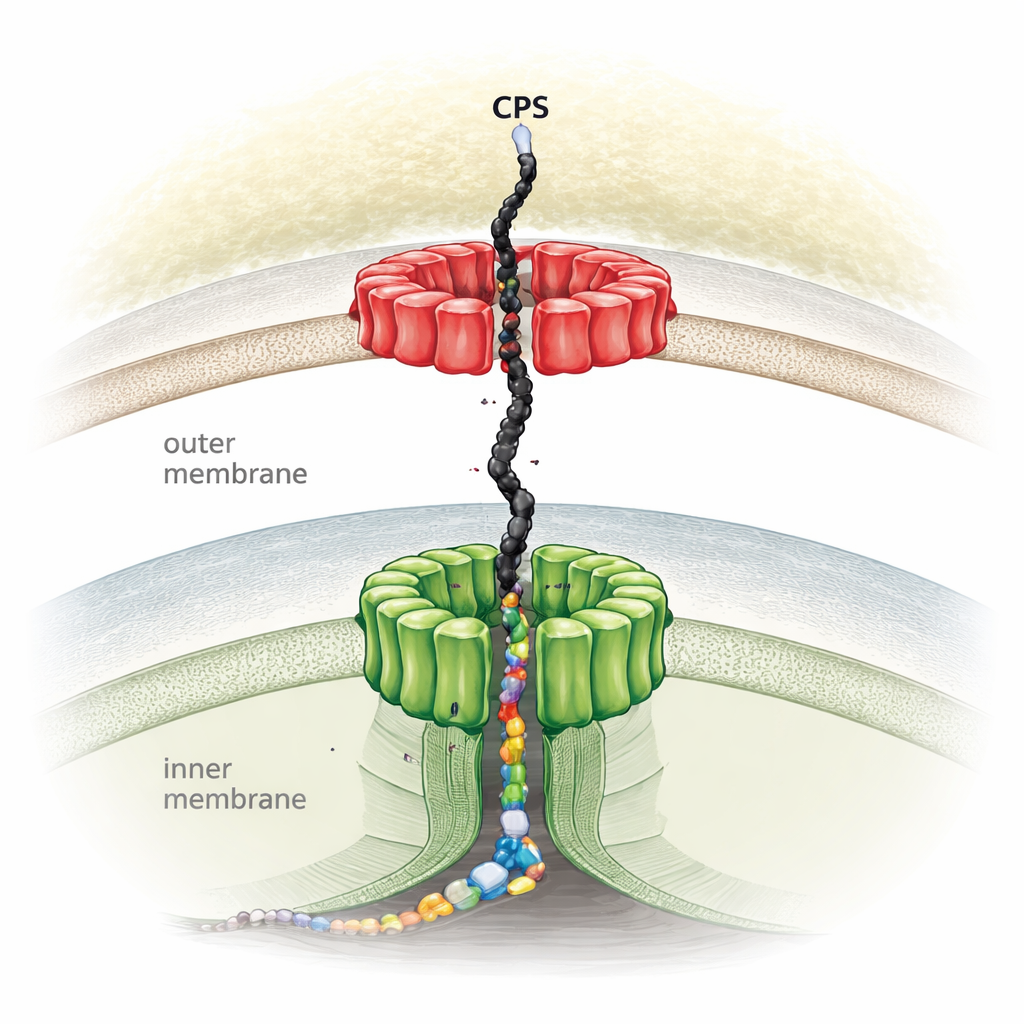
Het suikerschild rond gevaarlijke ziekteverwekkers
Veel schadelijke bacteriën omringen zich met capsulaire polysachariden—lange, vertakte ketens van suikers die een dikke buitenlaag vormen. Deze capsule helpt hen immuunaanvallen te ontwijken, bestand te zijn tegen antibiotica en resistente biofilms te vormen. Het werk richt zich op Escherichia coli, een goed bestudeerd modelorganisme dat een veelvoorkomende route gebruikt, de Wzx/Wzy-afhankelijke pathway, om deze suikerketens samen te stellen. In deze route worden eerst kleine herhaaleenheden van suikers binnenin de cel opgebouwd, over het binnenmembraan gekanteld, aan elkaar gekoppeld tot lange polymeren en uiteindelijk naar buiten geduwd om de capsule te vormen. Hoewel onderzoekers de namen van de belangrijkste eiwitspelers kenden, ontbrak een volledig beeld van hoe ze samenkomen tot één machine die de gehele bacteriële envelope overspant.
Een volledige moleculaire tunnel onthuld
Met behulp van hoogresolutie cryo-elektronenmicroscopie losten de auteurs de volledige driedimensionale structuur op van het Wza-Wzc-complex—de kern exportmachinerie voor capsulaire suikers in E. coli K12. Ze vonden dat acht kopieën van elk eiwit zich samenvoegen tot een hoge, continue kanaal dat loopt van het binnenmembraan naar het buitenmembraan en de waterige ruimte daartussen overbrugt. Wza zit in het buitenmembraan als een stijf ringvormig uitlaatportaal, terwijl Wzc een flexibele toren vormt die in het binnenmembraan verankerd is. Samen creëren ze een tunnel van ongeveer 250–360 angström lang, breed genoeg om een grote, flexibele suikermolecule vanaf de plaats waar ze wordt gemaakt bij het binnenmembraan tot aan het celoppervlak te geleiden zonder dat die wegdiffundeert of lekt. Het muteren van sleutelcontactpunten tussen Wza en Wzc stopte de capsuleproductie volledig, wat bevestigt dat dit gezamenlijke complex essentieel is voor export.
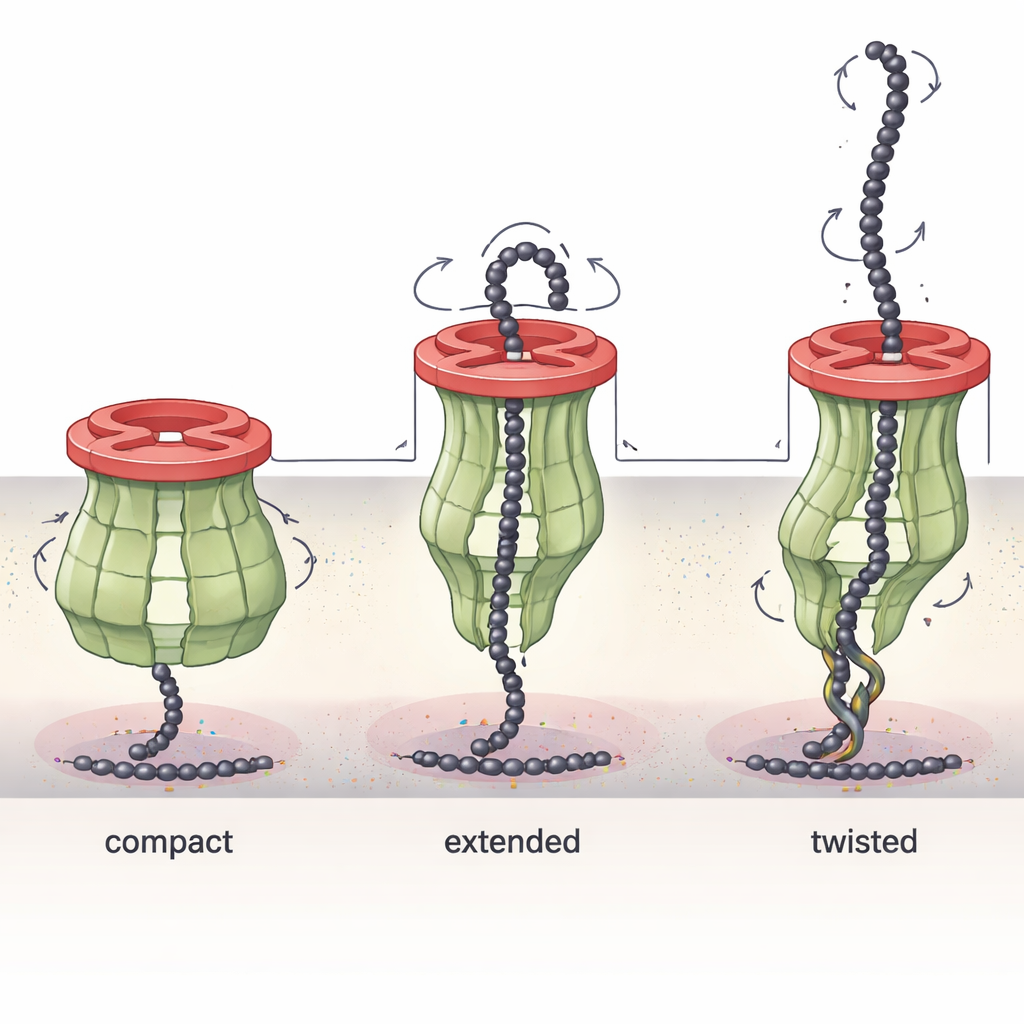
Een van vorm veranderende motor die suikers naar buiten trekt
Het Wzc-gedeelte van het complex bleek opmerkelijk dynamisch. Door meerdere structurele “momentopnames” onder verschillende chemische condities vast te leggen, toonden de onderzoekers aan dat Wzc’s lange periplasmische armen kunnen buigen, draaien en uitrekken als mechanische hefbomen. In één toestand is het kanaal compact en strak gesloten; in andere toestanden heeft Wzc geroteerd en uitgerekt, waarbij de breedte en de vorm van de tunnel subtiel veranderden. In bepaalde conformaties blokkeren de armen deels het kanaal of maken ze minder strakke contacten met Wza, en in extreme gevallen kan een enkele Wzc-ring twee Wza-ringen tegelijk betrekken. Deze waarnemingen ondersteunen een model waarin Wzc enigszins fungeert als een moleculaire lier: zijn draai- en lengtebewegingen helpen de groeiende suikerketen van het binnenmembraan weg te trekken en in het poreuze buitenmembraan te voeren, terwijl ze ook de assemblage en desassemblage van het hele complex coördineren.
Een suikerherkennend landingsplatform
Een andere puzzel was hoe de machinerie de juiste suikerbouwstenen herkent temidden van de vele koolhydraten in en rond de cel. Wzc bevat een "jellyroll"-domein net boven het binnenmembraan waarvan de rol tot dan toe onduidelijk was. Structurele vergelijkingen met bekende suikerbindende eiwitten, gecombineerd met biochemische testen op arrays van gezuiverde koolhydraten, toonden aan dat dit domein specifieke suikermotieven kan herkennen die vergelijkbaar zijn met die in de E. coli-capsule. Het verwijderen van de jellyroll-regio verminderde de capsuleproductie sterk, maar maakte die niet volledig onmogelijk, wat suggereert dat het functioneert als een landingsplatform dat nieuw gekantelde suikerunits opvangt en ze richting een polymerisatieplatform leidt dat door Wzc samen met het enzym Wzy wordt gevormd, dat de eenheden aan elkaar naait tot een lange keten.
Groei, export en reset coördineren
Ten slotte koppelt de studie deze structurele kenmerken aan een biochemisch controlesysteem gebaseerd op fosforylering—de omkeerbare toevoeging van fosfaatgroepen aan een tyrosinerijke staart op Wzc. Wanneer Wzc sterk gefosforyleerd is, komt het meestal voor als losse individuele eenheden. Als fosfaten door een partnerenzym worden verwijderd, assembleren de kinase-domeinen van Wzc in een octameer en herschikken ze de armen zodat deze Wza kunnen betrekken en het polymerase Wzy kunnen omringen. Terwijl de capsuleketoog groeit en door de tunnel wordt getrokken, helpt verdere draaiing en uitrekking van Wzc waarschijnlijk het voltooide polymeer vrij te geven in Wza voor export. Zodra de secretie voltooid is, fosforyleert Wzc zichzelf opnieuw, wat ertoe leidt dat het complex uiteenvalt en het systeem reset voor een volgende ronde van capsuleproductie.
Waarom dit belangrijk is voor de bestrijding van infecties
In gewone bewoordingen laat dit werk zien, bijna bout voor bout, hoe bacteriën een moleculaire pijpleiding bouwen die lange suikerketens van binnenin de cel naar buiten rijgt, waar ze een beschermende mantel vormen. Door de structuur en bewegingen van het Wza-Wzc-complex in kaart te brengen en suikerherkenning en controle-elementen te lokaliseren, belicht de studie verschillende kwetsbare plekken die toekomstige geneesmiddelen of vaccins zouden kunnen aanwenden. Het verstoren van deze exportmachine zou bacteriën niet per se direct doden, maar het zou hen hun pantser kunnen ontnemen, waardoor ze veel kwetsbaarder worden voor onze immuunverdediging en voor bestaande antibiotica.
Bronvermelding: Yuan, B., Sieben, C., Raj, P. et al. Molecular insights into the capsular polysaccharide transporter Wza-Wzc complex. Nat Commun 17, 1436 (2026). https://doi.org/10.1038/s41467-026-69136-2
Trefwoorden: bacteriële capsule, polysacharide-secretie, Wza-Wzc-complex, cryo-EM-structuur, antimicrobiële doelwitten