Clear Sky Science · nl
Een door mRNA afgeleverde consensusallergeen wekt een neutraliserende IgG-respons op tegen voedsel- en pollenallergenen
Waarom veel allergieën tegelijk behandeld zouden kunnen worden
Voor mensen die niet alleen op één voedsel of pollen reageren, maar op vele verwante bronnen, kan het dagelijks leven aanvoelen als lopen door een mijnenveld. Een hapje perzik, een handvol noten of een lente-bries vol pollen kan allemaal hetzelfde gevaarlijke reactiepatroon uitlokken. Deze studie onderzoekt een nieuwe manier om dergelijke kruisallergieën te kalmeren met één enkele, ontworpen eiwit dat via mRNA wordt afgeleverd — dezelfde basistechnologie die in sommige COVID-19-vaccins wordt gebruikt — om het immuunsysteem te trainen een hele familie verwante allergenen in één keer te blokkeren.
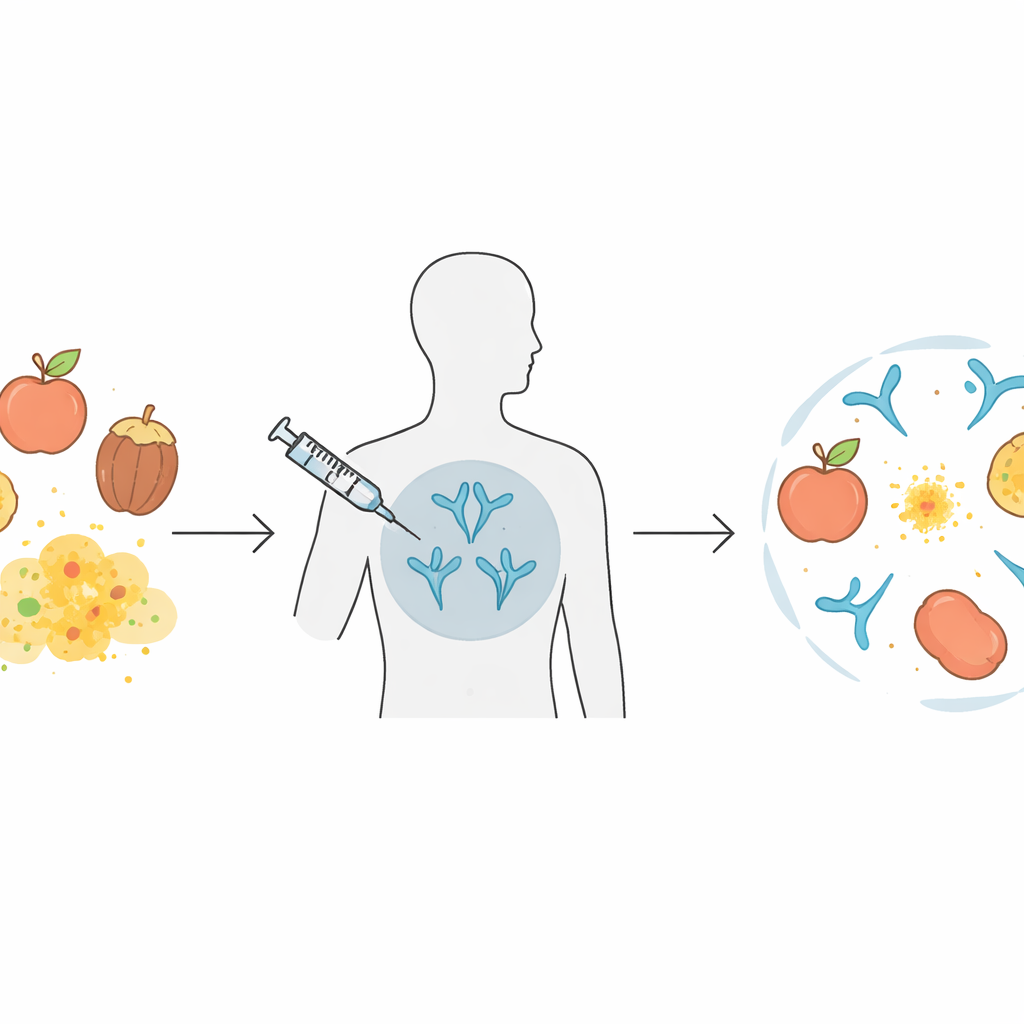
Hoe één allergie er vele kan worden
Veel mensen met voedselallergieën zijn niet allergisch voor slechts één stof. Ze kunnen reageren op meerdere vruchten, noten, groenten en zelfs pollen omdat deze bronnen gelijkaardige eiwitten delen. In dit werk ligt de focus op een familie plantaardige eiwitten die niet-specifieke lipid transfer-eiwitten (nsLTPs) worden genoemd, veelvoorkomend in voedingsmiddelen zoals perziken, appels, noten en in pollen van bepaalde bomen en onkruiden. In Mediterrane landen kan het zogenaamde “LTP-syndroom” patiënten laten reageren op een brede lijst voedingsmiddelen, soms met levensbedreigende anafylaxie. Huidige allergie-immunotherapieën richten zich meestal op extracten van één enkele bron en dekken mogelijk niet alle kruisreagerende verwanten, wat leidt tot lange behandeltrajecten en onvolledige bescherming.
Het ontwerpen van een “consensus”allergeen
De onderzoekers stelden zich tot doel één eiwit te ontwerpen dat veel verschillende nsLTP-allergenen tegelijk nabootst. Ze vergeleken aminozuursequenties van nsLTPs gevonden in zowel voedingsmiddelen als pollen en bouwden een consensusversie, genoemd cnsLTP1, die geen enkel natuurlijk eiwit kopieert maar gedeelde structurele kenmerken van de familie vastlegt. Laboratoriumtests toonden aan dat dit ontworpen eiwit vouwde zoals natuurlijke nsLTPs, stabiel bleef bij opwarming en afkoeling en, cruciaal, werd herkend door IgE-antilichamen van patiënten die al allergisch zijn voor nsLTPs. Die herkenning duidt erop dat cnsLTP1 dezelfde sleutelpunten voor het uitlokken van allergieën presenteert als allergenen in het echte leven, wat essentieel is als het immuunsysteem anders getraind moet worden.
Het immuunsysteem trainen met mRNA- en proteïnevaccins
Het team testte cnsLTP1 vervolgens in muizen met twee verschillende afleveringsmethoden: een traditioneel proteïnevaccin gemengd met adjuvantia, en een mRNA-vaccin verpakt in lipidenanpartikels, vergelijkbaar van samenstelling met goedgekeurde mRNA-vaccins. Bij naive muizen gaven beide benaderingen sterke antilichaamreacties tegen cnsLTP1, in het bijzonder IgG-subklassen die bij muizen bekend staan om een beschermende, allergieblokkerende rol. Het op mRNA gebaseerde vaccin produceerde doorgaans meer van een bepaald IgG-type en deed dat na minder doses. De tegen cnsLTP1 opgewekte antilichamen binden niet alleen aan het ontworpen eiwit maar ook aan een brede reeks verschillende voedsel- en pollen-nsLTPs, vaak breder dan antilichamen opgewekt tegen enkele natuurlijke allergenen zoals perzik- of ouderwets pellitory-nsLTPs. Dit betekent dat het consensusontwerp erin slaagde het immuunsysteem te leren vele verwante allergenen te herkennen.
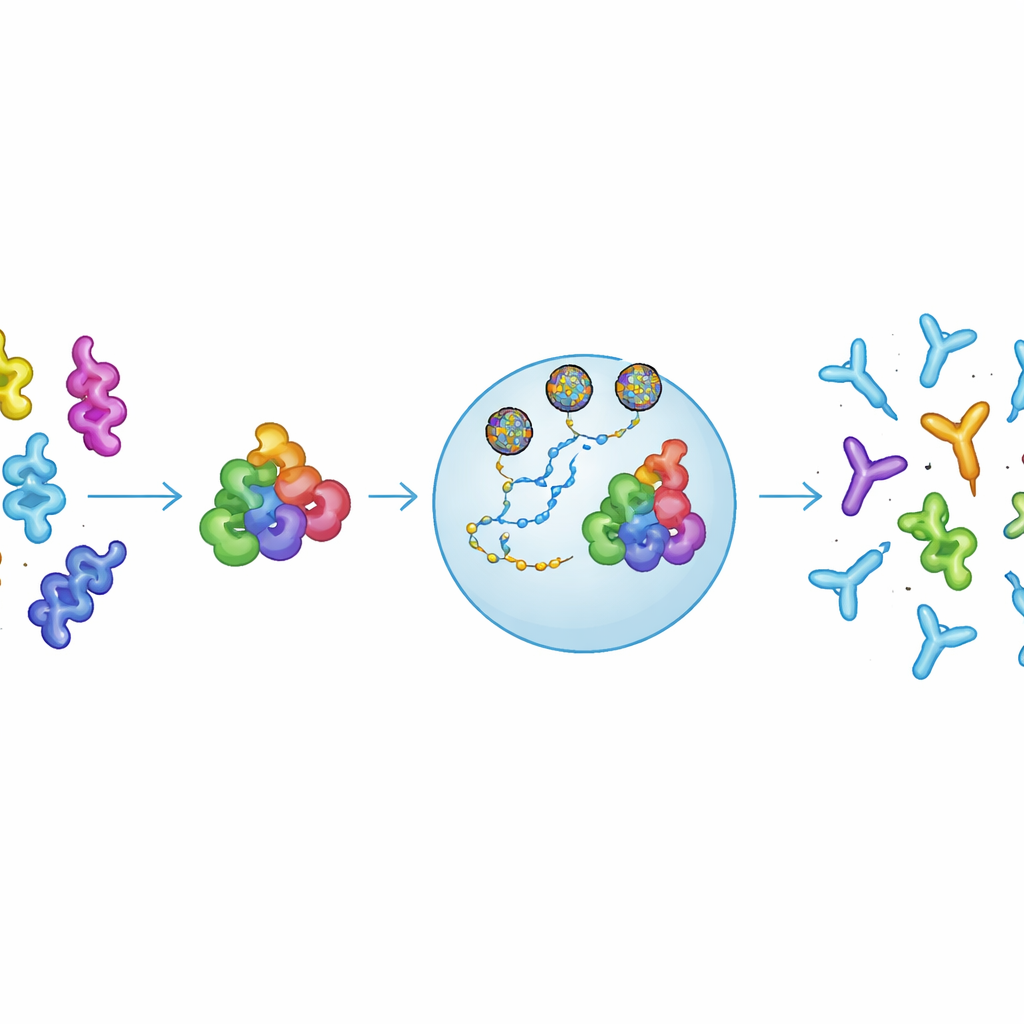
Allergische reacties in het lab blokkeren en testen in allergische muizen
Om te onderzoeken of deze antilichamen daadwerkelijk allergische reacties konden verstoren, mengden de onderzoekers muisserum met allergenen en voegden vervolgens humaan serum toe van patiënten met ernstige nsLTP-allergieën. Ze vonden dat door cnsLTP1 geïnduceerde antilichamen IgE konden blokkeren om aan meerdere nsLTPs te binden, en dat ze de degranulatie van gehumaniseerde basofiel-achtige cellen — een celgebaseerde vervanger voor allergische activatie — verminderden. In een zwaardere test gebruikte het team een muismodel dat al gesensibiliseerd was voor perzik-nsLTP en vatbaar is voor anafylaxie. Het mRNA-vaccin werd goed verdragen en verhoogde IgG-antilichamen tegen meerdere nsLTPs, maar onder de specifieke geteste condities verminderde het niet duidelijk anafylactische symptomen zoals daling van de lichaamstemperatuur of merkers van mestcelactivatie. Dit suggereert dat hoewel het immuunsysteem werd hervormd, het regime nog niet krachtig of nauwkeurig genoeg was om ernstige reacties volledig te voorkomen.
Wat dit kan betekenen voor toekomstige allergiezorg
De studie levert een proof of concept dat één enkel, ontworpen “consensus”allergeen afgeleverd via mRNA brede, kruisreactieve en functioneel blokkerende IgG-antilichamen kan opwekken tegen een hele familie verwante plantaardige voedsel- en pollenproteïnen. Hoewel het huidige protocol allergische muizen nog niet tegen anafylaxie beschermde, wijzen de bevindingen op een flexibel platform dat mogelijk verbeterd kan worden door dosis, adjuvantia of toedieningsroute aan te passen. Op de lange termijn zouden dergelijke op consensus gebaseerde mRNA-therapieën het mogelijk kunnen maken clusters van verwante allergieën te behandelen — zoals die aangedreven door nsLTPs, andere planteneiwitfamilies of zelfs snel muterende pathogenen — met kortere, preciezere en breder beschermende behandelingen.
Bronvermelding: Møiniche, M., Johansen, K.H., Parrón-Ballesteros, J. et al. An mRNA-delivered consensus allergen induces a neutralizing IgG response against food and pollen allergens. Nat Commun 17, 2402 (2026). https://doi.org/10.1038/s41467-026-69134-4
Trefwoorden: voedselallergie, pollenallergie, mRNA-immunotherapie, kruisreactiviteit, lipid transfer-eiwitten