Clear Sky Science · nl
MG53 bemiddelt communicatie tussen skeletspier en lever en verbetert alcoholmetabolisme bij alcoholische leverziekte
Spieren die de lever helpen
Overmatig drinken kan de lever langzaam vergiftigen, wat leidt tot vetophoping, littekenvorming en uiteindelijk leverfalen. Tegelijkertijd verliezen veel zware drinkers spiermassa en kracht, een aandoening die spierverlies wordt genoemd. Deze studie toont aan dat onze spieren in dit verhaal niet alleen toeschouwers zijn: ze zenden een beschermend eiwit uit dat naar de lever reist en helpt alcohol veiliger af te breken. Inzicht in deze verborgen samenwerking tussen spier en lever kan nieuwe wegen openen om alcoholische leverziekte te behandelen, een aandoening waarvoor effectieve therapieën nog steeds schaars zijn.
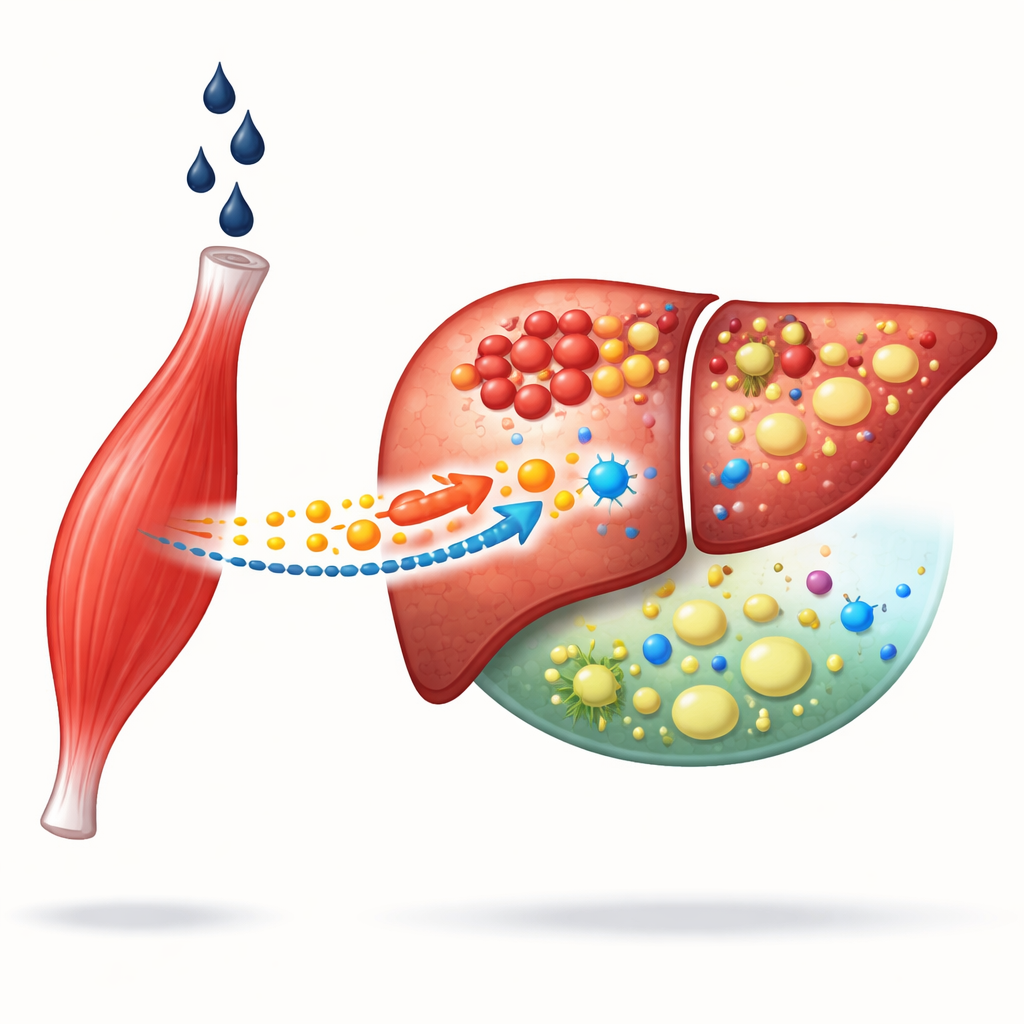
Wanneer drinken zowel spier als lever schaadt
Alcoholische leverziekte ontwikkelt zich over jaren van zwaar drinken en hangt nauw samen met spierverlies. Patiënten met zwakkere spieren hebben doorgaans ernstiger leverschade en een hoger risico op complicaties. De auteurs begonnen met het analyseren van nationale gezondheidsenquêtes en humane leverproteïne-databases. Ze vonden dat mensen met een lage spiermassa ongeveer twee keer zo waarschijnlijk alcoholgerelateerde leverproblemen hadden, vooral mannen. Van de vele circulerende eiwitten viel er één op als sterke kandidaat die de gezondheid van spieren met leveruitkomsten verbindt: MG53, een eiwit dat voornamelijk door skeletspier wordt gemaakt en bekendstaat als een soort ‘moleculaire pleister’ voor het herstellen van beschadigde celmembranen.
Een reizende beschermer van spier naar lever
Onder normale omstandigheden maken levercellen zelf geen MG53 en vertrouwen ze op wat via de bloedbaan arriveert. Bij mensen en muizen met alcoholische leverziekte zagen de onderzoekers dat de MG53-niveaus in het bloed daalden maar binnenin de lever stegen, wat suggereert dat het eiwit uit de circulatie wordt onttrokken naar beschadigd leverweefsel. Muizen die genetisch zo waren gemodificeerd dat ze geen MG53 hadden, waren veel kwetsbaarder voor alcoholgerelateerde schade: hun lever werd vetter, meer ontstoken, meer vervormd door littekenweefsel en hun overlevingskansen daalden sterk. Wanneer het ontbrekende eiwit werd aangevuld met een laboratoriumgemaakte versie, verbeterden veel van deze problemen, wat aangeeft dat MG53 een cruciaal onderdeel is van de verdedigingslinie van het lichaam tegen chronische alcoholschade.
Hoe MG53 de alcoholafbraak versterkt
Alcohol veilig afbreken vereist twee belangrijke leverenzymen: alcoholdehydrogenase (ADH) en aldehyde dehydrogenase 2 (ALDH2). Deze enzymcomplexen zetten alcohol om in een zeer reactieve tussenstof en vervolgens in een minder schadelijke stof die het lichaam kan uitscheiden. Dit proces is afhankelijk van zink, een sporenelement dat vaak uitgeput raakt bij zware drinkers. De studie laat zien dat MG53 zich fysiek bindt aan beide enzymen en helpt zink naar hen te transporteren, fungeren als een metallochaperonne—een drager die de enzymen voorziet van het metaal dat ze nodig hebben om efficiënt te werken. Bij muizen zonder MG53 daalden de leverzinkniveaus verder, stapelden alcohol en zijn toxische afbraakproducten zich op in het bloed en nam oxidatieve stress toe. Het toevoegen van recombinante MG53 herstelde de zinkniveaus, verhoogde de enzymactiviteit en verminderde toxische alcoholtussenproducten.
Het bouwen van een slimmer medicijnbezorgpakket
Om deze inzichten in een potentiële behandeling om te zetten, ontwierp het team kleine bio‑afgeleide nanodeeltjes die MG53 samen met zink verpakken. Deze MG53@Zn-deeltjes zijn opgebouwd rond een menselijke serumalbumine‑mantel en zijn zo geschaald dat ze zich in de lever ophopen. In celkweken die werden blootgesteld aan zeer hoge alcoholniveaus drongen de deeltjes de levercellen binnen, verminderden oxidatieve stress en vetophoping en behouden de cellen beter hun overleving dan MG53 alleen. Bij muizen die een chronisch-plus-bingedieet met alcohol kregen, verbeterde herhaalde toediening van MG53@Zn-nanodeeltjes de overleving, herstelde de leverzinkvoorraden, verlaagde markers voor leverschade en ontsteking, verminderde littekenvorming en verwijderde alcohol en zijn toxische tussenstof efficiënter. Belangrijk is dat de nanodeeltjes veilig leken bij gezonde muizen tijdens een maandlange behandelingsperiode.
Wat dit betekent voor toekomstige zorg
Voor leken is de kernboodschap dat spier en lever nauwer samenwerken dan eerder werd aangenomen. Een uit de spier vrijgekomen eiwit kan naar de lever reizen, zink afleveren aan alcoholverwerkende enzymen en het orgaan helpen omgaan met de stress van zwaar drinken. Door een nanodeeltje te ontwikkelen dat zowel dit eiwit als zink direct naar de lever levert, schetsen de onderzoekers een veelbelovende strategie om alcoholische leverziekte te behandelen. Hoewel deze resultaten tot nu toe beperkt zijn tot diermodellen en mannelijke proefpersonen, wijzen ze op toekomstige therapieën die de eigen reparatiemechanismen van het lichaam ondersteunen in plaats van alleen symptomen te behandelen nadat er al ernstige schade is opgetreden.
Bronvermelding: Shu, T., Zeng, X., Wang, J. et al. MG53 mediates skeletal muscle-liver cross-talk and enhances alcohol metabolism in alcoholic liver disease. Nat Commun 17, 2722 (2026). https://doi.org/10.1038/s41467-026-69132-6
Trefwoorden: alcoholische leverziekte, MG53, spier–lever communicatie, zinkmetabolisme, nanodeeltjestherapie