Clear Sky Science · nl
Gedesigneerde bacteriële therapie onderdrukt Enterohemorrhagic Escherichia coli via metabolische competitie en virulentiesilencing
Vriendelijke bacteriën als levende medicijnen
Voedselvergiftiging door bepaalde stammen van Escherichia coli kan veel meer veroorzaken dan alleen buikklachten. Sommige zogenaamde enterohemorragische E. coli (EHEC) scheiden krachtige toxines uit die nierfalen kunnen veroorzaken, vooral bij kinderen, en standaardantibiotica kunnen de situatie juist verergeren. Deze studie onderzoekt een ander soort behandeling: het gebruik van een geherprogrammeerde probioticum en een suiker die voorkomt in menselijke moedermelk, verpakt in slimme microcapsules, om gevaarlijke bacteriën te verdringen en hun schadelijke gedrag stil te leggen zonder het overige darmecosysteem te verstoren.
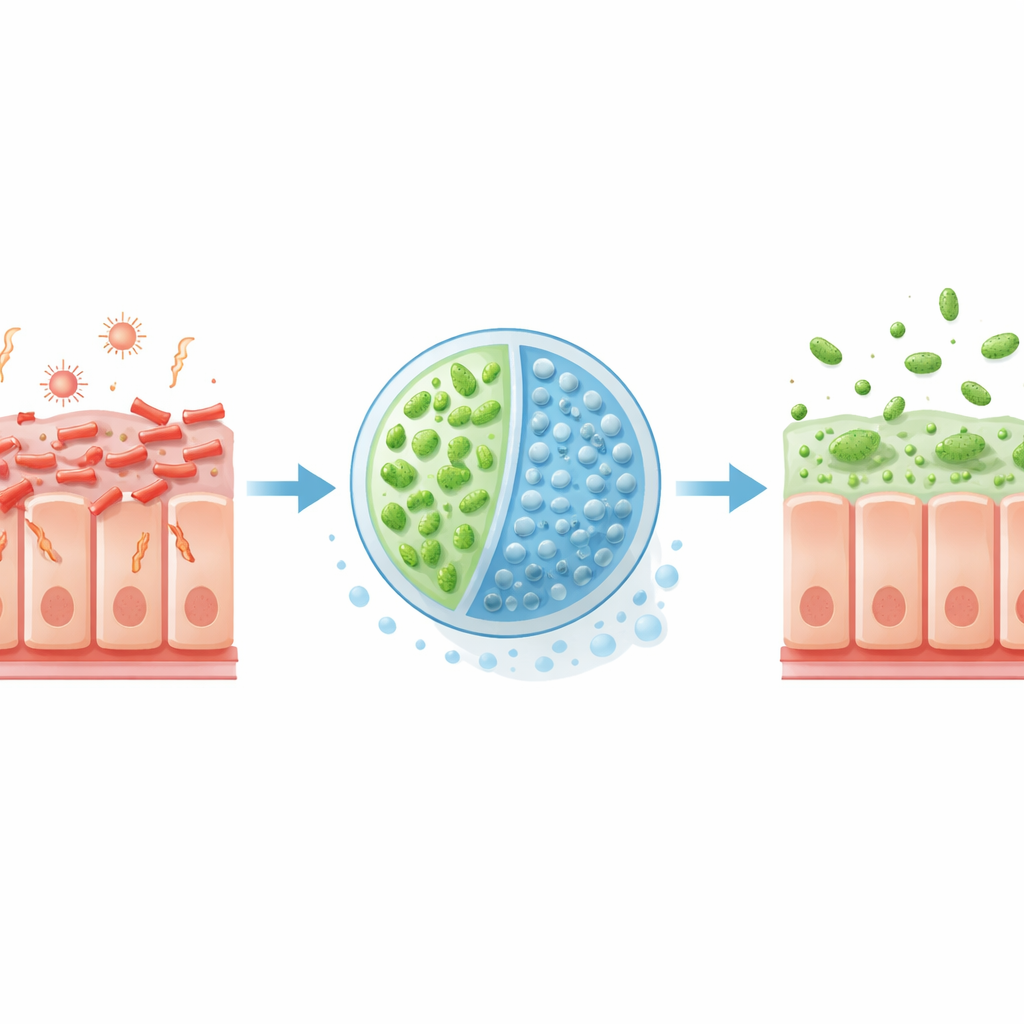
Waarom sommige E. coli zo gevaarlijk zijn
EHEC is een voedselovergedragen kiem die vaak via onvoldoende verhit vlees of besmette groente wordt opgelopen. Eenmaal in de darm hecht het zich stevig aan de darmcellen en injecteert het eiwitten die het celoppervlak herschikken, waardoor het bacteriën mogelijk maakt zich vast te klemmen en zich te verspreiden. Tegelijkertijd produceert EHEC Shiga-toxines, die in de bloedbaan kunnen terechtkomen en bloedvaten beschadigen, wat soms leidt tot de levensbedreigende aandoening hemolytisch-uremisch syndroom. Omdat veel antibiotica stress bij deze bacteriën veroorzaken en juist meer toxineafgifte triggeren, hebben artsen weinig veilige opties buiten ondersteunende zorg, wat nieuwe, gerichte benaderingen zeer wenselijk maakt.
Een probioticum herprogrammeren om EHEC uit te hongeren en te ontwapenen
De onderzoekers gebruikten Escherichia coli Nissle 1917, een al lang gebruikt probioticum, en herbouwden het tot een therapeutische microbe genaamd EcN3. Ze voorzagen EcN3 van extra genen waarmee het efficiënter een suurzout, glucuronzuur, kan afbreken—een voedingsbron die EHEC in de dikke darm prefereert. Daarnaast gaven ze EcN3 een enzym dat de moedermelksuiker 2′-fucosyllactose in twee delen splitst: lactose en fucose. Lactose fungeert als een interne "schakelaar" die het verbeterde nutriëntengebruik in EcN3 activeert, waardoor het glucuronzuur opneemt en EHEC van deze brandstof berooft. Fucose werkt als een signaal dat EHEC aanzet om belangrijke virulentiegenen minder actief te maken, waardoor zijn vermogen om zich stevig te hechten en schade te veroorzaken afneemt.
Slimme capsules die therapie op de juiste plek vrijgeven
Het simpelweg toedienen van geengineerde bacteriën en suiker aan de darm is niet genoeg: maagsap kan het probioticum doden en andere microben kunnen de suiker opeten voordat deze de dikke darm bereikt. Om dit op te lossen bouwde het team multicompartment microsferen—kleine bolletjes van alginaatgel met twee aparte interne kamers. De ene kamer bevat EcN3 en de andere bevat 2′-fucosyllactose, waardoor ze gescheiden blijven tot de bolletjes de dikke darm bereiken. Deze microcapsules zijn bestand tegen afbraak in nagebootst maagsap maar lossen op onder colonachtige omstandigheden, en geven zowel de geengineerde bacteriën als de suiker precies daar vrij waar ze nodig zijn. Bij muizen leidde het ingekapselde systeem tot hogere overleving van EcN3 en sterkere activatie van zijn geengineerde genen vergeleken met het geven van dezelfde componenten zonder capsules.
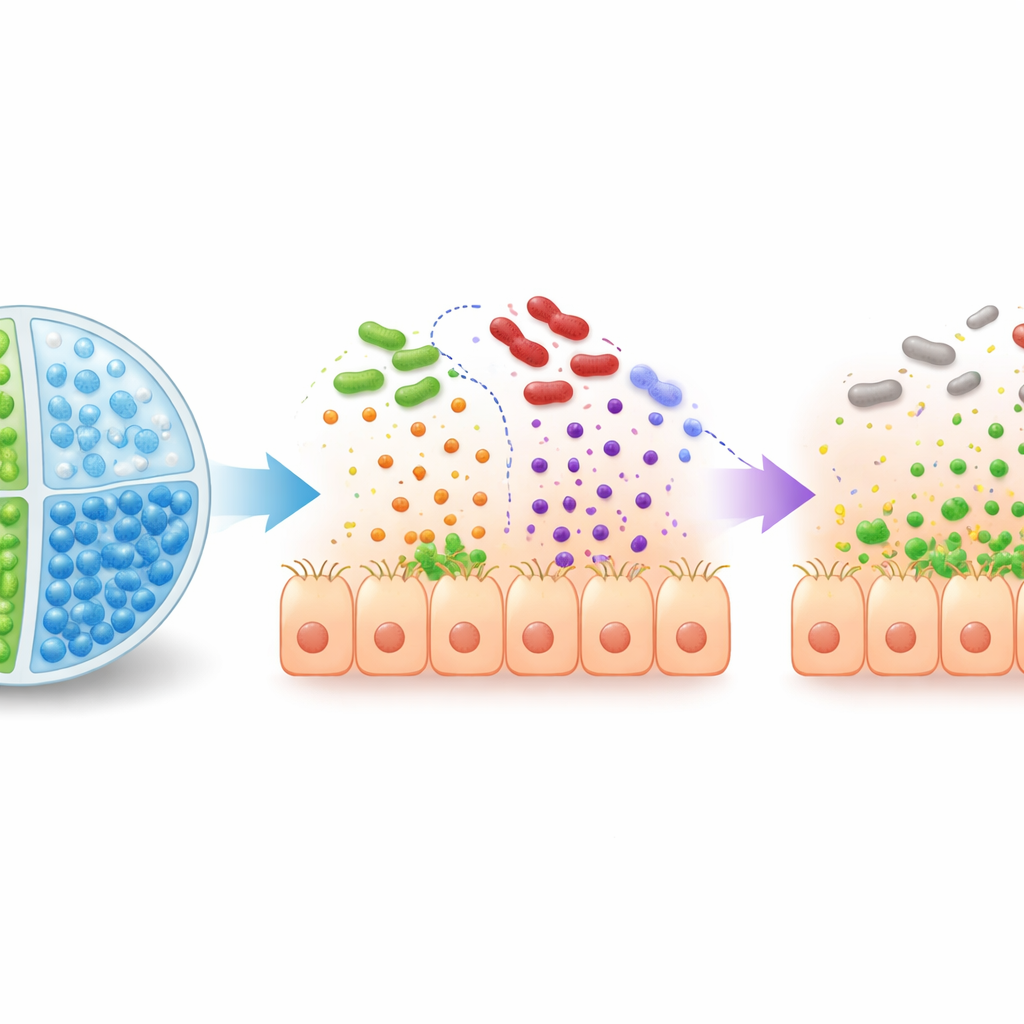
Bescherming testen in diermodellen
Het team testte hun strategie in zuigelingenkonijnen geïnfecteerd met EHEC en in muizen geïnfecteerd met Citrobacter rodentium, een nauw verwant pathogeen dat veel aspecten van de menselijke ziekte nabootst. Wanneer na infectie werd behandeld met EcN3 plus 2′-fucosyllactose, bleek dat de dieren minder ziekteverwekkers in de darm hadden, lagere expressie van de hechtingsgenen van de bacterie en minder schade aan darmweefsel—en dat allemaal zonder toegenomen productie van Shiga-toxine. Als preventieve maatregel werkte de vrije (niet-ingekapselde) combinatie slecht omdat de suiker snel door de bestaande microbiota werd verbruikt. Daarentegen hadden zowel konijnen als muizen die EcN3 en 2′-fucosyllactose samen in duale kamers-microsferen kregen toegediend, sterk verminderde kolonisatie door de pathogeen, mildere ziekteverschijnselen en betere overleving.
Helpen goede microben en de darmbarrière herstellen
Met DNA-sequencing om de darmbacteriën te profileren vonden de wetenschappers dat infectie de normale microbiële balans verstoorde: schadelijke Citrobacter nam toe terwijl gunstige groepen verzwakten. Behandeling met de geengineerde microcapsules verminderde niet alleen de pathogeenniveaus, maar herstelde ook de gemeenschap naar een gezondere staat, met name door een toename van Lactobacillus-soorten die bekendstaan om hun ondersteuning van darmgezondheid. Maatregelen van de darmbarrièrefunctie vertelden een vergelijkbaar verhaal: dieren die de ingekapselde therapie kregen hadden hogere expressie van slijmgerelateerde en tight-junction-genen, dikkere beschermende slijmlaag en minder lekkage van een fluorescerende tracer van de darm naar de bloedbaan, wat wijst op strakkere, minder ontstoken darmwanden.
Een blik op toekomstige antibioticavrije infectiezorg
Samenvattend toont dit werk een tweesporen, gerichte strategie tegen een berucht moeilijk te behandelen voedselovergedragen infectie. Door een geengineerd probioticum dat concurreert om voedsel en een onschuldig suikersignaal kan waarnemen te combineren met microcapsules die beide componenten naar de dikke darm afleveren, verzwakt de therapie EHEC, verlaagt het zijn aantallen en beschermt de darm zonder te vertrouwen op traditionele antibiotica. Hoewel verdere veiligheids- en klinische studies nodig zijn, illustreert de benadering hoe levende medicijnen en slimme materialen ooit nauwkeurige, microbioomvriendelijke manieren kunnen bieden om ernstige darminfecties te beheersen en de afhankelijkheid van conventionele geneesmiddelen te verminderen.
Bronvermelding: Ma, G., Liu, R., Li, X. et al. Engineered bacterial therapy suppresses Enterohemorrhagic Escherichia coli through metabolic competition and virulence silencing. Nat Commun 17, 2307 (2026). https://doi.org/10.1038/s41467-026-69126-4
Trefwoorden: geengineerde probiotica, therapie voor darminfecties, EHEC, microbioom, microsferen voor medicijnafgifte