Clear Sky Science · nl
Een isoleerbare phosphaalumeen(3) die kleine moleculen kan activeren via unieke reactieschema's
Lastige bindingen verbreken met een nieuw chemisch instrument
Chemici zoeken voortdurend naar manieren om hardnekkige moleculen tot reactie te bewegen. Veel alledaagse stoffen, van waterstofgas tot kooldioxide, zijn opvallend stabiel, waardoor ze moeilijk te transformeren zijn tot nuttige producten. Dit artikel beschrijft een nieuw ontworpen molekuul, opgebouwd uit aluminium en fosfor, dat zulke terughoudende partners kan vastpakken en hun bindingen kan opensplitsen. Het begrijpen en beheersen van dit type bindingsactivatie kan ooit helpen om afvalgassen om te zetten in grondstoffen, of zachtere, metaalbesparende routes bieden om fijnere chemicaliën en materialen te maken.
Een ontwerpverbinding tussen aluminium en fosfor
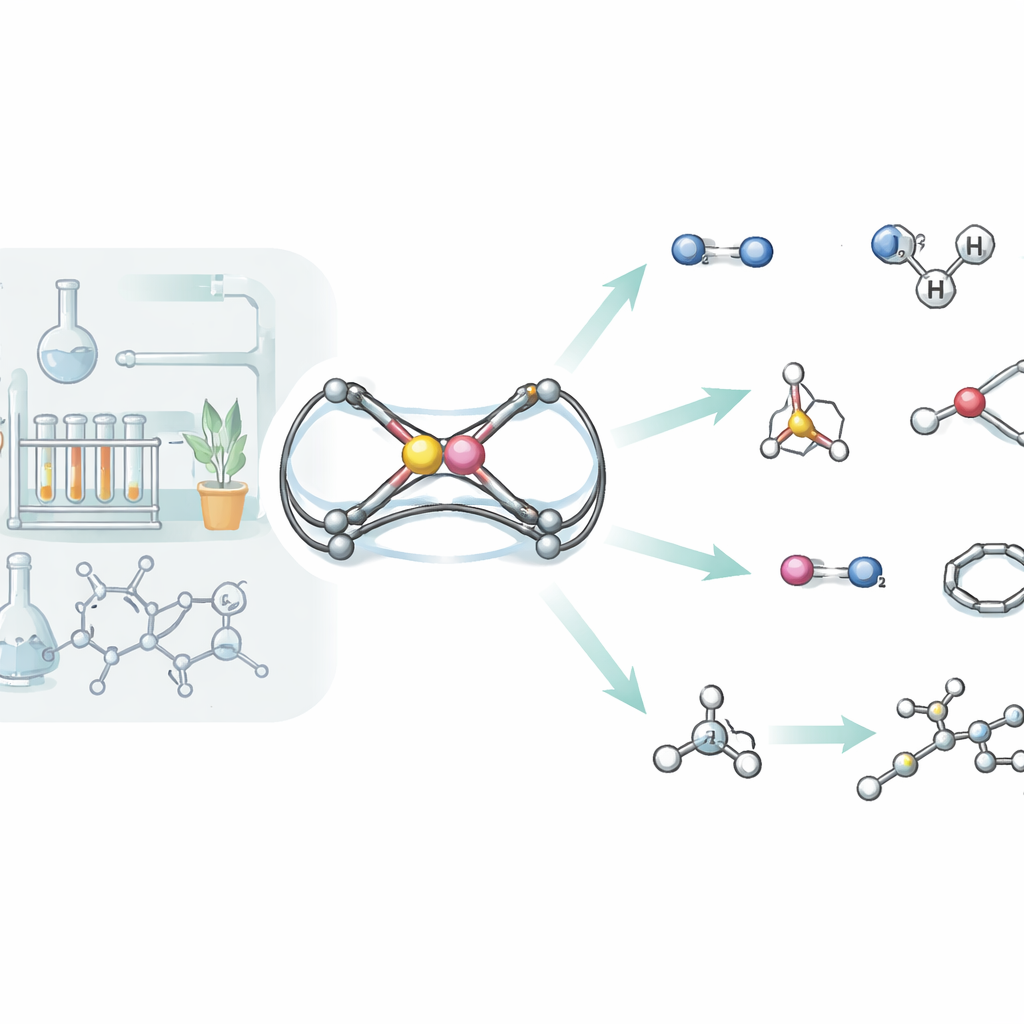
Centraal in de studie staat een zeldzaam soort verbinding tussen twee hoofdgroepelementen: aluminium en fosfor. De onderzoekers maakten een molecuul, in het artikel aangeduid als “3”, waarin deze twee atomen een nauwe dubbele binding delen. Om dit reactieve paar te behoeden voor desintegratie, omringden ze het met een omvangrijk organisch raamwerk dat het beschermt tegen toevallige reacties. Met twee verschillende synthetische routes verkregen ze dit complex in isoleerbare vorm en kweekten ze enkelvoudige kristallen geschikt voor röntgendiffractie, wat bevestigde dat fosfor gebonden is aan aluminium met een korte, dubbelbindingsachtige band terwijl elk atoom ondersteund wordt door stikstofhoudende liganden. Berekeningen toonden aan dat elektronen ongelijk verdeeld zijn tussen aluminium en fosfor, waardoor de binding gepolariseerd is en vatbaar voor aanval door andere moleculen.
Hoe het nieuwe molecuul met waterstofgas omgaat
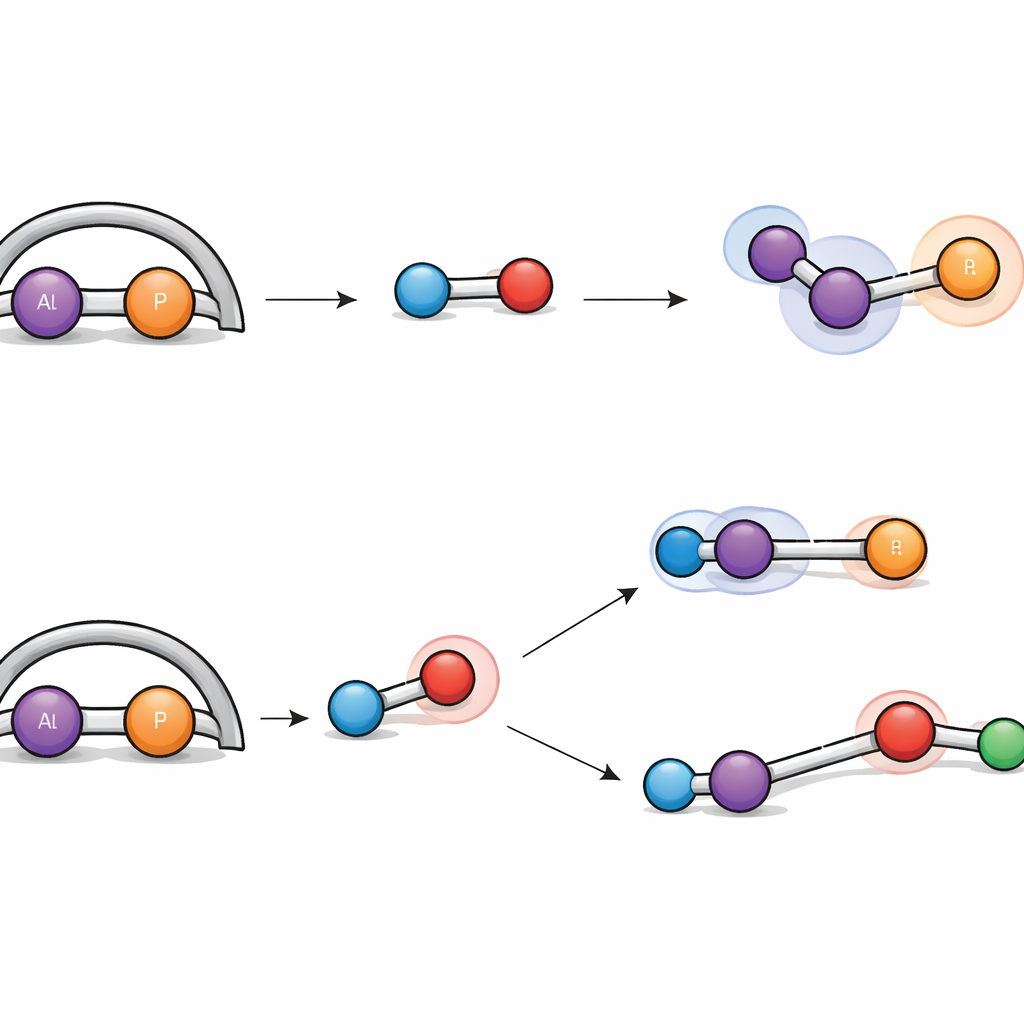
Waterstofgas is berucht moeilijk te splijten zonder edelmetalen, maar de nieuwe aluminium‑fosfor eenheid slaagt daar toch in. Bij blootstelling aan waterstof onder milde omstandigheden reageert het complex op twee verschillende manieren. In de ene route voegt de H–H‑binding zich eenvoudig over de aluminium–fosfor dubbele binding, waardoor die in twee enkele bindingen verandert en één waterstofatoom aan elk atoom blijft zitten. In de andere route wordt het waterstofmolecuul coöperatief uit elkaar getrokken door aluminium en een naburig stikstofatoom, een gedrag dat doet denken aan zogenaamde „gefrustreerde Lewis-paren”, die waterstof activeren zonder traditionele metaal katalysatoren. Gedetailleerde computersimulaties volgden beide routes en lieten zien dat hun energiedrempels vergelijkbaar zijn, wat verklaart waarom beide producten naast elkaar gevormd worden.
Een breed scala aan kleine moleculen uiteenrafelen
Waterstof is nog maar het begin. Het team testte systematisch hoe hun aluminium‑fosfor scaffold reageert met een breed scala aan kleine moleculen, waaronder wit fosfor, isocyaniden, kooldioxide, distikstofmonoxide, trimethylsilylazide, seleendimeren, silanen, aminen, styreen en eenvoudige alkynen. In veel van deze reacties wordt de oorspronkelijke Al=P‑verbinding volledig verbroken, waarbij de twee atomen terechtkomen in grotere kooi‑ of ringachtige structuren die fragmenten van het binnenkomende molecuul incorporeren. Zo wordt wit fosfor (P4) opengebroken en herbouwd tot een aluminium‑fosforkooi, terwijl kooldioxide tweemaal geïnjecteerd wordt om een zesring te vormen die aluminium en fosfor via twee nieuwe koolstof‑zuurstofbruggen verbindt. Bij silanen en aminen gedraagt het molecuul zich eerder als een klassieke dubbele binding: de binnenkomende Si–H of N–H‑eenheid voegt keurig over Al=P toe, wat opnieuw het π‑bindingskarakter van deze ongewone koppeling aantoont.
Waarom het omringende raamwerk ertoe doet
Een van de belangrijkste lessen uit het werk is dat het omvangrijke, stikstofrijke raamwerk rond de Al=P‑eenheid niet slechts steigerwerk is; het stuurt hoe en waar reacties plaatsvinden. Door hun resultaten te vergelijken met eerdere, kortlevendere aluminium‑fosforsystemen tonen de auteurs aan dat kleine veranderingen in de dragende liganden de balans tussen verschillende routes omkeren, zoals eenvoudige additie over de dubbele binding versus meer uitgebreide bindingssplijting en ringvorming. Geavanceerde analyses van elektronenverdeling onthulden sterke polarisatie van de Al=P‑binding en benadrukten hoe naburige stikstofatomen met aluminium kunnen samenwerken, vooral bij waterstofactivatie. Sterische omvang—de fysieke krapte van grote groepen—duwt binnenkomende moleculen ook richting de ene of de andere reactieve plaats.
Wat dit betekent voor toekomstige chemie
Voor niet‑specialisten kan de alfabetsoep van reagentia in deze studie ver weg lijken, maar de onderliggende boodschap is duidelijk: door zowel de bindingen als de vorm rond hoofdgroepelementen zorgvuldig af te stemmen, kunnen chemici wendbare hulpmiddelen bouwen die traditionele metaal katalysatoren evenaren of aanvullen. Dit isoleerbare aluminium‑fosforcomplex overleeft niet alleen in een fles, maar pakt ook een breed scala aan hardnekkige kleine moleculen aan onder milde omstandigheden, splijt waterstof, herschikt wit fosfor en vangt kooldioxide. Het werk laat zien dat subtiele veranderingen aan het „handvat” van een molecuul zijn reactiviteit diepgaand kunnen ombuigen, en biedt een blauwdruk voor het ontwerpen van toekomstige katalysatoren die eenvoudige, stabiele moleculen met precisie en efficiëntie omzetten in waardevollere producten.
Bronvermelding: Cha, Y., Yang, Z., Zhuang, X. et al. An isolable phosphaalumene(3) capable of small molecule activation via unique modes of reactivity. Nat Commun 17, 2390 (2026). https://doi.org/10.1038/s41467-026-69118-4
Trefwoorden: activatie van kleine moleculen, hoofdrij chemie, aluminium-fosfor dubbele binding, gefrustreerd Lewis-paar, bindingsactivatiemechanismen