Clear Sky Science · nl
Remmingsmechanisme van schimmel β−1,3-glucaan-synthases door triterpenoïde antischimmelmiddelen
Waarom het stoppen van schimmelinfecties belangrijk is
Schimmelinfecties doden stilletjes meer dan een miljoen mensen per jaar en vormen wereldwijd een bedreiging voor gewassen en ecosystemen. Artsen hebben al maar een beperkte voorraad antischimmelmiddelen, en sommige gevaarlijke schimmels evolueren om deze te ontwijken. Deze studie onthult op moleculair niveau hoe een nieuwe klasse antischimmelmiddelen zich vasthecht aan en een essentieel enzym uitschakelt dat schimmels nodig hebben om hun beschermende celwand te bouwen. Inzicht in dit proces biedt een routekaart om betere behandelingen te ontwerpen die resistente schimmels te slim af kunnen zijn.
De bakker van de schimmelcelwand
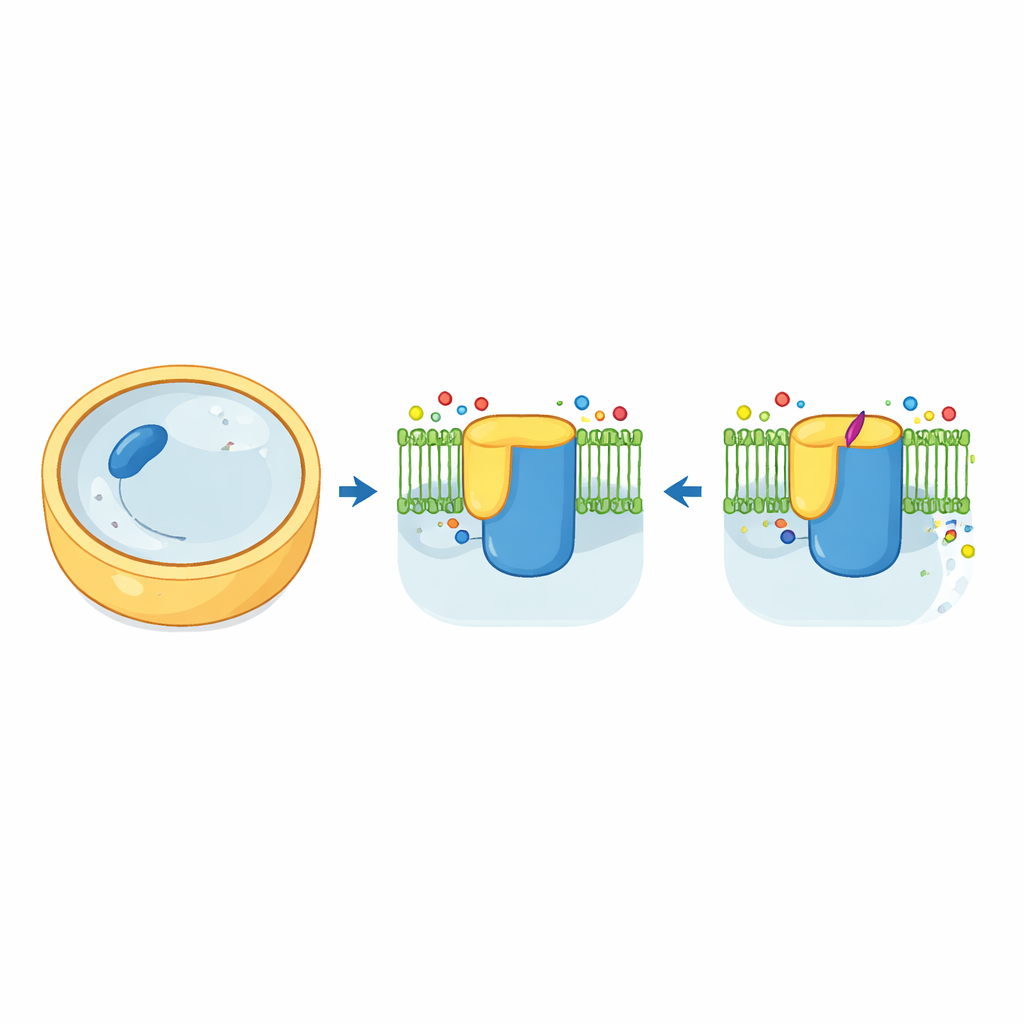
Schimmelcellen zijn omgeven door een stevige wand die grotendeels bestaat uit een suikergedragen polymeer genaamd beta-1,3-glucaan. Het enzym dat dit polymeer vervaardigt en exporteert, bekend als beta-1,3-glucaan-synthase, werkt als een baksteenmaker en transportband in één. In gist (Saccharomyces) bestaat dit machinerie uit twee zeer vergelijkbare versies, Fks1 en Fks2, elk ingebed in het celmembraan en gereguleerd door een kleine hulpstof genaamd Rho1. Met cryo-elektronenmicroscopie legden de auteurs driedimensionale, hoge-resolutie beelden vast van zowel Fks1 als Fks2 in hun natuurlijke toestand. De structuren tonen een groot cytosolisch “werkblad” verbonden met een woud van membraan-doorstekende helixen, met een centrale holte die waarschijnlijk fungeert als de tunnel waardoor de groeiende glucaanketen de cel verlaat.
Hoe een natuurlijk product het enzym grijpt
Klinisch belangrijke triterpenoïde geneesmiddelen, waaronder het orale middel ibrexafungerp, vinden hun oorsprong in een natuurlijk bestanddeel genaamd enfumafungin. Tot nu toe wist men niet precies waar op de glucaan-synthase deze middelen binden. De onderzoekers bepaalden structuren van zowel Fks1 als Fks2 gebonden aan enfumafungin. Verrassend genoeg klemt het middel zich niet in het actieve centrum waar suikereenheden worden gekoppeld. In plaats daarvan nestelt het zich aan de buitenzijde van een enkele membraanhelix genaamd TM5, in het membraan op ongeveer drie nanometer van het katalytische centrum en nabij het waarschijnlijke glucaan-uitgangskanaal. Belangrijke aminozuren in dit vlak omklemmen de hydrofobe kern van het middel en raken zijn zure staart, terwijl het suikerzetel nauwelijks het eiwit raakt — wat verklaart waarom chemici dat gedeelte hebben kunnen aanpassen zonder verlies van werkzaamheid.
Geneesmiddelen die een bewegende machine bevriezen
Op het eerste gezicht lijkt de algemene vorm van het enzym met en zonder enfumafungin vrijwel ongewijzigd. Het cruciale verschil zit in de organisatie van de omliggende lipiden en in de flexibiliteit van bepaalde helixen. Wanneer het middel bindt, roteert een nabijzijnde aromatische zijketen om enfumafungin vast te klemmen en stabiliseert, samen met een ander residu, een geordende lipidelaag naast het middel. Aanvullende sterolachtige lipiden ordenen zich keurig rond een reeks horizontale helixen die helpen het pad voor glucaanexport te definiëren. Deze lipiden werken als wiggen en steunen, waardoor de helixen en de kanaalopening in een bepaalde “basale” configuratie worden vergrendeld. Genetische proeven tonen dat wijziging van veel van de contactpunten voor het middel of deze sterolen de binding verzwakt of de enzymfunctie vernietigt, en mutaties op deze plaatsen komen overeen met bekende resistentiemutaties in menselijke en plantpathogenen.
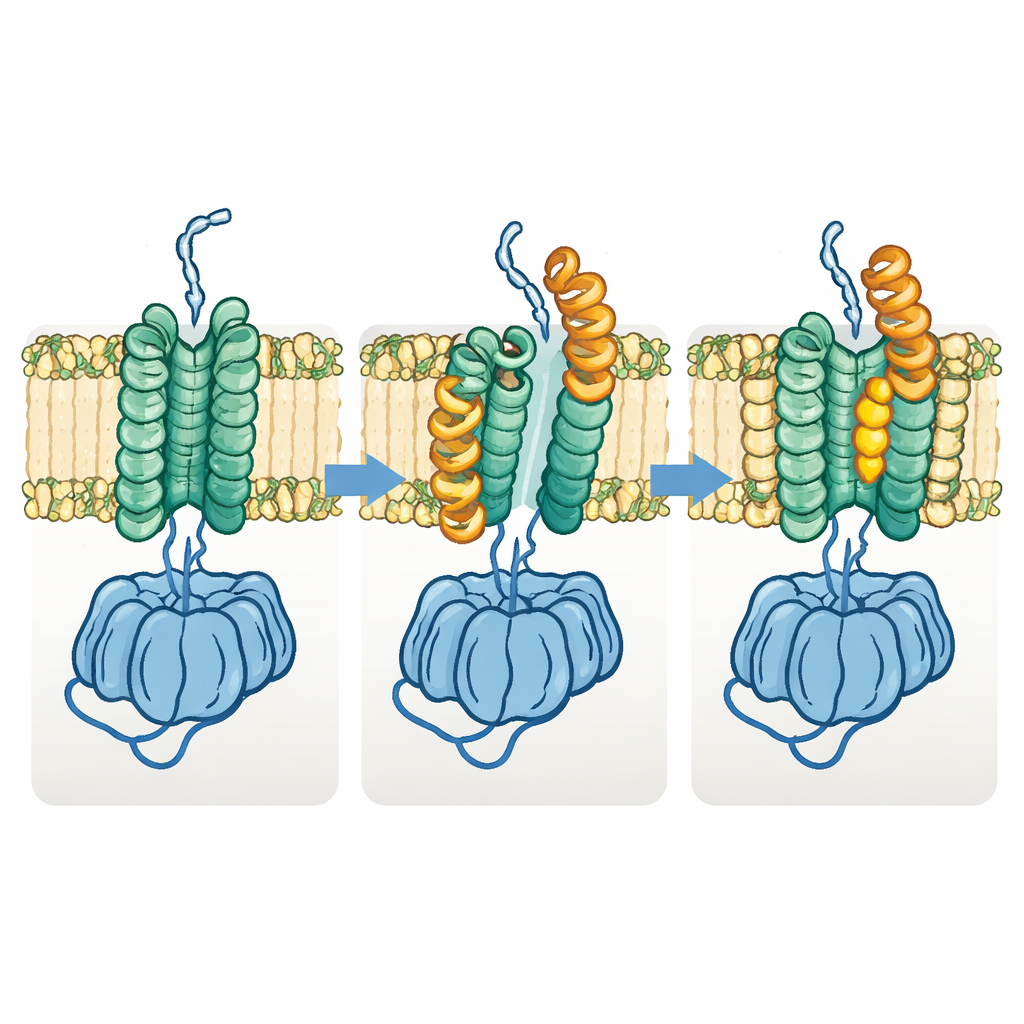
Een noodzakelijke vormverandering voor polymeertransport
Het team ontdekte ook een onderscheidende “open” vorm van Fks1. In deze toestand verschuift de ene helft van het membraangebied zijdelings en zwaaien sleutel-horizontale helixen naar buiten, waardoor de ruimte tussen de twee membraanbundels wordt opengesperd en de schijnbare glucaantunnel wijder wordt. Vergelijking van vele structuren suggereert dat het enzym tijdens normale werking tussen de basale en open toestanden schakelt: de basale toestand bereidt de polymerisatie voor en initieert die, terwijl de open toestand de groeiende keten in staat stelt zich zijwaarts door het membraan naar buiten te verplaatsen. Toen de auteurs disulfidebruggen inbrachten om het enzym permanent in een van beide toestanden te vergrendelen, verloren beide varianten grotendeels hun activiteit, wat ondersteunt dat deze vormverandering essentieel is voor de functie.
Wat dit betekent voor toekomstige antischimmelmiddelen
Door aan te tonen dat enfumafungin en verwante middelen niet het katalytische vlak blokkeren maar de lokale membraanomgeving hervormen en de glucaan-synthase in zijn basale toestand bevriezen, onthult deze studie een onconventionele wijze van geneesmiddelwerking. De studie laat ook zien dat Fks1 en Fks2 vrijwel identieke structuren en geneesmiddelresponsen delen, wat verklaart waarom beide in beschouwing moeten worden genomen bij het bestrijden van resistentie. Meer algemeen benadrukt het werk hoe kleine moleculen ‘onbehandelbare’ membraaneiwitten kunnen beïnvloeden door zich aan ondiepe oppervlakken te binden en lipiden te rekruteren, en biedt het een conceptueel sjabloon voor het ontwerpen van volgende-generatie antischimmelmiddelen die effectief blijven naarmate schimmels evolueren.
Bronvermelding: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Trefwoorden: antischimmelmiddelen, schimmelmembraan, glucaan-synthase, medicijnresistentie, cryo-elektronenmicroscopie