Clear Sky Science · nl
Cryo-EM-structuren van bacteriofaag T4-portal-nekasembly-intermediairen onthullen een mechanisme voor het vasthouden van het virale genoom
Hoe een virus zijn DNA onder druk houdt
Bacteriofaag T4 is een virus dat E. coli-bacteriën infecteert en zijn DNA zo strak in zijn kop verpakt dat de druk binnenin vijf tot zeven keer hoger kan zijn dan in een champagnefles. Toch lekt het DNA niet weg terwijl het virus de rest van zijn lichaam afrondt. Deze studie onthult, op moleculair niveau, hoe T4 dat probleem oplost met een klein dubbeldeursysteem dat als een luchtsluis voor zijn genetisch materiaal fungeert.
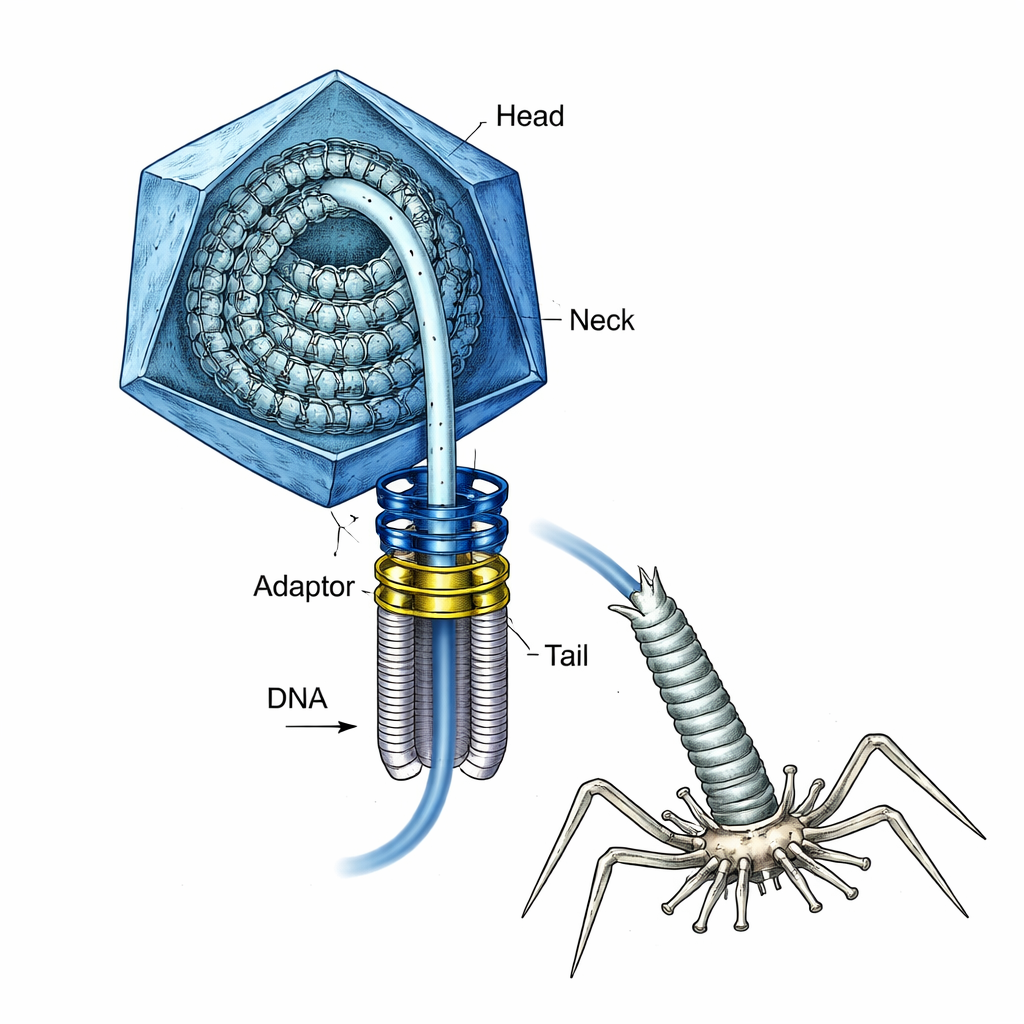
Het virus met een geladen veer binnenin
T4 is lange tijd een werkpaard geweest in de moleculaire biologie en dient ook als model voor het ontwerpen van toekomstige vaccins en genleveringsmiddelen. Tijdens de assemblage bouwt het virus eerst een lege eiwitmantel, of kop, en een speciale ringvormige “portal” op één hoekpunt. Een krachtige moleculaire motor trekt dan het DNA via deze portal in de kop totdat de kop “vol” is. Op dat moment moet de motor loskomen, moeten nek en staart worden aangebracht en later moet het DNA in een bacterie worden geïnjecteerd—zonder dat het onder druk staande DNA voortijdig naar buiten spuit. Hoe het virus dit hooggespannen DNA veilig opsloot tijdens die overgangsfasen was niet goed begrepen.
De nek in het lab herbouwen
De onderzoekers reconstrueerden sleutelonderdelen van T4 in bacteriën en brachten ze gecontroleerd samen om te observeren hoe de nek—de verbinding tussen kop en staart—assembleert. Twee virale eiwitten, gp13 en gp14 genoemd, werden apart geproduceerd. Op zichzelf zwommen ze als losse eenheden rond, maar samen schoten ze in elkaar tot gestapelde ringen die een centraal tunnel vormen voor DNA-passages. Tot verrassing van de wetenschappers verscheen een derde eiwit steeds in deze preparaten: Hfq, een bekend bacterieel eiwit dat doorgaans helpt bij de regulatie van RNA en genactiviteit in E. coli. Massaspectrometrie bevestigde dat Hfq specifiek aan gp14 bindt, wat suggereert dat het virus dit gastheereiwit leent als onderdeel van zijn nek.
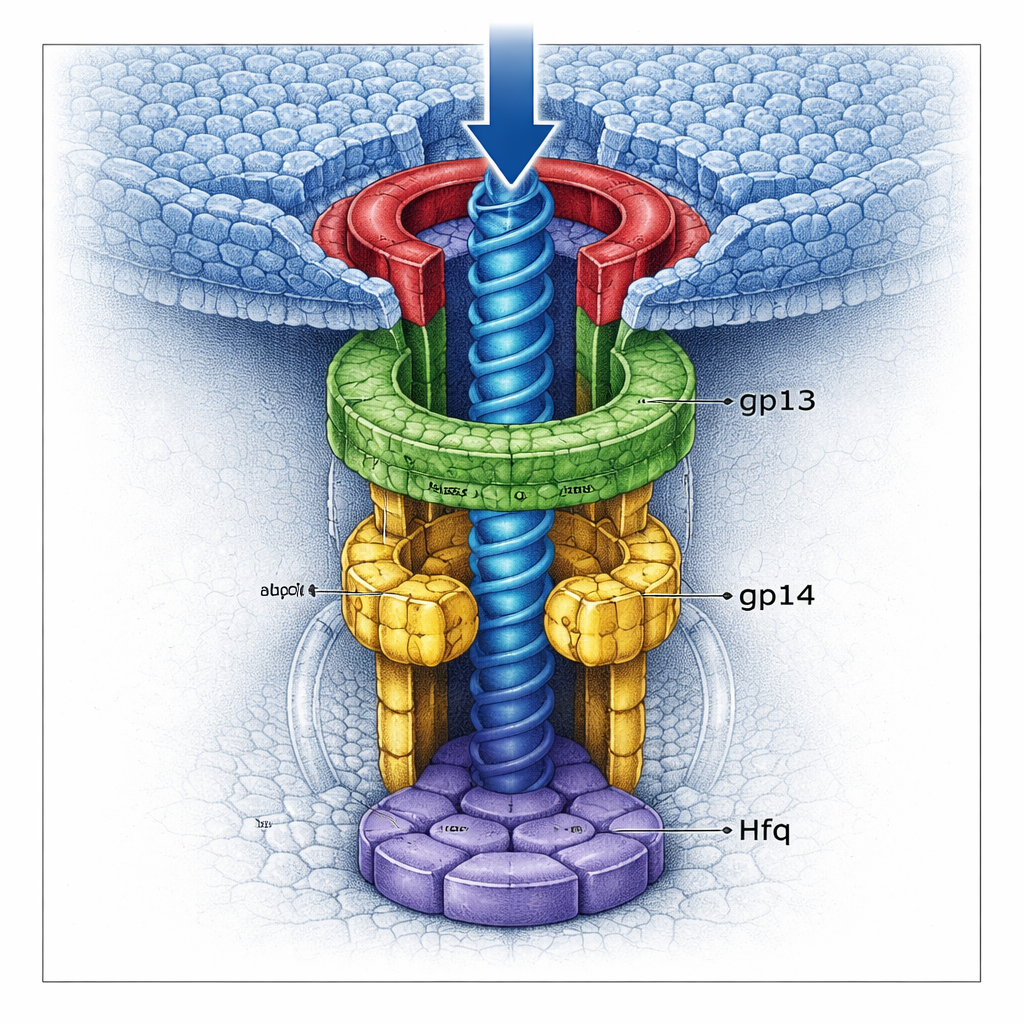
Een dubbele deur die het genoom vergrendelt
Met behulp van hoogresolutie kryo-elektronenmicroscopie visualiseerde het team meerdere versies van het nekscomplex tot bijna atomair detail. Ze ontdekten dat gp13 een brede ring vormt die zich aanpast aan de portal, terwijl gp14 eronder zit als een hexameer en een smallere doorgang creëert. Cruciaal is dat elk gp14-subunit een lange lus bijdraagt die naar het midden van de tunnel zwaait. Samen vormen zes van zulke “stoplussen” een dichte poort die het laatste segment DNA kan grijpen als het probeert de kop te verlaten. Onder gp14 assembleert het gekaapte Hfq-eiwit tot zijn eigen hexameer en sluit de onderzijde van het kanaal af als een tweede deur. Wanneer Hfq aanwezig is, is de gp13–gp14-structuur vollediger en stijver, en vernauwen de gecombineerde deuren de tunnel nog verder, waardoor DNA-lekkage aanzienlijk minder waarschijnlijk wordt.
Timing, foutpreventie en een geleende hulp
De studie toont ook aan dat dit systeem meer is dan een statische stop; het is een zorgvuldig gechoreografeerde reeks van vormveranderingen. Zodra de kop vol is, duwt de interne druk de portal in een nieuwe conformatie die bindingsplaatsen voor gp13 blootlegt. Een vooraf samengestelde gp13–gp14–Hfq-nek dockt vervolgens op de portal. Gp13 buigt, zwaait omhoog en vergrendelt zich zowel op de portal als op de buitenmantel, waardoor de nek stevig in de kop wordt geweven. Gedurende deze fase houden de gp14-stoplussen en de Hfq-stopper het DNA op zijn plaats. Hfq vervult een tweede rol als kwaliteitscontrolefactor: door sleuteloppervlakken op gp14 te bezetten voorkomt het dat gp14 in de verkeerde positie aan de portal bindt, wat tot foutieve assemblage van de nek zou leiden. Pas wanneer de vooraf gebouwde staart arriveert, vormt een staartpoteiwit, gp15, een nog sterkere binding met gp14, verdrijft Hfq en opent de weg voor gecontroleerde DNA-afgifte in de staart.
Waarom dit belangrijk is buiten één virus
In eenvoudige bewoordingen gebruikt T4 een tweedeurveiligheidsslot om een krachtige DNA-“veer” tegen te houden terwijl het de rest van het virus afbouwt. De eerste deur is opgebouwd uit zijn eigen nek-eiwit, gp14, en de tweede deur wordt geleend van het gastheer-eiwit Hfq, dat het virus tijdelijk gebruikt en daarna loslaat. Deze dubbele poort zorgt ervoor dat vrijwel geen DNA verloren gaat en dat het uiteindelijke virus volledig infectieus is. Omdat veel grote virussen hun genomen onder vergelijkbare extreme drukken verpakken en verwante architectuur delen, suggereert dit werk dat vergelijkbare sleutelsystemen, en zelfs het tijdelijke kapen van gastheereiwitten, wijdverspreid kunnen zijn. Inzicht in deze mechanismen kan het ontwerp van veiligere virale vectoren voor de geneeskunde sturen en aanwijzingen bieden voor nieuwe manieren om schadelijke virussen te blokkeren door hun genoom-„sloten” te richten.
Bronvermelding: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
Trefwoorden: bacteriofaag T4, virale assemblage, kryo-elektronenmicroscopie, genoomverpakking, gastheer–virusinteractie