Clear Sky Science · nl
In situ-structuren van het portal-neus-staartcomplex van bacteriofaag T4 verhelderen een mechanisme voor positionering van het virale genoom
Hoe een virus zijn genetische veer laadt
Bacteriofagen — virussen die bacteriën infecteren — behoren tot de meest verfijnde nanomachines in de natuur. Een van de best onderzochte, bacteriofaag T4, moet zijn lange DNA-genoom in een piepkop proppen en het vervolgens in een fractie van een seconde in een bacterie schieten. Deze studie onthult, bijna atoom voor atoom, hoe T4 zijn DNA zorgvuldig positioneert als een samengeperste veer in zijn staart, klaar om in een nieuwe gastheercel te worden afgevuurd zonder ook maar één genetische "letter" te verliezen. 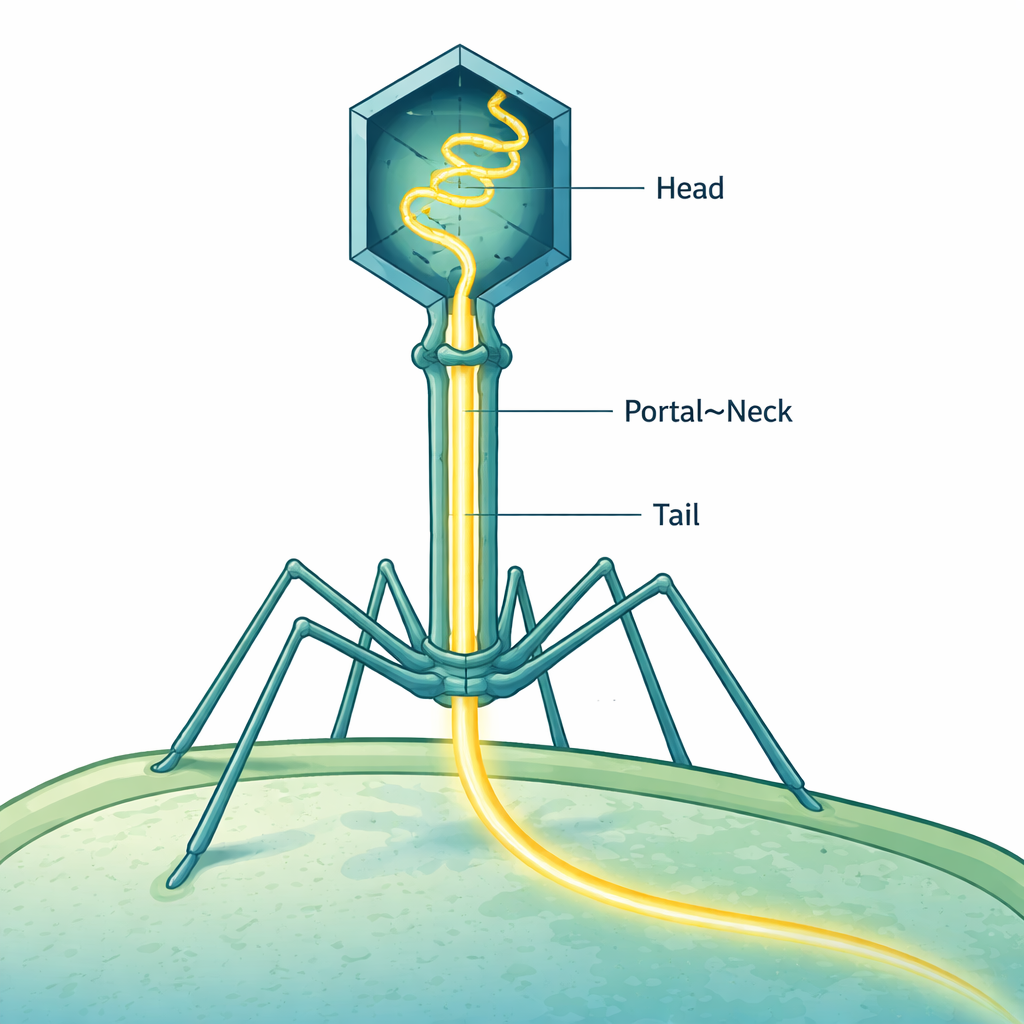
Een hoog-druk viraal hoofd
Binnen de eiwitschelp van de faag is het DNA dicht opeengepakt tot bijna kristalstructuur-dichtheid, waardoor een interne druk ontstaat van ongeveer 25–35 atmosfeer — vergelijkbaar met de druk in diepe oceaangroeven. De onderzoekers gebruikten hogeresolutie cryo-elektronenmicroscopie om te visualiseren wat er gebeurt bij het speciale “portaal” waar het DNA het hoofd binnenkomt en verlaat. Ze vonden dat wanneer het hoofd vol raakt, het ringvormige portal-eiwit van vorm verandert — van een schijfachtige naar een paddenstoelachtige structuur — en relatief naar beneden verschuift ten opzichte van de schaal. Deze drukgedreven verschuiving lijkt het signaal te geven dat er voldoende DNA is verpakt, waardoor de motor die het DNA naar binnen pompte loslaat en nieuwe aankoppelplaatsen voor het volgende deel van het virale apparaat blootlegt.
Opbouwen van een vergrendelende nek tussen kop en staart
Zodra het DNA-hoofd vol is, assembleert er een nekstructuur tussen kop en staart die fungeert als zowel connector als klep. Twee nek-eiwitten, gp13 en gp14 genaamd, vormen ringen onder het portaal. Gp13 zwaait een deel van zijn structuur omhoog om het portaal vast te grijpen en reikt ook naar de omliggende schaal, waarmee kop en nek stevig aan elkaar worden gebonden en bevestigingspunten voor decoratieve vezels bieden. Gp14, dat eronder zit, vormt aanvankelijk samen met een gastheer-eiwit genaamd Hfq een dubbele "genoomsluiting" die het uitgangskanaal effectief afsluit zodat het DNA onder hoge druk niet voortijdig kan ontsnappen. In deze verzegelde toestand stopt het DNA nabij de nek en wordt op zijn plaats gehouden terwijl de rest van het virus de assemblage voltooit.
Aankoppelen van de staart opent de klep
De volgende stap is het bevestigen van een voorgebouwde staart, bestaande uit een binnenbuis omgeven door een contractiele mantel en eindigend in een complex basisplaatje dat het bacteriële oppervlak herkent. Bovenaan deze staart bevindt zich een "staartterminator"-ring, gp15, en net daaronder sluit een andere ring, gp3, de binnenbuis af. Wanneer deze staart op de nek aanlegt, ondergaat gp14 een dramatische herschikking: de lusvormige delen die de poort vormen draaien naar beneden en klemmen zich vast aan gp15, terwijl een uitgestrekte staart van gp14 zich om gp15 wikkelt om een zeer groot, geladen contactoppervlak te vormen. Deze bewegingen verdrijven de Hfq-STOPPER en zwaaien de gp14-lussen uit de weg, waardoor de eens gesloten nek wordt getransformeerd tot een volledig open kanaal dat nu op één lijn ligt met de holle buis van de staart.
DNA gevangen door een moleculaire liniaal
Met de poort open stroomt het DNA — nog steeds onder hoge druk — niet simpelweg naar buiten. In plaats daarvan reist het ongeveer 17 nanometer door de nieuwgevormde portal–nek–staart-verbinding. Bij de overgang naar gp3 en de bovenkant van de staartbuis komt het DNA een "tape-measure protein" (TMP) tegen, een lang opgerold eiwit dat oorspronkelijk als liniaal diende om de lengte van de staart te bepalen. Het uiteinde van TMP bevat DNA-bindende segmenten die de top van het genoom grijpen. De aanhoudende druk vanuit het verpakte hoofd duwt dan dit DNA–TMP-complex verder naar beneden in de staartbuis, waarbij de coiled-coil segmenten van TMP als een veer worden samengedrukt en het DNA-eind naar de onderkant van de tweede ring van de staartbuis wordt verplaatst. 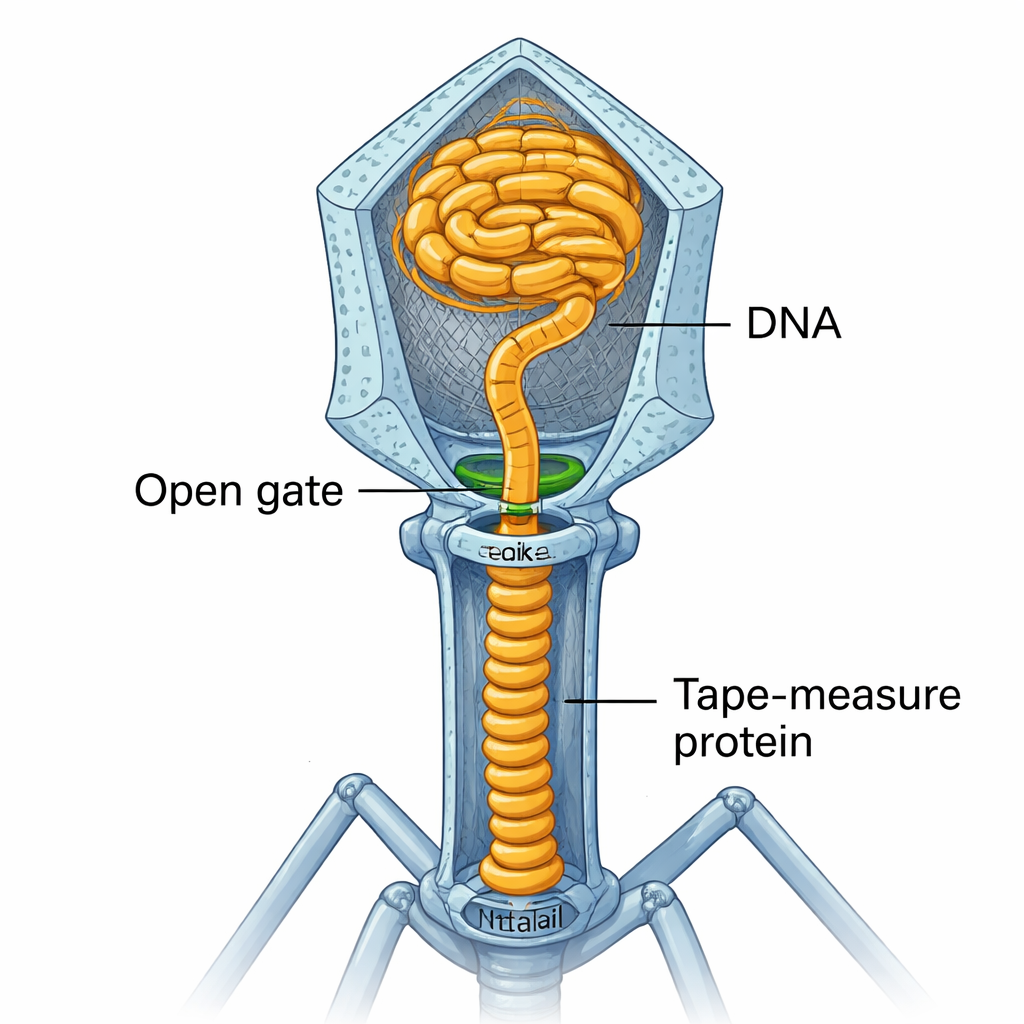
Een veerbeladen genoom gereed om af te vuren
Deze structurele momentopnamen tonen aan dat na assemblage het faaggenoom niet simpelweg in de kop wordt opgeslagen; het is doelbewust gepositioneerd zodat het voorste uiteinde diep binnen een intern tunnelstelsel hangt dat van de kop door de nek in de staart loopt. Het DNA wordt daar gehouden door het samengeperste tape-measure-eiwit en een "stopper" bij het basisplaatje, waardoor een metastabiele, veerbeladen toestand ontstaat. Wanneer het basisplaatje een bacterieel receptor waarneemt en zich eraan vastklikt, veroorzaakt dat veranderingen die deze stopper verwijderen en het samengeperste DNA–TMP-complex vooruit laten schieten, waardoor het genoom vloeiend de gastheercel binnengeleid wordt. In wezen heeft het virus een druk-aangedreven laad- en richtsysteem ontwikkeld dat snelle, volledige en betrouwbare aflevering van zijn genetische lading verzekert.
Bronvermelding: Fokine, A., Zhu, J., Klose, T. et al. In situ structures of the portal-neck-tail complex of bacteriophage T4 inform a viral genome positioning mechanism. Nat Commun 17, 1965 (2026). https://doi.org/10.1038/s41467-026-69106-8
Trefwoorden: bacteriofaag T4, verpakking van viraal DNA, cryo-elektronenmicroscopie, virusstructuur, faaginfectiemechanisme