Clear Sky Science · nl
Structurele basis van pauzes tijdens het starten van transcriptie in Mycobacterium tuberculosis
Hoe de gen-schakelaars van een kiem kunnen vastlopen
Mycobacterium tuberculosis, de bacterie die tuberculose veroorzaakt, moet voortdurend genen aan- en uitzetten om te overleven in de vijandige omgeving van het lichaam. Het werk dat in dit artikel wordt beschreven werpt een blik op een van de vroegste stappen van deze genetische regeling en legt een vluchtige “pauze” vast die optreedt precies wanneer de cel begint DNA in RNA te lezen. Het begrijpen van deze pauze helpt verklaren hoe de microbe beslist of hij een gen volledig activeert of de poging afbreekt — en kan uiteindelijk nieuwe zwakke plekken voor antibiotica aan het licht brengen.
Het bericht vanaf DNA beginnen
In bacteriën beweegt een groot eiwitcomplex, RNA-polymerase, langs het DNA om RNA te maken, de eerste stap richting eiwitproductie. Om te beginnen werkt het samen met hulp-eiwitten die sigmafactoren worden genoemd; die leiden het naar specifieke startplaatsen op het DNA en helpen een klein “belletje” in de dubbele helix te openen. Voor Mycobacterium tuberculosis is één van deze helpers, sigma E, bijzonder belangrijk wanneer de bacterie stress ervaart buiten het binnenste celmembraan. Een andere factor, CarD, helpt het open DNA-bubbel te stabiliseren. Samen vormen deze componenten een initiatiecomplex dat de eerste bouwstenen van RNA maakt voordat het óf besluit tot een volledig bericht óf de poging staakt en korte RNA-fragmenten vrijgeeft.
Een verborgen pauze van zes à zeven letters
Vorig biochemisch werk en studies op enkel-molecuulniveau suggereerden dat RNA-polymerase vaak al heel vroeg pauzeert, wanneer de nieuw gevormde RNA-keten slechts zes of zeven bouwstenen lang is. Die pauzes zijn echter extreem kort en moeilijk direct waar te nemen, waardoor hoge-resolutie structuren ontbraken. In deze studie gebruikten de auteurs cryo-elektronenmicroscopie om verschillende versies van het initiatiemachinerie van M. tuberculosis te bevriezen en te visualiseren. Ze ontwierpen DNA–RNA-skeletten die het complex vangen wanneer het RNA zes of zeven eenheden lang is en bepaalden structuren voor drie hoofdtoestanden: twee “regelmatige” initiatiecomplexen en een onderscheidend gepauzeerd initiatiecomplex.
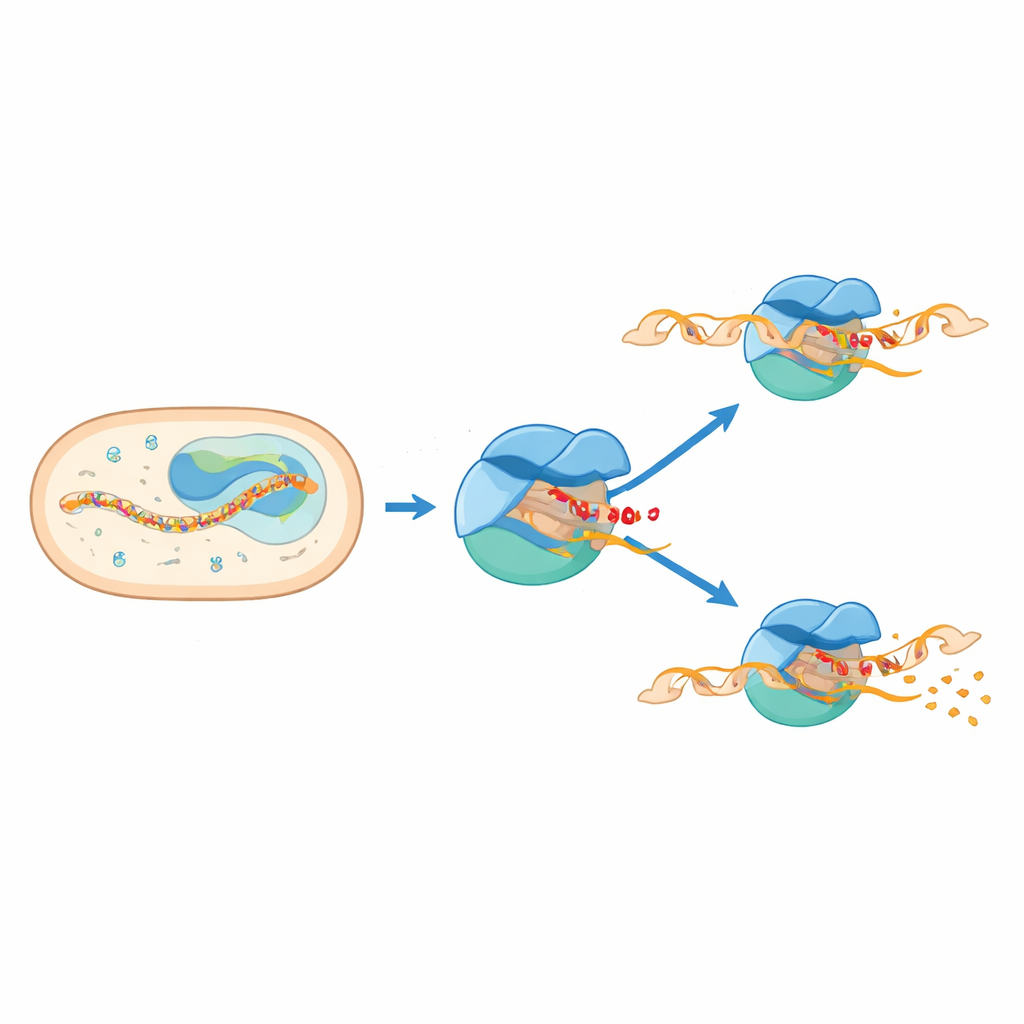
Wanneer twee delen van het machinaal in conflict komen
De structuren laten zien dat de pauze ontstaat wanneer twee delen van het complex proberen dezelfde ruimte in te nemen. Een flexibele sectie van sigma E, bekend als regio 3.2, steekt uit in het kanaal waarlangs het groeiende RNA moet passeren om het enzym te verlaten. Naarmate het RNA zes of zeven eenheden bereikt, botst het voortste uiteinde met deze uitstekende lus. Die botsing dwingt een zwenkende beweging af van een groot module binnen RNA-polymerase en vervormt een belangrijk structureel element, de brughelix. Tegelijkertijd wordt het DNA net stroomopwaarts van de actieve plaats naar binnen getrokken en deels ontwonden, waardoor een “opgesloten” en geknikte bubbel ontstaat. Deze gekoppelde bewegingen vergrendelen het complex in een gepauzeerde, half-gevorderde toestand die mechanische spanning opslaat.
Een vormveranderende helper stabiliseert de bubbel
CarD, de hulpfactor, blijkt een veelzijdigere rol te vervullen dan eerder werd aangenomen. In het niet-gepauzeerde initiatiecomplex klemt CarD zich in de minor groove van één DNA-streng aan de rand van de bubbel en helpt daarmee de bubbel open te houden zodat RNA-polymerase kan beginnen met synthetiseren. In het gepauzeerde complex verschuift CarD en grijpt nu de tegenoverliggende, niet-sjabloonstreng van DNA vast, waarbij het samen met sigma E de opgeschafte bubbel steviger vastzet. Biochemische tests tonen aan dat CarD sigma E–afhankelijke transcriptie versterkt en beïnvloedt hoeveel RNA-moleculen zich ophopen in de zes-tot-zeven-eenhedenfase. Deze bevindingen suggereren dat CarD zowel de initiële open toestand stabiliseert als helpt voorkomen dat het gepauzeerde complex voortijdig instort.
Een controlepunt tussen falen en toewijding
Door hoogresolutiestructuren op deels voorgeopend DNA te vergelijken met lageresolutiestructuren opgebouwd op volledig paarsend DNA, laten de auteurs zien dat dezelfde basisvormen van pauzering ook onder meer natuurlijke omstandigheden voorkomen. Ze stellen voor dat de botsing tussen het groeiende RNA en de sigma 3.2-lus een energiegeladen controlepunt creëert bij zes tot zeven RNA-eenheden. Vanuit deze geponeerde toestand kan het complex twee hoofdroutes volgen: het kan het korte RNA loslaten en zich resetten — een abortieve poging — of het kan de opgeslagen spanning gebruiken om los te breken van de promotorregio en over te gaan naar stabiele, langdurige RNA-productie. De herpositionering van CarD en het lossere houvast van de sigmafactor op het upstream-DNA lijken deze beslissing te sturen.
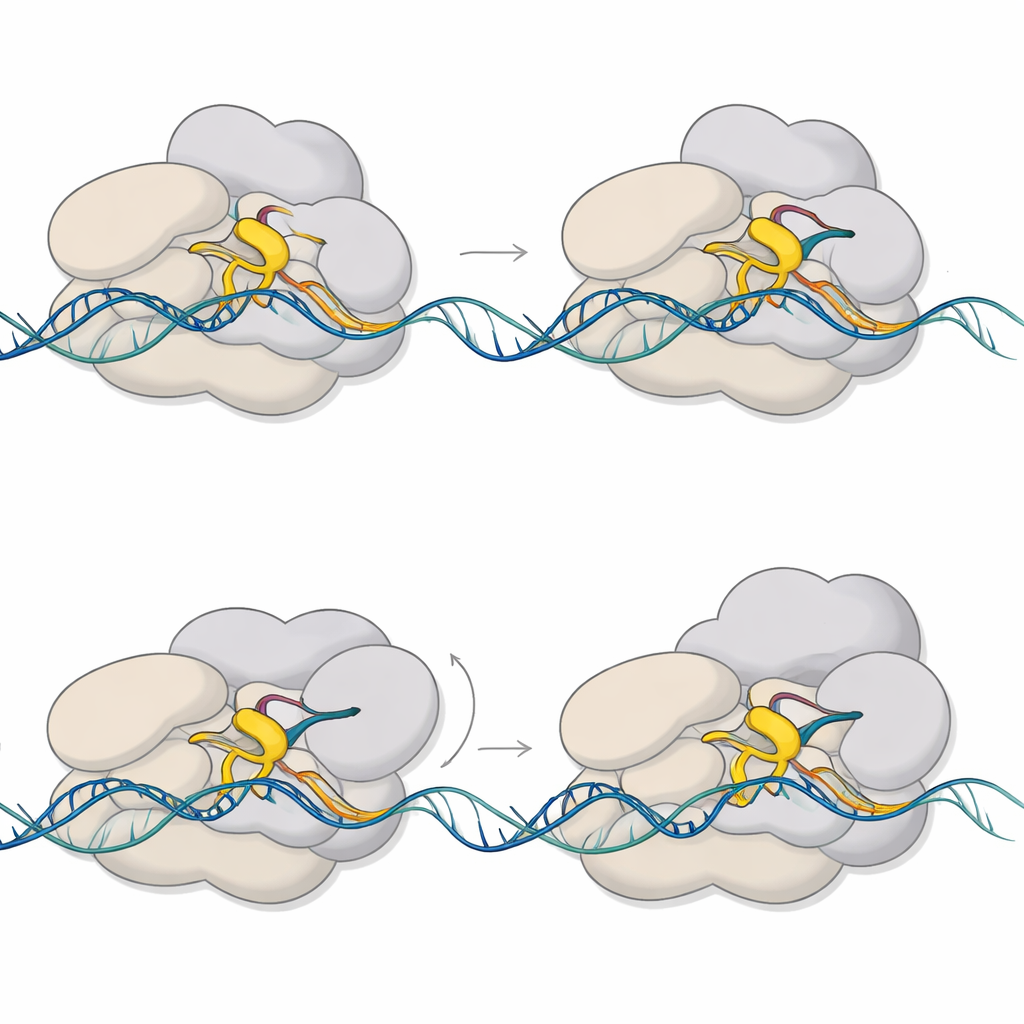
Waarom dit van belang is voor tuberculose
Voor een algemeen publiek is de hoofdboodschap dat de tuberkelbacterie genen niet simpelweg aanzet als een lichtschakelaar. In plaats daarvan aarzelt hij bij een uiterst kort RNA-lengte en gebruikt die korte mechanische pauze als een beslissingspunt tussen afbreken of toewijding aan volledige genactivatie. Dit werk legt die pauze vast tot op atomair niveau en toont hoe een kleine bewegende lus, een zwenkende kern en een hervormde DNA-bubbel samen een regelbaar controlepunt vormen. Omdat sigma E en CarD centraal staan in hoe M. tuberculosis op stress reageert, zouden deze inzichten onderzoekers uiteindelijk kunnen helpen middelen te ontwerpen die deze vroege stap blokkeren en het aanpassings- en overlevingsvermogen van de bacterie verzwakken.
Bronvermelding: Zheng, L., Xu, K. Structural basis of pausing during transcription initiation in mycobacterium tuberculosis. Nat Commun 17, 2197 (2026). https://doi.org/10.1038/s41467-026-69104-w
Trefwoorden: initiëren van transcriptie, pauzeren van RNA-polymerase, Mycobacterium tuberculosis, sigmafactoren, cryo-EM