Clear Sky Science · nl
Acuut door peritonitis geïnduceerde adipocyten CD127+ ILC1s uiten PD-L1 en verlichten ontsteking bij muizen
Waarom buikvet kan helpen dodelijke infecties te bestrijden
Wanneer bacteriën uit een gescheurde darm in de buik lekken, kan het lichaam verstrikt raken in een levensbedreigende toestand die sepsis wordt genoemd. Deze studie onthult een onverwachte bondgenoot in die strijd: een speciale groep immuuncellen die in buikvet schuilen, tijdens vroege infectie heen migreren en fungeren als een ingebouwde rem op ontsporende ontsteking. Begrijpen hoe deze cellen werken kan nieuwe behandelingen inspireren die gevaarlijke infecties kalmeren zonder het immuunsysteem volledig uit te schakelen.
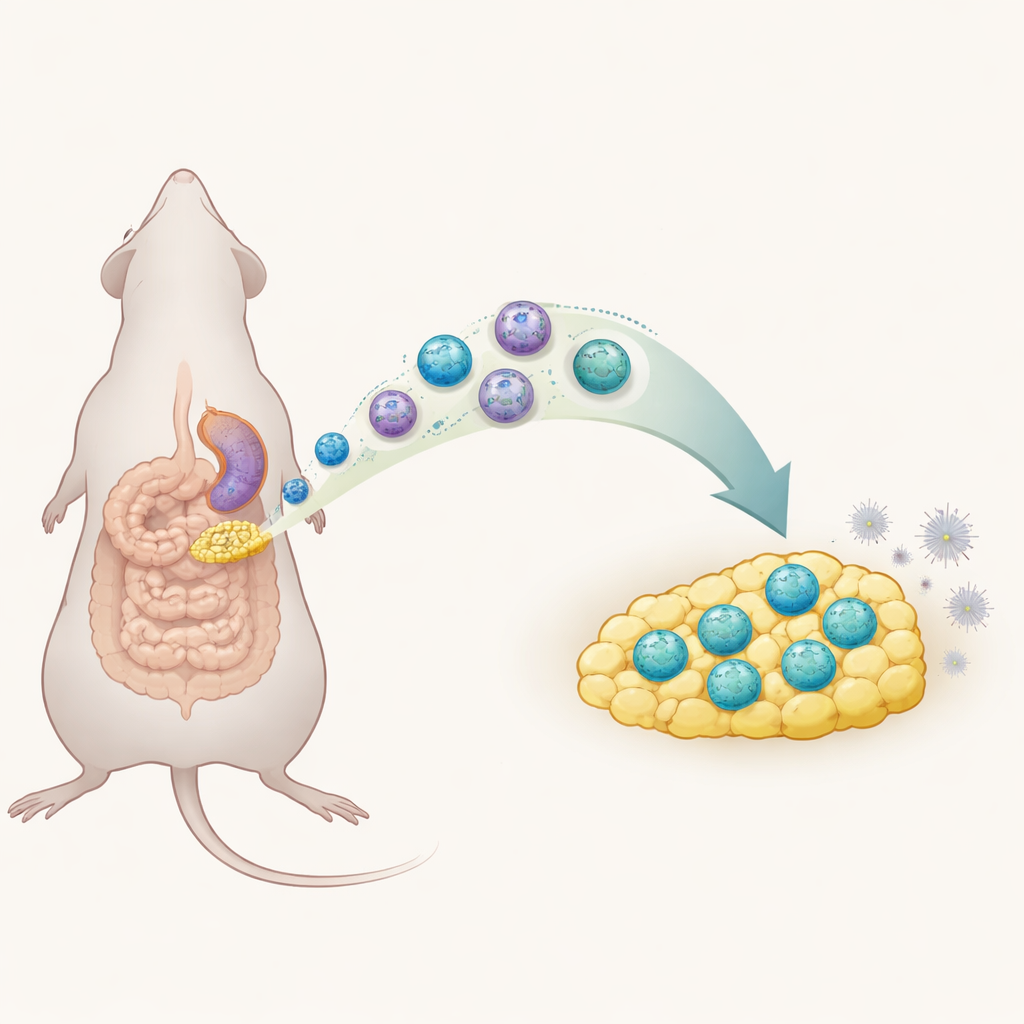
Een gevaarlijke lek in de buikholte
Peritonitis treedt op wanneer het slijmvlies van de buikholte ontstoken raakt, meestal doordat bacteriën uit een geperforeerde darm wegvloeien. Als deze vroege ontstorming niet wordt gecontroleerd, kunnen patiënten sepsis ontwikkelen, wat ondanks moderne zorg nog steeds ongeveer één op de vijf getroffenen doodt. Artsen kunnen de infectie behandelen met chirurgie en antibiotica, maar ze hebben weinig middelen om de eigen immuunreactie van het lichaam weg te sturen van schadelijke overactiviteit. Het vet dat over de darmen hangt, het zogenaamde mesenteriale vetweefsel, staat bekend om naar beschadigde plekken van de darm te trekken, wat suggereert dat het een actieve rol speelt in deze vroege immuunrespons.
Verborgen bewakers in buikvet
In de afgelopen jaren hebben wetenschappers “aangeboren lymfoïde cellen” ontdekt, snel reagerende immuensentinels die in veel weefsels leven. Eén subtype, groep 1 ILCs, helpt normaal gesproken bij het opwekken van sterke ontstekingsreacties. In deze muizenstudie gebruikten de onderzoekers een standaard chirurgisch model van peritonitis om te onderzoeken hoe deze cellen zich gedragen in mesenteriaal vet. Ze vonden dat zes uur na de beschadiging dit vet oplichtte met ontstekingssignalen en een toestroom van ILC1-cellen, terwijl andere verwante celtypen nauwelijks veranderden. Dit tijdsverloop kwam overeen met het ziektepiek in de dieren, wat suggereert dat ILC1s nauw verbonden waren met de vroege ontstekingsfase in de buikholte.
Reizende cellen die van aard veranderen
Dieper gravend gebruikten de onderzoekers geavanceerde enkel-celprofilering om de ILC1-populatie in subgroepen te verdelen. Onder normale omstandigheden ontbrak bij de meeste buikvet-ILC1s het molecuul CD127 op hun oppervlak. Tijdens acute peritonitis verscheen en breidde zich echter een nieuwe groep CD127-positieve ILC1s uit. Deze nieuwkomers produceerden minder van het krachtige ontstekingssignaal interferon-gamma dan hun CD127-negatieve verwanten, wat hen als opmerkelijk gematigd markeert. De wetenschappers toonden aan dat veel van deze cellen zich niet eenvoudigweg ter plaatse deelden: in plaats daarvan reisden ILC1s uit de milt via de bloedbaan naar mesenteriaal vet, deels gestuurd door een chemisch “homingsignaal” genaamd CXCL10 en zijn partnerreceptor CXCR3. Eenmaal in het vet veranderden hun oppervlaktemarkers, ze kregen CD127 en namen deze rustiger, meer regulerende persoonlijkheid aan.
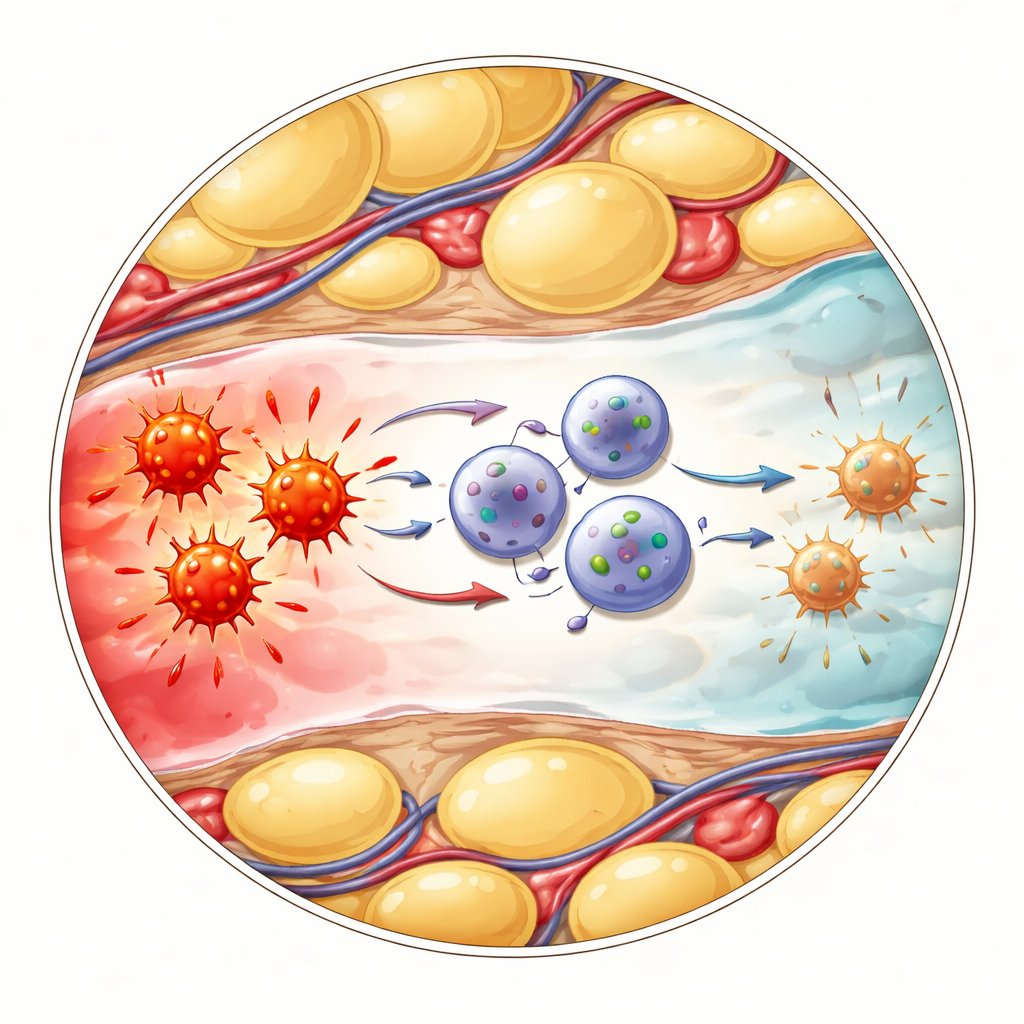
Hoe kalmerende cellen met vurige cellen communiceren
De volgende vraag was hoe deze gewijzigde ILC1s de ontsteking daadwerkelijk koelden. De onderzoekers richtten zich op een andere immuungroep, de gamma-delta T-cellen, die snel op gevaar reageren en grote hoeveelheden alarmerend molecuul TNF kunnen afgeven. Enkel-celanalyse suggereerde dat CD127-positieve ILC1s en gamma-delta T-cellen via een bekende “rem” route interacteren die de oppervlaktemoleculen PD-L1 en PD-1 omvat. In het geïnflammeerde buikvet verhoogden de nieuw aangekomen ILC1s sterk PD-L1, terwijl nabijgelegen gamma-delta T-cellen hoge niveaus van PD-1 vertoonden. Toen het team PD-1 met antilichamen blokkeerde, pompten gamma-delta T-cellen meer TNF uit, wat bevestigt dat dit contact hun ontstekingsuitvoer normaal gesproken beperkt. Evenzo leden muizen die genetisch zo waren aangepast dat ze geen ILC1s hadden aan ernstiger ziekte, hogere ontstekingsmarkers en meer TNF van gamma-delta T-cellen—effecten die konden worden verzacht door TNF direct te blokkeren.
Wat dit betekent voor toekomstige behandelingen
Samengevoegd stellen de auteurs een “milt‑naar‑buikvet” as voor: kort nadat bacteriën in de buik lekken, verlaten ILC1s de milt, trekken naar mesenteriaal vet en transformeren daar in CD127‑ en PD‑L1‑rijke cellen die de TNF‑productie door gamma‑delta T‑cellen dempen. In plaats van de vlammen aan te wakkeren, fungeren deze gespecialiseerde ILC1s als lokale vredestichters, voorkomen dat ontsteking overslaat en mogelijk helpen te voorkomen dat peritonitis uitdijt tot dodelijke sepsis. Op de lange termijn zouden geneesmiddelen die dit regulerende circuit in buikvet versterken of nabootsen een nieuwe manier kunnen bieden om ernstige infecties te behandelen—de immuunrespons zo afstemmen dat deze sterk genoeg blijft om ziekteverwekkers te bestrijden, maar niet zo sterk dat de patiënt gevaar loopt.
Bronvermelding: Nagata, R., Akama, Y., Goncalves, P. et al. Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice. Nat Commun 17, 2391 (2026). https://doi.org/10.1038/s41467-026-69100-0
Trefwoorden: peritonitis, aangeboren lymfoïde cellen, mesenteriaal vetweefsel, immuunregulatie, sepsis