Clear Sky Science · nl
Hernemen van nucleaire receptoren voor ligand‑gestuurde vorming van vloeibare condensaten en genregulatie
Hormonen omzetten in aan‑vragen beschikbare cel‑schakelaars
Onze cellen luisteren voortdurend naar signalen zoals hormonen en vitamines en zetten die om in acties, bijvoorbeeld het aan‑ of uitzetten van genen. Deze studie laat zien hoe wetenschappers in die natuurlijke taal kunnen tappen om synthetische “schakelaars” te bouwen die reageren op echte lichaamsignalen en zelfs kleine vloeibare druppels binnen cellen vormen om genactiviteit te versterken. Dergelijke hormoongestuurde schakelaars zouden op den duur kunnen helpen bij het ontwikkelen van slimmer getrainde gentherapieën, precieze biosensoren of ‘levende medicijnen’ die nauw gekoppeld zijn aan de fysiologie van een patiënt.
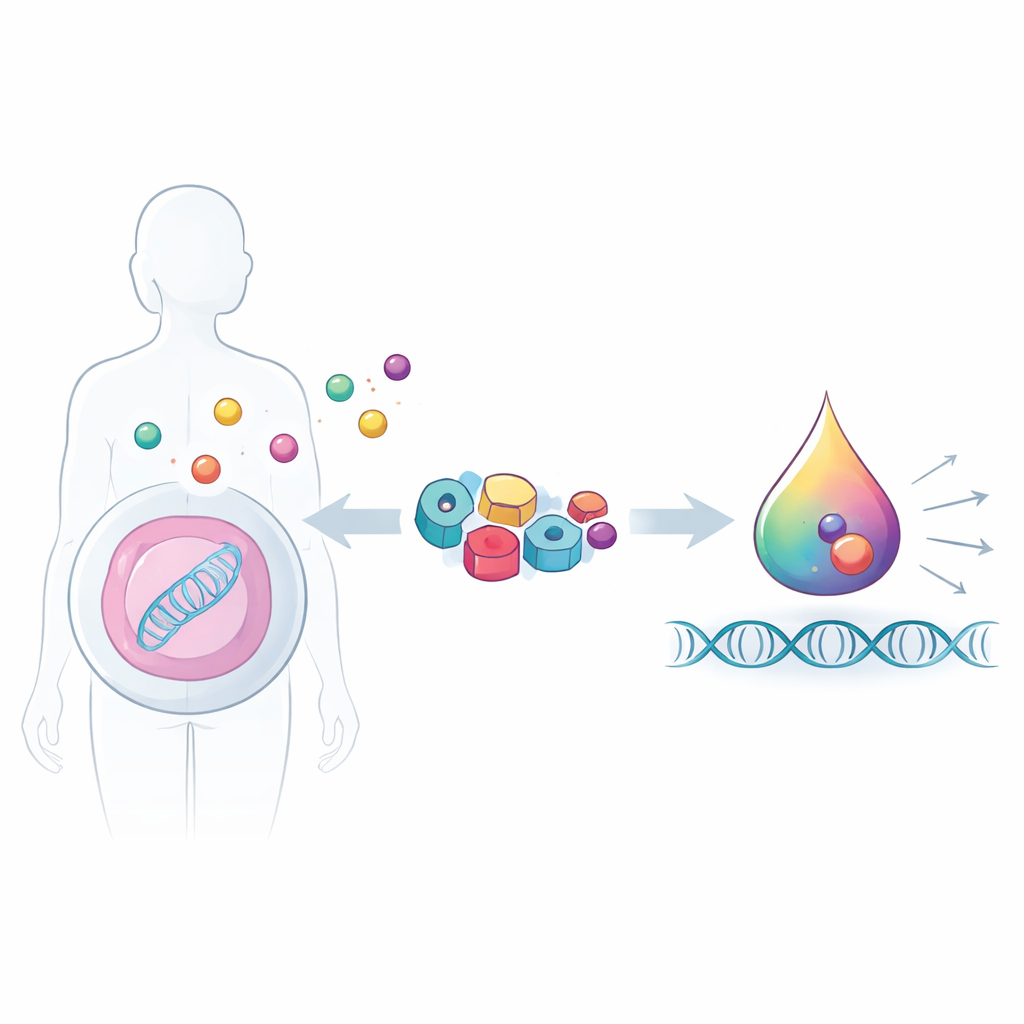
Gebruikmaken van de eigen signaallezers van de cel
Hormonen en verwante moleculen worden afgelezen door een familie eiwitten die nucleaire receptoren worden genoemd; deze receptoren zitten normaal in cellen en regelen genen als reactie op signalen zoals schildklierhormoon, vitamine D, oestrogeen en cortisol. Elke receptor heeft een holte die zijn specifieke hormoon bindt en een oppervlak dat hulp‑eiwitten, co‑activatoren genoemd, vastgrijpt wanneer het hormoon aanwezig is. In plaats van volledig kunstmatige onderdelen te ontwerpen, hergebruikten de onderzoekers deze natuurlijke receptoren en een klein stukje van een menselijk co‑activator‑eiwit (een korte TIF2‑peptide) als modulaire bouwstenen. Deze keuze betekent dat hun synthetische schakelaars dezelfde biochemische taal spreken als het lichaam, waardoor ze gemakkelijker in bestaande signaalroutes kunnen worden ingebouwd.
Chemische aan/uit‑schakelaars bouwen
Het team toonde eerst aan dat hormoonbinding twee ontwerp‑eiwitfragmenten op verzoek bij elkaar kon brengen. Ze fuseerden het ligandbindende deel van meerdere nucleaire receptoren aan de ene helft van een gesplitst rapportereiwit en fuseerden het TIF2‑peptide aan de andere helft. In menselijke cellen zorgde het toevoegen van het bijpassende hormoon ervoor dat de twee helften elkaar ontmoetten en het rapportersignaal herstelden, terwijl verwijderen of blokkeren van het hormoon de verbinding verbrak. Door receptoren te combineren met zowel hun activerende middelen (agonisten) als blokkermiddelen (antagonisten) bouwden ze tweevoudige schakelaars die door het ene middel konden worden ingeschakeld en door het andere konden worden uitgezet, soms herhaaldelijk en binnen enkele minuten. Ze gebruikten deze strategie ook om enzymen naar specifieke plekken binnen cellen te verplaatsen, waardoor lokale chemische niveaus op commando veranderden.
Genen controleren met vermenigvuldigde contacten
Om deze schakelaars om te zetten in genregelaars, koppelden de onderzoekers ze aan een CRISPR‑gebaseerd DNA‑bindend platform. Een “dode” Cas9‑proteïne werd naar gekozen DNA‑locaties geleid, terwijl de nucleaire receptor een sterk genactiverend domein droeg. Wanneer hormoon werd toegevoegd, hechtte de receptor zich aan TIF2‑segmenten die aan dCas9 waren bevestigd, waardoor de activator naar het doelgen werd gebracht. Een enkel TIF2‑segment gaf slechts bescheiden effecten, maar het aaneenschakelen van vele kopieën creëerde een multivalent landingsplatform dat veel receptoren tegelijk kon aantrekken. Dit verhoogde de genactivatie dramatisch—tot honderden keren boven het uitgangsniveau—en de respons bleef gevoelig binnen hormoonconcentraties die vergelijkbaar zijn met die in het lichaam. Antagonistische geneesmiddelen konden deze activiteit scherp terugschakelen, wat omkeerbare en precieze controle aantoont.
Vloeibare druppels creëren die expressie turbochargen
Toen het aantal TIF2‑kopieën toenam, merkte het team een scherp drempeleffect in de prestatie op, wat suggereerde dat de eiwitten mogelijk condenseerden tot druppels. Veel natuurlijke genregelaars vormen vloeibaar‑achtige “condensaten” die het benodigde transcriptie‑machinery concentreren. De onderzoekers ontwierpen opzettelijk steigers die veel TIF2‑motieven samenbinden met behulp van coiled‑coil‑peptiden, waardoor meerdere receptoren bij aanwezigheid van hormoon op dezelfde plek samenkomen. In levende cellen produceerde dit heldere, sferische druppels die zich als vloeistoffen gedroegen: ze fuseerden, herstelden zich na photobleaching en konden worden opgelost door chemicaliën die zwakke eiwitinteracties verstoren. Belangrijk is dat druppels alleen verschenen onder de juiste multivalente en hormonale omstandigheden, en dat antagonistische middelen ze konden laten verdwijnen, waarmee werd bewezen dat druppelvorming chemisch afstembaar is.
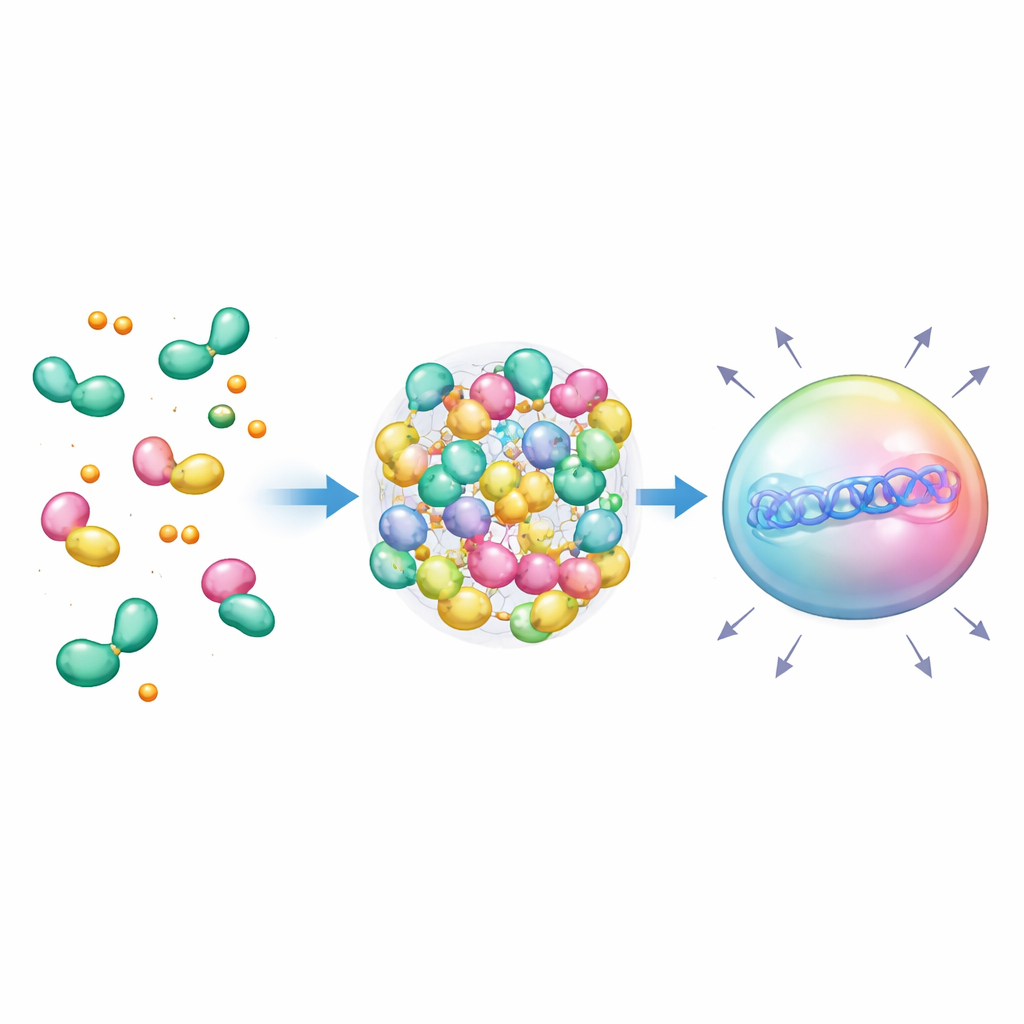
Van ontworpen druppels naar toekomstige therapieën
Door deze hormoongestuurde druppels te fuseren met DNA‑gerichte CRISPR‑instrumenten creëerden de auteurs nucleaire condensaten die direct boven specifieke genen zitten en hun activiteit enorm versterken—zelfs wanneer er slechts één DNA‑ankersite is. Omdat de componenten van menselijke oorsprong zijn en reageren op bekende signalen zoals cortisol en oestrogeen, zouden deze systemen uiteindelijk kunnen worden ingebed in therapeutische circuits die automatisch reageren op de hormoonspiegels van een patiënt. Hoewel zorgvuldige tests nodig zijn om te voorkomen dat ze interfereren met de eigen receptoren van het lichaam, illustreert dit werk een krachtig concept: natuurlijke hormoonlezers en vloeibare condensaten hergebruiken als programmeerbare schakelaars om de interne chemie te detecteren en gerichte genreacties aan te sturen.
Bronvermelding: Rihtar, E., Fink, T., Ivanovski, F. et al. Repurposing nuclear receptors for ligand-responsive liquid condensate formation and gene regulation. Nat Commun 17, 2218 (2026). https://doi.org/10.1038/s41467-026-69099-4
Trefwoorden: synthetische biologie, nucleaire receptoren, hormoonsignalering, genregulatie, fase‑scheiding