Clear Sky Science · nl
Een combinatorische synthetische strategie voor het ontwikkelen van eiwit-bezorgingsmiddelen voor genoomediting gericht op het muizennetvlies
Nieuwe hoop voor de behandeling van erfelijke blindheid
Veel vormen van erfelijke blindheid beginnen met één fout gen in de lichtgevoelige cellen achter in het oog. Moderne genbewerkingsmiddelen zoals CRISPR kunnen deze fouten in principe herstellen, maar het veilig afleveren van de bewerkende machinerie in de juiste cellen is een grote uitdaging geweest. Deze studie beschrijft een nieuwe manier om krachtige geneditors rechtstreeks in het muizennetvlies te vervoeren met speciaal ontworpen vetachtige deeltjes, wat de mogelijkheid opent voor eenmalige behandelingen die het gezichtsvermogen herstellen bij mensen met erfelijke oogaandoeningen.
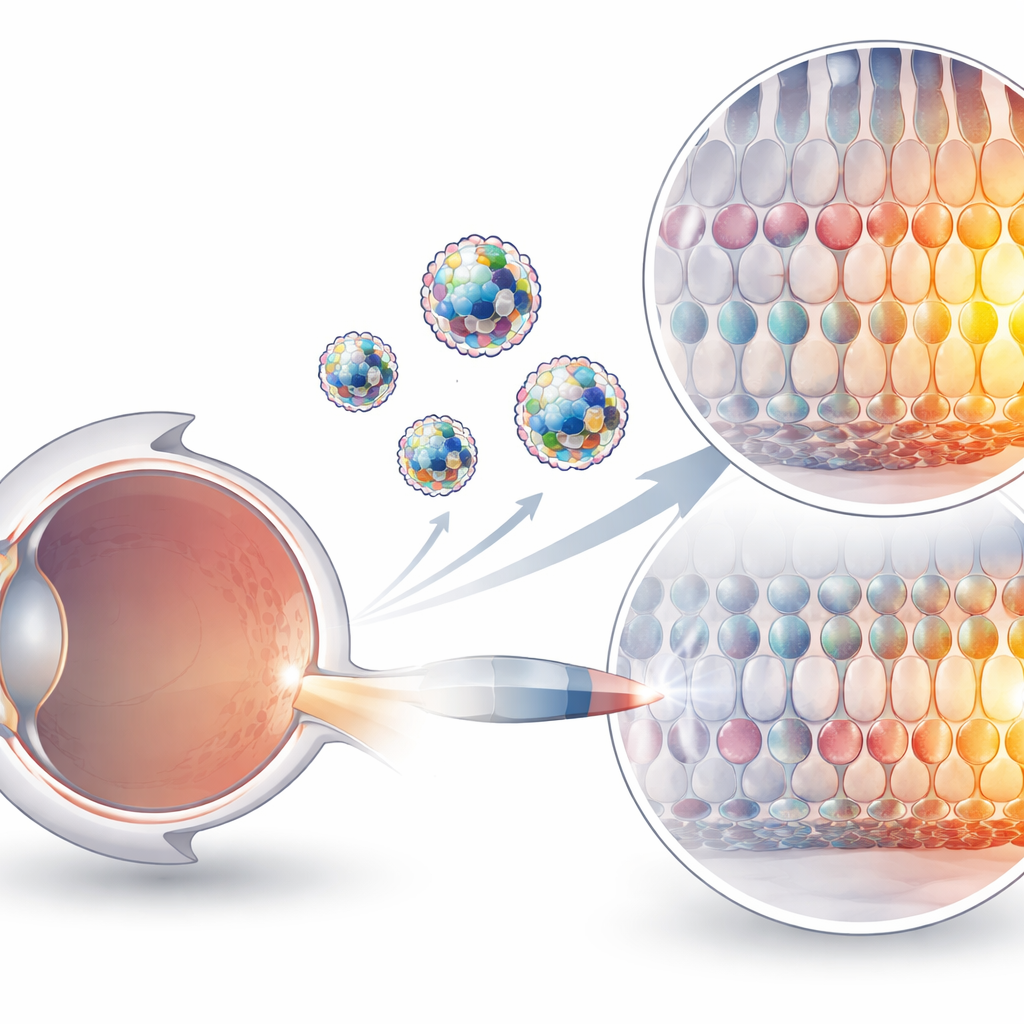
Waarom het afleveren van geneditors zo moeilijk is
Op CRISPR gebaseerde hulpmiddelen kunnen nu individuele DNA-letters veranderen zonder beide strengen door te knippen, een vooruitgang die ze aantrekkelijk maakt voor de behandeling van genetische aandoeningen. Maar deze hulpmiddelen zijn omvangrijke eiwit–RNA-complexen, geladen en kwetsbaar in het lichaam. Huidige aflevermethoden vertrouwen grotendeels op gemodificeerde virussen of op deeltjes die de genetische blauwdruk voor de editor vervoeren in plaats van de editor zelf. Virussen kunnen immuunreacties oproepen en hebben strikte afmetingslimieten, terwijl het afleveren van boodschapper-RNA zeer goed werkt in de lever maar in veel andere weefsels, inclusief het oog, inefficiënt blijft. Het direct injecteren van vooraf samengestelde eiwit–RNA-complexen is conceptueel schoner en veiliger, maar ze ontbraken tot dusver aan een geschikt voertuig om membranen te passeren en hun doelwitten te bereiken.
Een kleurstof-geïnspireerde shuttle voor eiwitten
De onderzoekers begonnen bij een onverwachte aanzet: Coomassie Brilliant Blue, een diepblauwe kleurstof die veel in laboratoria wordt gebruikt en al goedgekeurd is voor bepaalde oogoperaties. Deze kleurstof bindt sterk aan veel verschillende eiwitten. Het team koppelde chemisch Coomassie-"koppen" aan vetachtige "staarten" om een familie nieuwe moleculen te creëren die lipidoïden worden genoemd. In water hebben deze lipidoïden de neiging zich te clusteren tot deeltjes, waarbij de olieachtige delen naar binnen gericht zijn en de Coomassiegroepen naar buiten steken, waar ze eiwitten kunnen grijpen. Door de lengte, vertakking en lading van de staarten te variëren, bouwden de wetenschappers tientallen kandidaatverbindingen die bedoeld zijn om genbewerkings-eiwitten aan de ene kant te binden en met celmembranen aan de andere kant te interageren.
Testen van eiwitbezorging aan cellen van het oog
Om te onderzoeken welke ontwerpen echt werkten, gebruikte de groep eerst een eenvoudige test-eiwit genaamd Cre-recombinase dat een genetische schakelaar omzet van groen naar rood of van rood naar groen fluorescerend in gekweekte cellen en muizen. Verschillende Coomassie-lipidoïden brachten Cre efficiënt in gekweekte cellen, waardoor grote fracties cellen van groen naar rood overgingen. Wanneer ze onder het netvlies van reporter-muizen werden geïnjecteerd, veroorzaakten geselecteerde verbindingen opvallende kleurveranderingen zowel in de pigmentlaag die het zien ondersteunt als in de lichtgevoelige fotoreceptoren, wat toont dat de eiwitten de cellen bereikten die in veel blindheidsziekten het meest worden aangetast. Deze vroege experimenten toonden ook dat subtiele veranderingen in de lipidoïdstructuur konden verschuiven welke celtypen werden getarget, wat doet vermoeden dat toekomstige versies kunnen worden afgestemd op specifieke retinale lagen.
Versterken van genbewerking en het redden van gezichtsvermogen
Vervolgens laadde het team hun systeem met een adenine base-editor, een verfijnde CRISPR-variant die de specifieke enkellettermutatie kan corrigeren die gezichtsverlies veroorzaakt in rd12-muizen, een model van ernstige kinderblindheid. Op zichzelf drong het editor-eiwit–RNA-complex slecht in cellen door. Eén lipidoïde, genoemd CBB11, verbeterde de levering maar had de neiging te klonteren in oplossing. Om het te stabiliseren embedden de onderzoekers CBB11 in kleine, goed gedefinieerde liposomen—holle sferen gemaakt van verschillende soorten lipiden, waaronder klinisch gebruikte componenten uit mRNA-vaccins. In deze formuleringen pakte CBB11 aan het liposoomoppervlak het eiwitgedeelte van de editor, terwijl andere lipiden hielpen het RNA-geleidertje te binden, waardoor een coöperatieve schil ontstond die het hele complex aan de deeltjesbuitenkant vasthield.
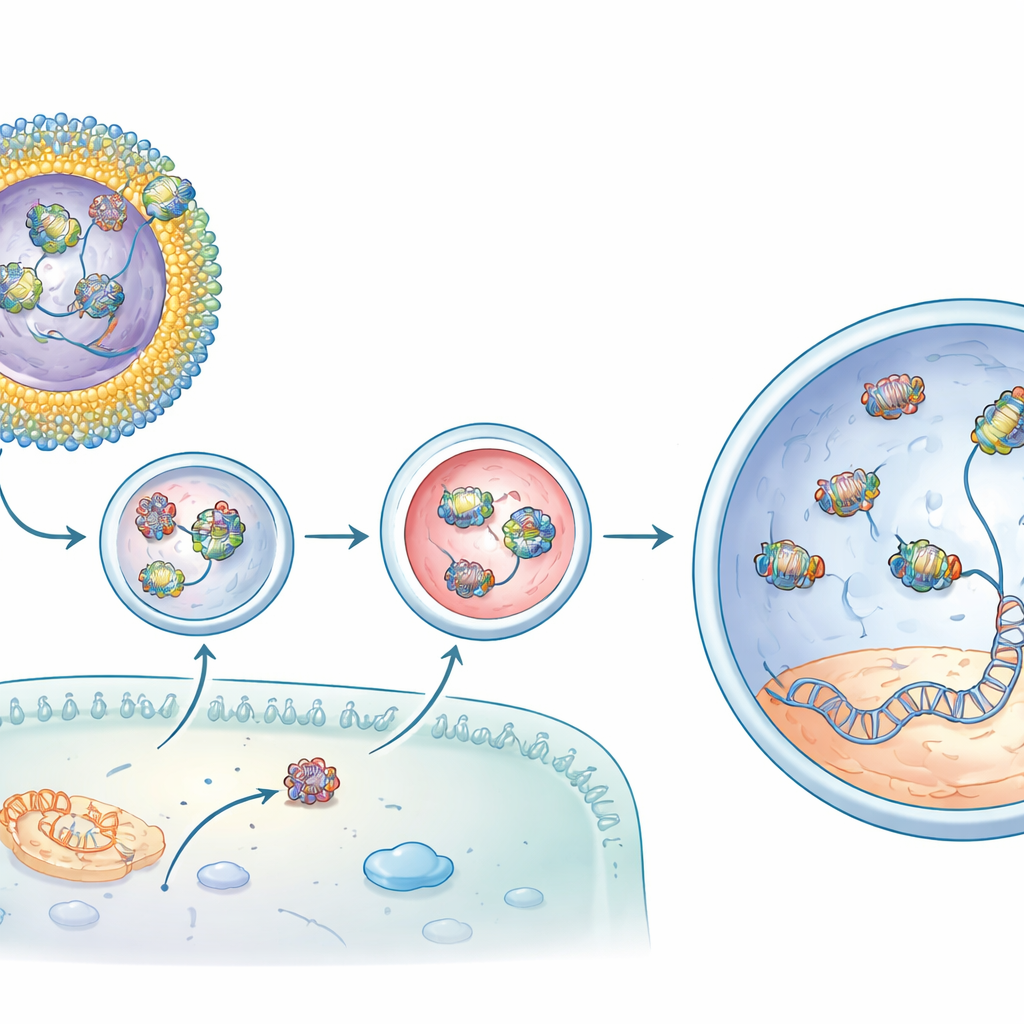
Van moleculair herstel naar herstelde lichtreacties
Wanneer deze CBB11-bevattende liposomen met de base-editor onder het netvlies van rd12-muizen werden geïnjecteerd, waren de resultaten opvallend. Vergeleken met de editor die alleen werd geïnjecteerd, verhoogde de geoptimaliseerde formulering de gewenste DNA-correctie in het doorgen gen met meer dan één grootorde en produceerde zelfs hogere niveaus van gecorrigeerd boodschapper-RNA. Chemische analyse toonde herstel van het lichtgevoelige retinaal pigment dat bij de ziekte ontbreekt. Het meest overtuigend waren elektrische opnames van de ogen van de dieren die aantoonden dat hun staafcellen veel van hun vermogen om op zwak licht te reageren herwonnen—tot ongeveer driekwart van het signaal van een normale muis in de beste gevallen. Off-target veranderingen elders in het genoom lagen op achtergrondniveaus, wat suggereert dat de bewerking zowel krachtig als nauwkeurig was.
Wat dit kan betekenen voor toekomstige otherapieën
Voor niet-specialisten is de kernboodschap dat de auteurs een herbruikbare "shuttlebus" voor genbewerkingseiwitten hebben ontwikkeld die rechtstreeks in het levende oog werkt. Door veilige, op vaccins lijkende vetdeeltjes te decoreren met een eiwit-grijzende kleurstof, creëerden ze een systeem dat verschillende editors aan zijn oppervlak kan vangen, ze in retinale cellen kan afleveren, ziekteveroorzakende mutaties kan corrigeren en meetbaar gezichtsvermogen kan herstellen bij muizen na een enkele behandeling. Hoewel verder werk nodig is om de veiligheid volledig te beoordelen, de targeting te verbeteren en de methode voor menselijk gebruik aan te passen, wijst dit platform op toekomstige eenmalige precisiegeneesmiddelen voor erfelijke retinale ziekten en mogelijk andere genetische aandoeningen waarbij zorgvuldige, gelokaliseerde DNA-herstel het verschil kan maken tussen blindheid en zicht.
Bronvermelding: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Trefwoorden: retinale gentherapie, CRISPR base-editing, liposomen, eiwitbezorging, erfelijke blindheid