Clear Sky Science · nl
Inzichten in de structuur en modulatie van menselijk TWIK-2
Waarom deze kleine poort in onze cellen ertoe doet
Diep in onze cellen regelen microscopische poorten van eiwit de stroom van geladen deeltjes, en daarmee hoe zenuwen vuren, hoe bloedvaten samentrekken en hoe ons immuunsysteem reageert. Eén van die poorten, TWIK-2 genaamd, wordt in verband gebracht met hoge druk in de longen en schadelijke ontsteking, maar tot nu toe wisten wetenschappers weinig over de bouw of de farmacologische beïnvloedbaarheid ervan. Deze studie onthult de gedetailleerde structuur van menselijk TWIK-2, beschrijft het elektrische gedrag en schetst hoe het kanaal gericht kan worden om nieuwe ontstekingsremmende geneesmiddelen te ontwikkelen.
Een kalm kanaal met grote gezondheidsgevolgen
TWIK-2 behoort tot een grote familie van ‘lek’-kaliumkanalen die helpen het rustpotentiaal van cellen vast te leggen door kaliumionen over het membraan te laten stromen. Terwijl andere familieleden, zoals TREK- en TASK-kanalen, intensief bestudeerd zijn en zijn gelinkt aan pijn en stemming, bleef TWIK-2 onopgemerkt omdat het moeilijk opneembaar is en slecht tot expressie komt in standaard labsystemen. Toch koppelen dier- en cellulaire studies TWIK-2 aan pulmonale hypertensie, acuut longoedeem, gehoorverlies en activatie van het NLRP3-inflammasoom, een immuunkomplex dat schadelijke ontsteking aandrijft bij sepsis en andere ziekten. Begrijpen hoe TWIK-2 werkt is dus essentieel voor zowel fundamentele biologie als het ontwerpen van gerichte therapieën.
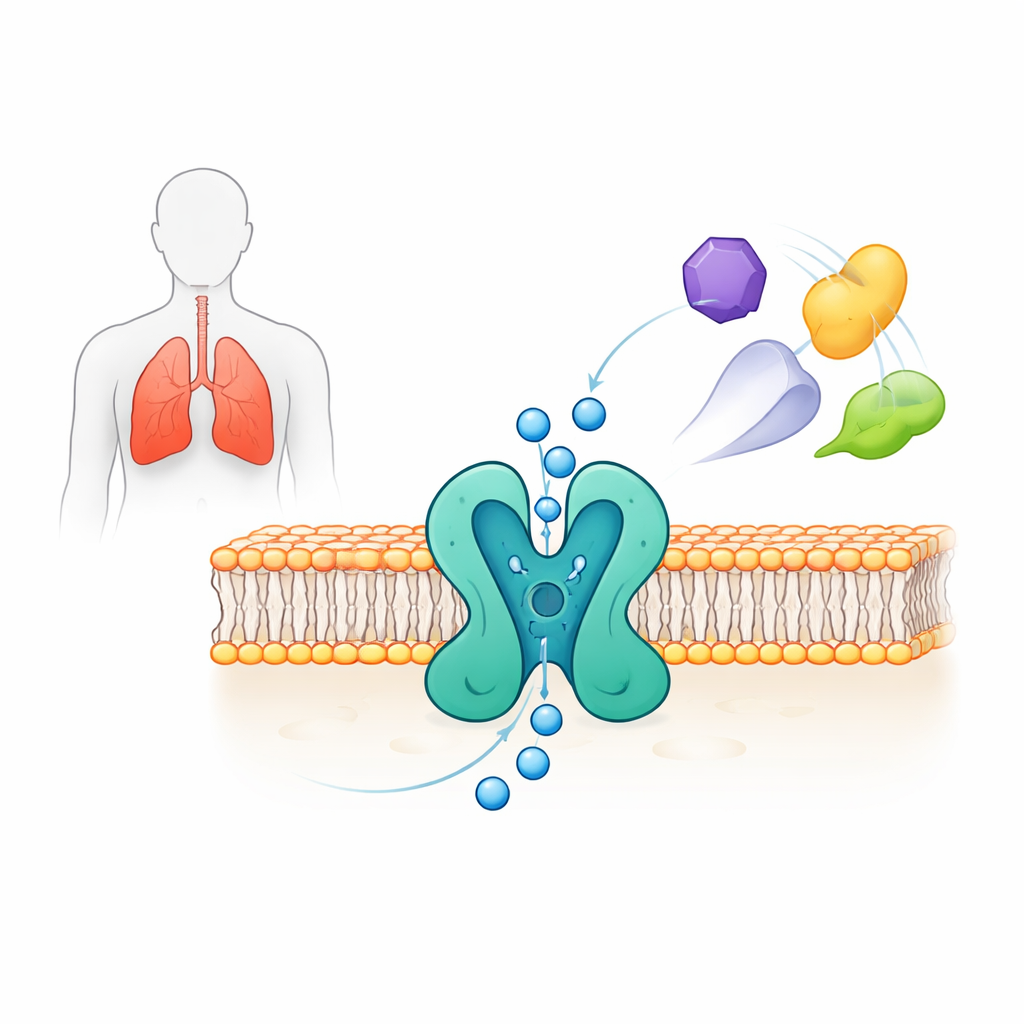
De poort zien op atomaire schaal
De onderzoekers brachten het volledige menselijke TWIK-2 tot expressie in menselijke cellijnen en gebruikten single-particle cryo-elektronenmicroscopie om de driedimensionale structuur te bepalen met een resolutie van ongeveer 3,7 Å. Het kanaal vormt een tweedelige assemblage die samen een centraal poreus kanaal voor kaliumionen creëert. Elke helft bevat vier membraanoverstekende segmenten en twee ‘pore helix’-structuren die een nauwe regio vormen, de selectiviteitsfilter, waar kalium van andere ionen wordt onderscheiden. Boven de pore creëren twee boogvormige ‘kap’-structuren twee afzonderlijke ingangspaden voor ionen van buiten de cel. De structuur toont ook subtiele asymmetrieën tussen de twee zijden van de pore die TWIK-2 een pseudo-vierdelige ordening geven, een kenmerk van deze kanaalfamilie.
Verborgen lipiden en een fijn afgestemd ionpad
Langs het iongeleidingspad brachten de onderzoekers in kaart hoe kaliumionen van het celinterieur bewegen, door een hydrofoob ‘manchet’, omhoog door de selectiviteitsfilter en naar buiten onder de kap. Het smalste punt is nog steeds groot genoeg zodat kalium in enkelvoudige volgorde kan passeren. Hoewel het eiwit zonder toegevoegde lipiden werd gezuiverd, toonden de cryo-EM-kaarten buisvormige dichtheden nabij het onderste deel van de pore en in zijzakken tussen helices. Deze vertegenwoordigen waarschijnlijk lipiden of detergentenstaarten die aan TWIK-2 vastzaten tijdens zuivering, wat suggereert dat natuurlijke membraanvetten zich in deze groeven kunnen nestelen en subtiel de vorm van aangrenzende helices verschuiven. Zulke verschuivingen, vooral in een helix genaamd M4 en in de lussen van de selectiviteitsfilter, zouden bepalen of het kanaal open, gesloten of ergens daartussenin is.
De poort onderzoeken met mutaties en blokkeringen
Om structuur aan functie te koppelen, gebruikten de wetenschappers een geautomatiseerd patch-clamp-systeem om stromen te meten van cellen die ofwel normaal TWIK-2 of versies met specifieke gewijzigde aminozuren uitdrukten. Ze vonden dat TWIK-2 sterk spanningsafhankelijk is maar, in tegenstelling tot de verwant TWIK-1, grotendeels ongevoelig voor veranderingen in extracellulaire zuurgraad. Mutaties van twee geconserveerde threonineresiduen aan de basis van de selectiviteitsfilter deden het kanaal sneller opengaan en meer stroom geleiden, wat suggereert dat deze plaatsen als scharnieren werken die de gesloten toestand stabiliseren. Wijzigingen bij de ingang en uitgang van de pore veranderden hoe snel het kanaal aan- en uitging, wat laat zien hoe strak het ionpad wordt gereguleerd. Het team testte daarna vier bekende kleine moleculen die verwante kanalen moduleren. Twee daarvan, ML365 en NPBA, blokkeerden TWIK-2 krachtig, terwijl de anderen geen effect hadden. Door te vergelijken hoe diverse mutaties de gevoeligheid voor drugs beïnvloedden, concluderen de auteurs dat deze verbindingen waarschijnlijk binden net onder de selectiviteitsfilter en in nabijgelegen holtes, en dat verschillende stoffen overlappende maar onderscheidende bindingswijzen gebruiken.
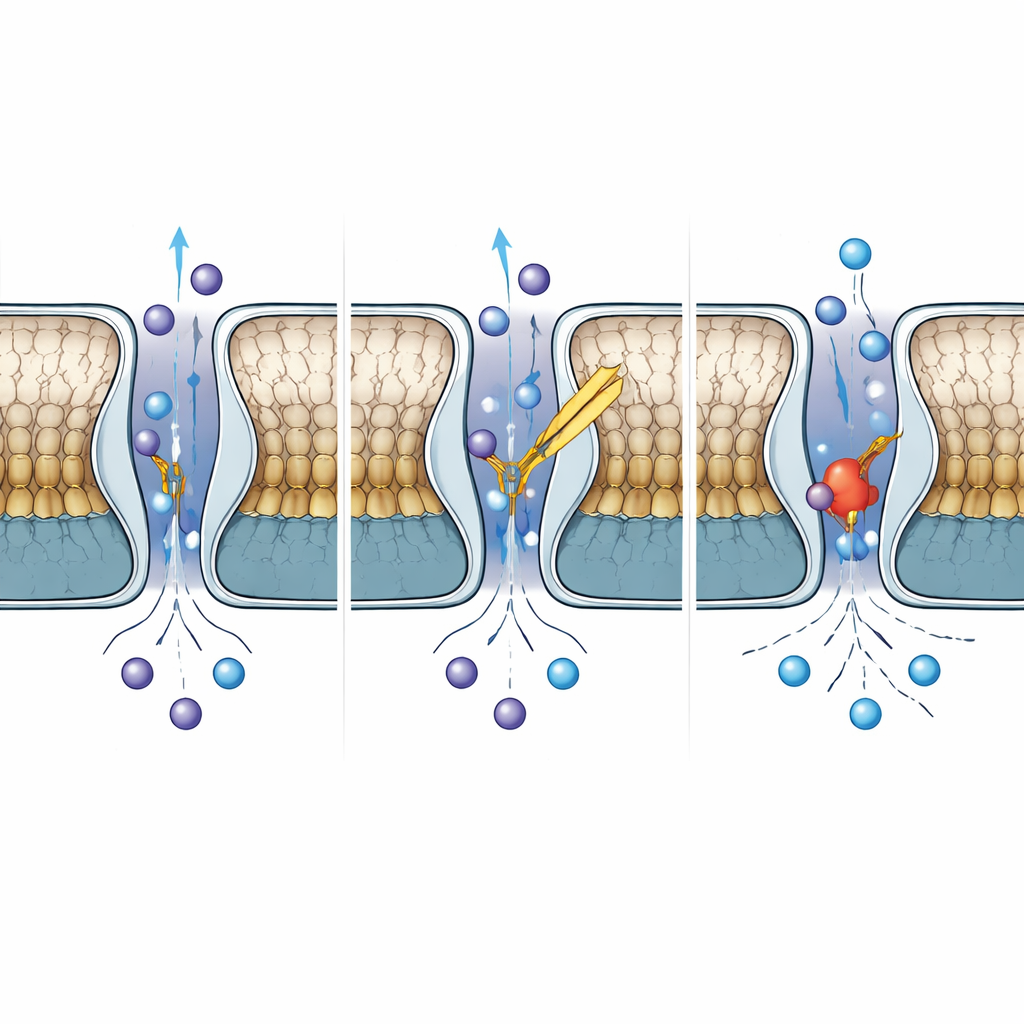
Hoe TWIK-2 verschilt van zijn naaste verwanten
Hoewel TWIK-2 meer dan de helft van zijn sequentie deelt met TWIK-1, wijkt hun gedrag op belangrijke punten af. Bij vergelijking van TWIK-2 met gepubliceerde TWIK-1-structuren bij neutrale en zure pH ontdekten de auteurs dat de kapregio van TWIK-2 lijkt op de zuur-geïnhibeerde vorm van TWIK-1, terwijl de selectiviteitsfilter toch is geordend als in de geleidelijke, open vorm. Een enkele histidine in TWIK-1, bekend als protonensensor die bij lage pH in de pore zwaait om ionstroom te blokkeren, is in TWIK-2 vervangen door een tyrosine. Zelfs wanneer het team een histidine terugbracht op die positie in TWIK-2, werd het kanaal niet pH-gevoelig, wat aantoont dat pH-regulatie in deze kanalen afhankelijk is van een breder netwerk van residuen en bewegingen, niet slechts één ‘schakel’-aminozuur.
Van structuur naar toekomstige therapieën
Alles bij elkaar biedt dit werk het eerste hoogresolutiebeeld van menselijk TWIK-2 en brengt het in kaart hoe specifieke structurele kenmerken de ionstroom, spanningsrespons en gevoeligheid voor kleine molecuulblokkers vormgeven. De ontdekking dat bestaande verbindingen TWIK-2 selectief kunnen remmen, gecombineerd met een robuust geautomatiseerd screeningsplatform, opent de deur naar grootschalige zoektochten naar veiligere en krachtigere geneesmiddelen. Omdat TWIK-2-activiteit in immuuncellen is gekoppeld aan ongecontroleerde ontsteking, vooral in de longen, zouden dergelijke middelen de basis kunnen vormen voor nieuwe ontstekingsremmende behandelingen die werken door deze kleine maar krachtige poort in het celmembraan subtiel ‘af te stemmen’.
Bronvermelding: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
Trefwoorden: TWIK-2 kaliumkanaal, two-pore-domain K2P kanalen, cryo-EM ionkanaalstructuur, modulatoren van kaliumkanalen, pulmonale ontsteking