Clear Sky Science · nl
Colonaal ruimtelijk single-cell proteomics en muismodellen koppelen mitochondriale disfunctie aan tekort aan dimerische IgA-secernerende plasmacellen bij ziekte van Crohn
Waarom darmantistoffen belangrijk zijn bij de ziekte van Crohn
De ziekte van Crohn staat vooral bekend om pijnlijke opvlammingen van darmontsteking, maar lang voordat symptomen serieus worden, kunnen subtiele veranderingen optreden in hoe het immuunsysteem de darm beschermt. Deze studie stelt een eenvoudige maar belangrijke vraag: produceren mensen met Crohn in remissie nog steeds het juiste type antistoffen om darmmicroben onder controle te houden? Door patiëntmonsters te combineren met hoogresolutie weefselprofilering, metabolische analyses en muismodellen, ontdekken de auteurs een verborgen zwakte in het antistoffenscherm van de darm die samenhangt met de cellulaire energievoorziening.
Een beschermende laag die tekortschiet
Onze darmen zijn afhankelijk van een speciaal antistoftype, secretorisch IgA, dat in het slijm van de darm wordt afgegeven. IgA, vooral in zijn “dubbele” vorm dimerisch IgA, bedekt bacteriën en andere microben en helpt ze op het oppervlak te houden in plaats van diep in het weefsel. In dit werk onderzochten de onderzoekers colonsbiopten, bloed en ontlasting van mensen met Crohn in remissie en van niet-geïnflammeerde controles. In het colonweefsel hadden Crohn-patiënten zelfs meer B-cellen en antistofproducerende cellen en hogere niveaus van IgA-gerelateerde genen en eiwitten. Wanneer het team echter IgA in de ontlasting mat, vonden ze het tegenovergestelde van wat je zou verwachten: secretorisch IgA in het darmlumen was significant verminderd. 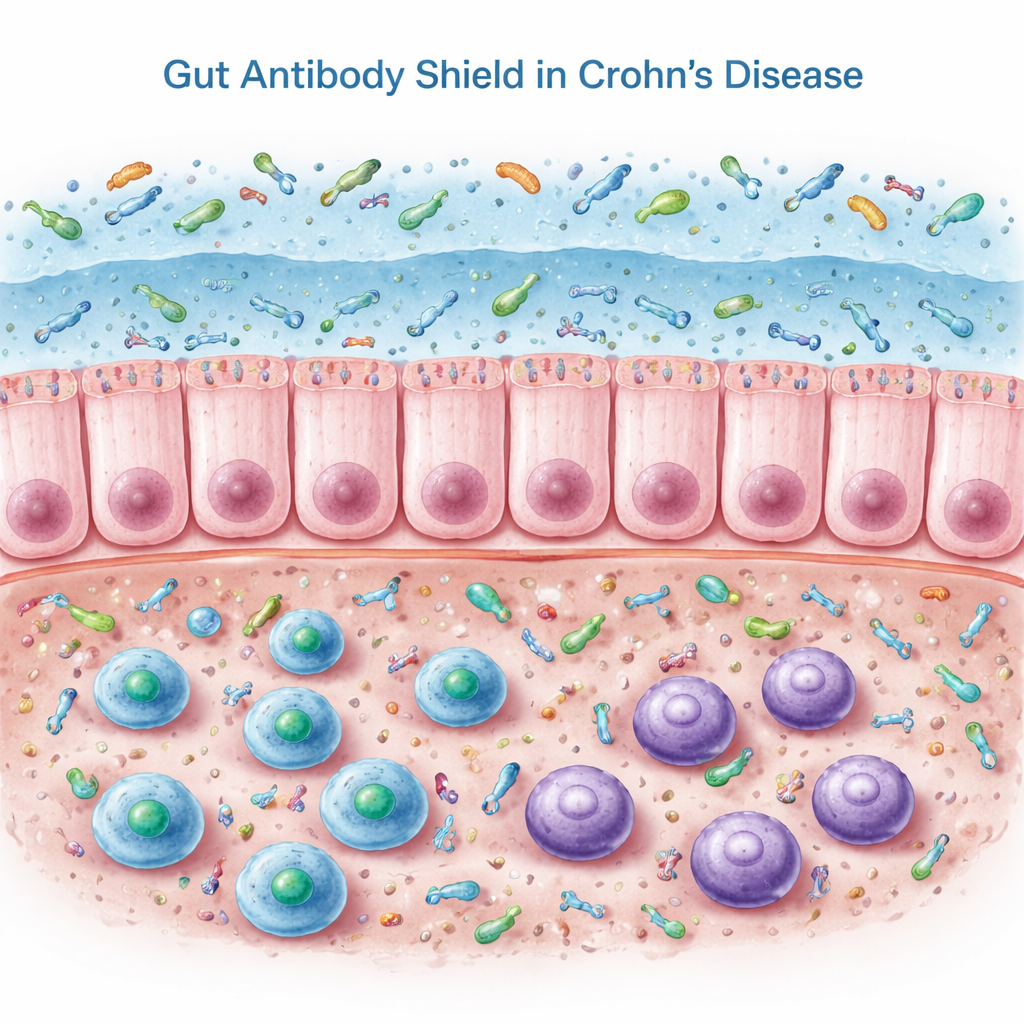
Halverwege vastgelopen: antistofproducerende cellen die niet volledig rijpen
De cellen die IgA afscheiden—plasmacellen—rijpen normaal gesproken via gedefinieerde stadia van actieve, kortlevende voorlopers naar langlevende specialisten die grote hoeveelheden dimerisch IgA produceren. Met ruimtelijke single-cell proteomics, waarmee vele eiwitten op individuele cellen in intact weefsel in kaart worden gebracht, konden de auteurs onrijpe en volledig gerijpte plasmacelsubsets in het colon onderscheiden. Bij Crohn-patiënten waren vroege plasmablasten en onrijpe plasmacellen uitgebreid aanwezig, terwijl de meest gerijpte plasmacellen verminderd waren. Biochemische analyses bevestigden dat de verhouding dimerisch tot monomerisch IgA lager was in Crohn-colons, en elke antistofproducerende cel scheidde gemiddeld minder dimerisch IgA uit. Toen het team omgeschakelde geheugen-B-cellen uit het colon isoleerde en ze in kweek naar plasmacellen liet differentiëren, faalden cellen van Crohn-patiënten in het opwaarderen van belangrijke rijpingsmarkers en produceerden ze minder totaal en dimerisch IgA, hoewel de IgG-productie grotendeels normaal bleef. Dit suggereert een intrinsieke blokkade in het rijpingsprogramma specifiek voor IgA-secernerende plasmacellen.
Energiefabriekjes onder druk
Om te begrijpen wat deze blokkade veroorzaakt, bekeken de onderzoekers de cellulaire stofwisseling. Ze vonden dat plasmacellen in Crohn-weefsel hogere niveaus van CD38 uitdrukten, een enzym aan het celoppervlak dat NAD+ verbruikt, een centrale brandstof voor mitochondriale energieproductie. Genen die betrokken zijn bij mitochondriale oxidatieve fosforylering—de belangrijkste manier waarop cellen ATP produceren uit voedingsstoffen—waren over het algemeen gedownreguleerd in colonaal weefsel van Crohn-patiënten, en plasmametabolietpatronen kwamen overeen met een verschuiving weg van efficiënte mitochondriale respiratie. In ex vivo-experimenten consumeerden uit Crohn-afgeleide plasmacellen weinig glucose, gaven minder lactaat af en toonden verminderde expressie van mitochondriale energiegenen, wat wijst op een metabolisch “kater” of verzwakte toestand. 
Aanwijzingen uit muismodellen en dieet
Muismodellen leverden aanvullende steun. Muizen met een gedefinieerde mitochondriale mutatie die het ATP-producerende enzymcomplex V aantastte, hadden minder rijpe plasmacellen in darmgeassocieerde lymfoïde weefsels, verminderde expressie van plasmacelmarkers in het colon en lagere niveaus van zowel monomerisch als dimerisch IgA in colonaal weefsel. Omgekeerd ontwikkelden gezonde muizen die een glucosevrij, eiwitrijk dieet kregen—een dieet dat mitochondriale activiteit in de darm verbetert—meer IgA-producerende cellen en hogere fecale IgA. Deze aanvullende experimenten koppelen de mitochondriale prestatie direct aan het vermogen van plasmacellen om te rijpen en een robuuste IgA-barrière in de darm te handhaven.
Wat dit betekent voor mensen met de ziekte van Crohn
Samengevat schetst de studie een beeld waarin de ziekte van Crohn, zelfs tijdens klinische remissie, geassocieerd is met een overvloed aan onrijpe B-lijncellen in het colon en een tekort aan volledig gerijpte, energie-intensieve plasmacellen die dimerisch IgA in het slijm afscheiden. De darm kan er rustig uitzien, maar het antistoffenscherm is dunner en minder effectief. Door dit defect te koppelen aan mitochondriale disfunctie—mogelijk deels aangedreven door verhoogde CD38-activiteit—suggereert het werk dat therapieën gericht op het herstellen van cellulaire energiestofwisseling of het verfijnen van CD38-signaleringsroutes kunnen helpen de mucosale IgA-barrière te herbouwen. Voor patiënten opent dit het vooruitzicht dat toekomstige behandelingen niet alleen ontsteking onderdrukken wanneer die optreedt, maar ook de frontlinie van antistofverdediging in de darm versterken om opvlammingen te voorkomen.
Bronvermelding: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
Trefwoorden: Ziekte van Crohn, darmantistoffen, IgA, mitochondriën, intestinale immuniteit