Clear Sky Science · nl
Tenascin C+ myofibroblasten verergeren vasculaire neointimale hyperplasie door de propagatie van zenuw-macrofagen interacties in muizen
Wanneer bloedvaten op de verkeerde manier genezen
Procedures die dichtgeslibde slagaders weer openen, zoals angioplastiek en bypassoperaties, redden talloze levens. Toch laten ze vaak een verborgen probleem achter: na verloop van tijd kan het behandelde vat van binnenuit steeds verder littekenweefsel vormen, opnieuw vernauwen en patiënten weer risico geven. Deze studie in muizen onthult een onverwacht drieledig gesprek tussen steuncellen, zenuwen en immuuncellen in de vaatwand dat dit schadelijke overgenezen aandrijft, en wijst een molecule genaamd tenascin C aan als een veelbelovend doelwit om die cyclus te doorbreken.
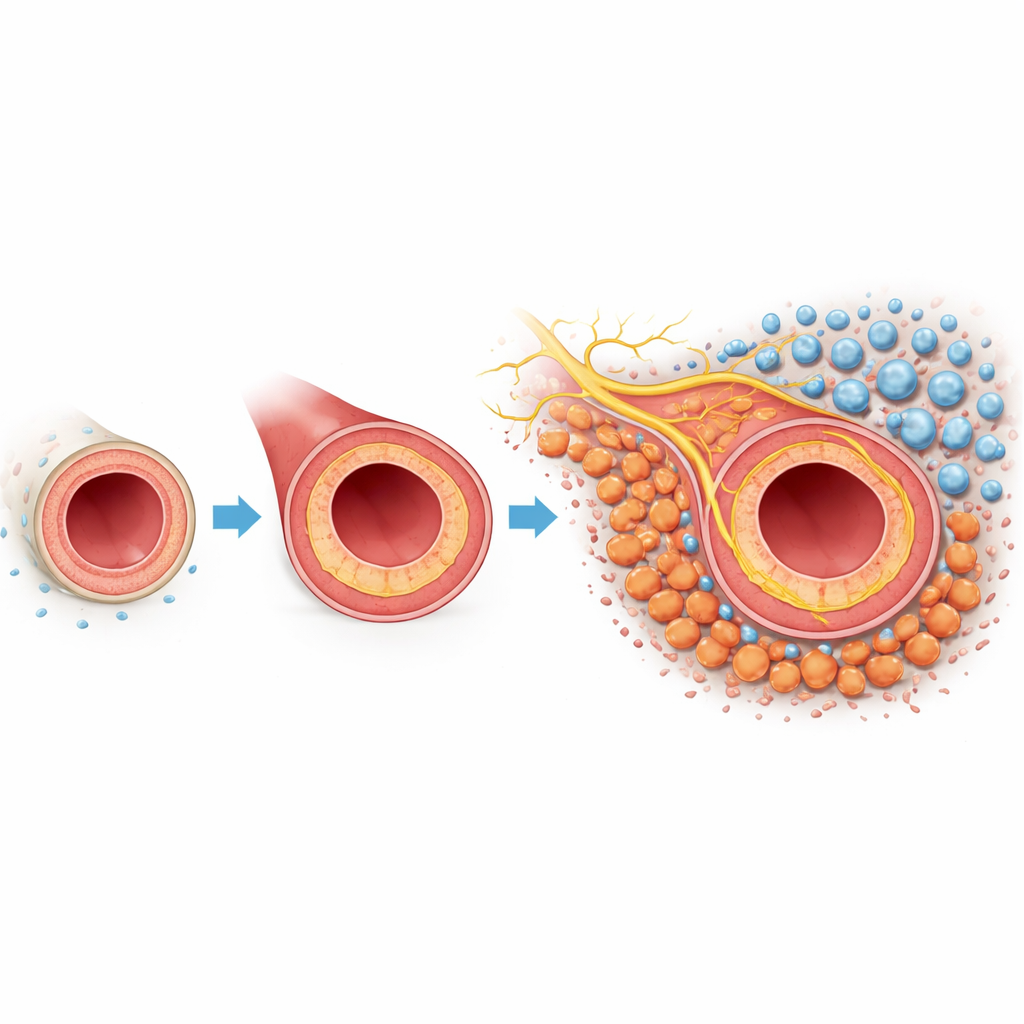
Een nadere blik op problematisch littekenvorming in slagaders
Wanneer een slagader beschadigd raakt of tijdens een operatie wordt gemanipuleerd, kan de binnenste bekleding te agressief teruggroeien. Deze naar binnen gerichte groei, neointimale hyperplasie genoemd, verdikt de vaatwand en verkleint het kanaal waarlangs het bloed stroomt. De buitenste laag van het vat, de adventitia, bevat fibroblasten—steuncellen die normaal de structuur van het vat in stand houden. In dit muismodel, waarin de halsslagader gedeeltelijk werd dichtgeknoopt om een verwonding na te bootsen, gebruikten de onderzoekers enkelcellig genetisch profielonderzoek en ruimtelijke kaartlegging om elk belangrijk celtype in kaart te brengen. Ze ontdekten dat fibroblasten bijzonder talrijk waren en hun gedrag na letsel drastisch veranderden, wat erop wijst dat deze cellen centrale spelers in de littekenreactie kunnen zijn.
De opkomst van littekenvormende tenascin C-cellen
Dieper in de fibroblastpopulatie ontdekte het team een onderscheidende subset die alleen na letsel verscheen. Deze cellen droegen kenmerken van myofibroblasten—hoge niveaus van het contractiele eiwit α-smooth muscle actin en een andere marker genaamd periostine—wat aangeeft dat ze waren overgeschakeld naar een littekenmakende modus. Cruciaal was dat deze subset ook grote hoeveelheden tenascin C produceerde, een matrixeiwit dat normaal schaars is in gezonde volwassen weefsels maar overvloedig aanwezig is bij ziekte en weefselherstel. Laboratoriumexperimenten toonden aan dat blootstelling van normale adventitiale fibroblasten aan transforming growth factor beta of extra tenascin C hen dreef om deze tenascin C–positieve myofibroblasten te worden. De cellen scheidden vervolgens nog meer tenascin C uit, waardoor een zichzelf versterkende lus ontstond via een specifiek oppervlakte-receptorpaar, integrine αvβ1, dat de populatie van littekenvormende cellen gestaag uitbreidde.
Zenuwen en immuuncellen trekken in de buurt
Het verhaal eindigde niet bij littekenvorming. Met behulp van 3D whole-mount beeldvorming en ruimtelijke transcriptomica observeerden de onderzoekers dat de tenascin C-rijke myofibroblasten clusteren nabij uitgroeiende zenuwvezels en immuuncellen die macrofagen worden genoemd in de buitenste vaatwand. Beschadigde slagaders vertoonden dichte, verwarde zintuiglijke zenuwen en meer synapsachtige structuren dan normaal, zowel in muizen als in menselijke arteriële monsters met neointimale hyperplasie. Macrofagen in deze regio’s droegen een inflammatoir signatuur en produceerden moleculen zoals IL-1β en TGF-β1 die het littekenproces verder kunnen aanwakkeren. Samen schetsten de gegevens een beeld van een gereorganiseerde microomgeving waarin littekenvormende cellen, zenuwen en macrofagen fysiek met elkaar vermengen en elkaar beïnvloeden.
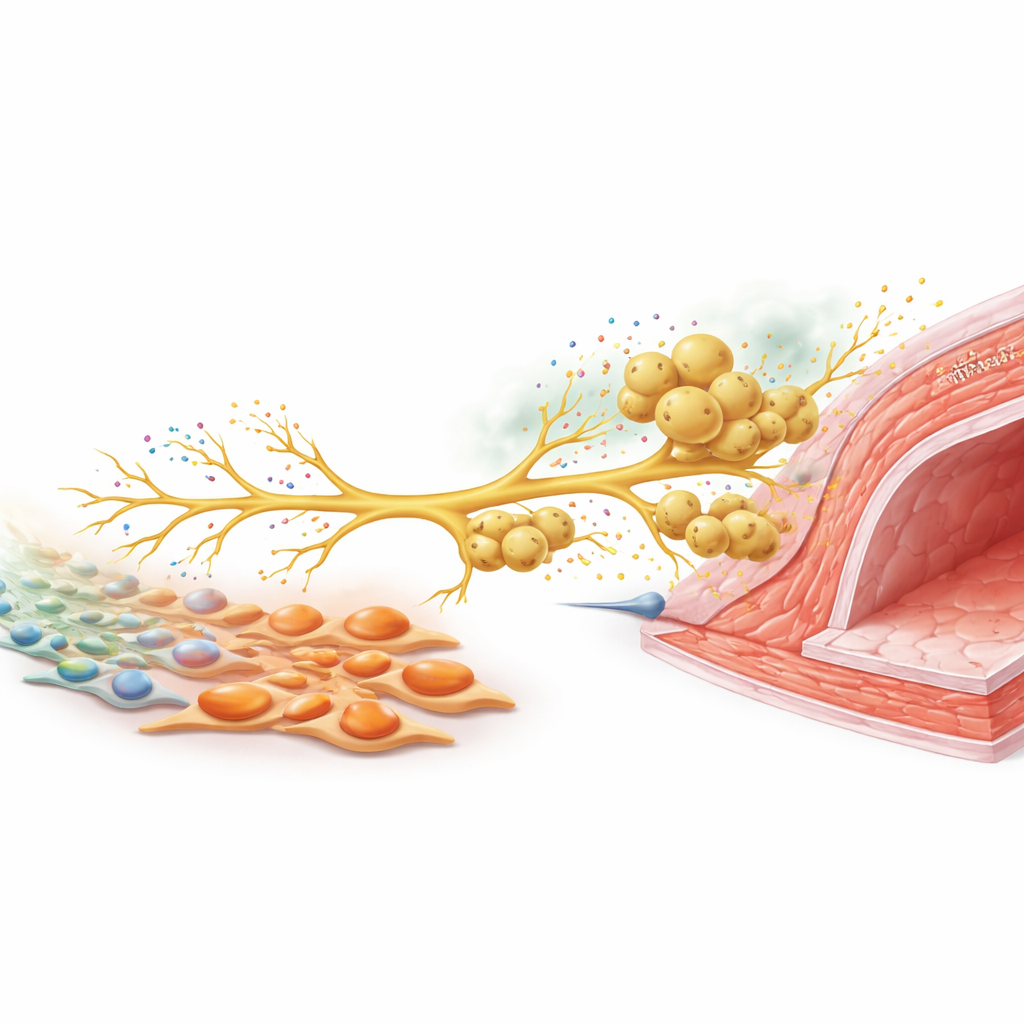
Een zenuwsignaal dat meer verdedigers oproept
Om te begrijpen hoe deze celtypen communiceren, concentreerde het team zich op zintuiglijke zenuwen die schadelijke prikkels waarnemen. In kweek bevorderden tenascin C-rijke myofibroblasten de uitgroei van zenuwvezels uit neuronen van dorsale wortelganglia. In beschadigde muizen verhoogden deze sensorische neuronen de productie van CCL2, een chemisch signaal dat bekend staat om het aantrekken van macrofagen. Wanneer neuronen en macrofagen samen werden gekweekt, migreerden macrofagen langs groeiende zenuwvezels, net zoals ze rond slagaders in vivo deden. Het stilleggen van CCL2 in neuronen verminderde de rekrutering van macrofagen sterk. In dieren verminderde het terugschakelen van zintuiglijke zenuwactiviteit met een toxine, of het selectief verwijderen van tenascin C alleen in fibroblasten, zowel de zenuwdichtheid, CCL2-niveaus, de ophoping van macrofagen en uiteindelijk de verdikking van de vaatwand. Het combineren van beide maatregelen gaf geen extra voordeel, wat suggereert dat ze werkzaam zijn binnen hetzelfde pad.
Waarom deze nieuwe route ertoe doet
Gezamenlijk onthullen de bevindingen een vicieuze cirkel: letsel zet fibroblasten aan om tenascin C-producerende myofibroblasten te worden; deze cellen herschikken de matrix en stimuleren zintuiglijke zenuwen; geactiveerde zenuwen geven CCL2 af, dat macrofagen aantrekt; en macrofagen scheiden inflammatoire en fibrotische factoren uit die het littekenproces verergeren en de slagader verder vernauwen. Door tenascin C en zijn downstream zenuw–macrofagen-as als centrale drijfveren van deze lus te identificeren, suggereert het werk dat behandelingen die deze molecule of zijn signaalpartners targeten, kunnen helpen om gerepareerde slagaders langer open te houden en patiënten duurzamere bescherming te bieden na cardiovasculaire ingrepen.
Bronvermelding: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
Trefwoorden: neointimale hyperplasie, tenascin C, vasculair remodelleren, zintuiglijke zenuwen, macrofagen ontsteking