Clear Sky Science · nl
Paclitaxel stimuleert de uitbreiding van TREM2+ macrofagen die ten grondslag ligt aan de mindere therapeutische werkzaamheid vergeleken met Nab-paclitaxel
Waarom deze studie belangrijk is
Veel vrouwen met borstkanker krijgen chemotherapie met taxanen, meestal paclitaxel of een nieuwere vorm gebonden aan kleine albumine-deeltjes, bekend als nab‑paclitaxel. Artsen vermoedden al langer dat het nieuwere middel vaak beter werkt, maar de redenen waren onduidelijk. Deze studie onderzoekt patiëntgegevens en dierexperimenten om te laten zien dat standaard paclitaxel onbedoeld kan helpen bij het verspreiden van kanker naar de longen door het immuunsysteem te herschikken, en wijst tevens op een manier om dit schadelijke neveneffect te blokkeren.
Twee vergelijkbare middelen, twee verschillende uitkomsten
De onderzoekers vergeleken eerst de prestaties van paclitaxel en nab‑paclitaxel in de praktijk bij duizenden vrouwen met borstkanker. Door resultaten van 17 klinische studies met in totaal 6.486 patiënten samen te voegen, vonden zij dat nab‑paclitaxel leidde tot hogere tumorkrimpingspercentages en vaker tot volledige verdwijning van kanker in de borst en nabijgelegen lymfeklieren vóór de operatie. Dit voordeel was vooral groot bij patiënten die werden behandeld nadat eerdere therapieën hadden gefaald. Beide middelen werden echter in vergelijkbare doses toegediend en zijn ontworpen om delende kankercellen op ongeveer dezelfde manier aan te vallen, wat suggereert dat er iets anders speelt dan directe tumorceldood.
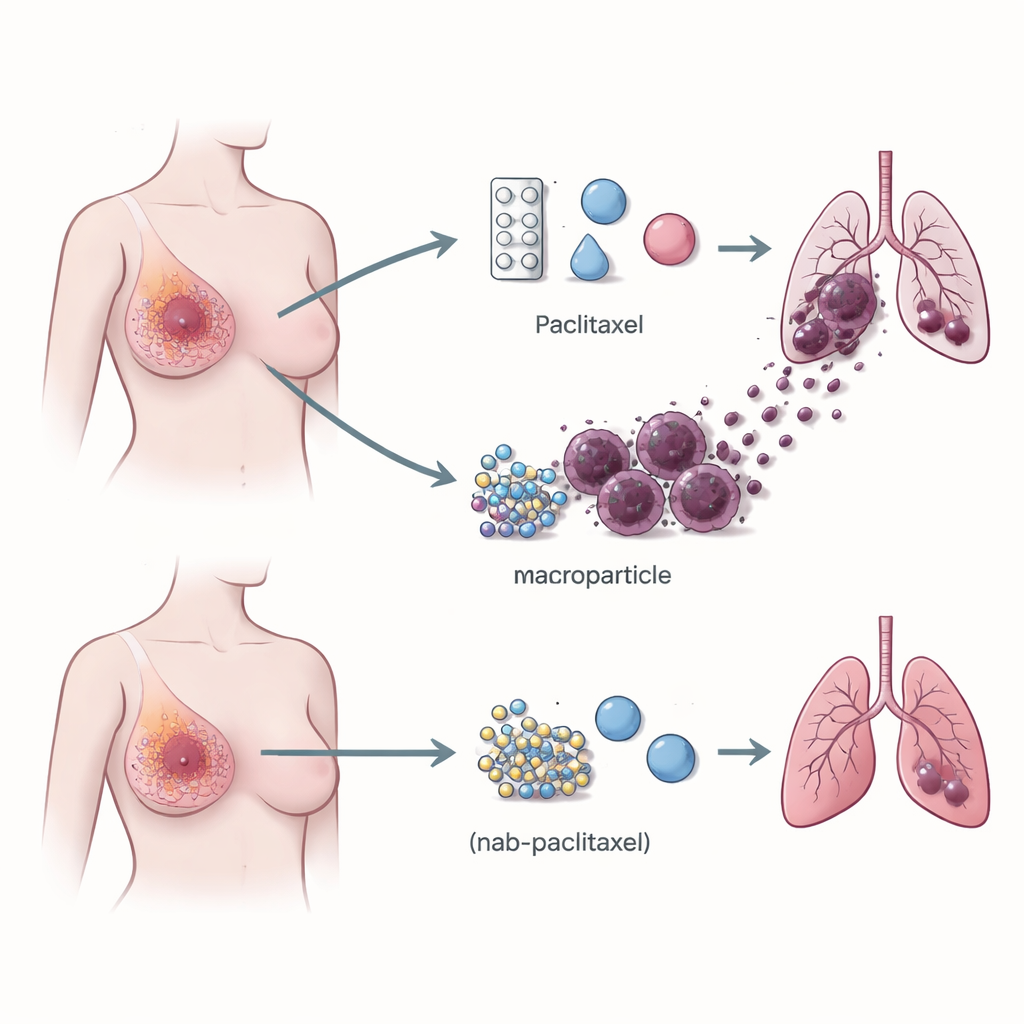
Immuuncellen die kanker helpen reizen
De aandacht verschoof naar de immuunomgeving van de tumor — de samenstelling van witte bloedcellen die kanker kunnen bestrijden of, verrassend vaak, juist kunnen helpen groeien. Met single‑cell RNA‑sequencing, een techniek die de genactiviteit in duizenden individuele cellen uitleest, vergeleek het team tumoren van patiënten behandeld met paclitaxel versus nab‑paclitaxel. Ze ontdekten dat tumoren van paclitaxelbehandelde patiënten veel meer macrofagen bevatten met een receptor genaamd TREM2 op hun oppervlak. Deze TREM2‑positieve macrofagen waren verrijkt aan de randen van tumoren en waren veel talrijker bij patiënten die later longmetastasen ontwikkelden dan bij degenen wiens kanker op zijn plaats bleef. Dit patroon bleek ook in grotere patiëntengroepen en in muismodellen, wat een sterke link legt tussen dit type macrofaag en het risico op uitzaaiing.
Als behandeling tumoren verkleint maar verspreiding stimuleert
Bij muizen met borsttumoren deed paclitaxel wat ervan werd verwacht: het vertraagde of verkleinde primaire tumoren. Tegelijkertijd nam het aantal kankerneerslagen in de longen toe en steeg het aantal TREM2‑positieve macrofagen in tumoren en in de bloedbaan. Nab‑paclitaxel daarentegen verminderde de tumoromvang zonder longmetastasen te stimuleren of deze macrofagen uit te breiden, hoewel het net zo effectief was in het krimpen van de hoofdtumor. Wanneer het TREM2‑gen bij muizen werd verwijderd, of wanneer TREM2 werd verminderd met antisense‑oligonucleotiden (korte DNA‑stukjes die specifieke genen laten zwijgen), bleef paclitaxel primaire tumoren verkleinen maar verloor het grotendeels zijn vermogen om longuitzaaiingen te bevorderen. Dit toont aan dat TREM2‑dragende macrofagen geen bijstanders zijn; ze zijn noodzakelijke partners in paclitaxel‑gedreven metastase.
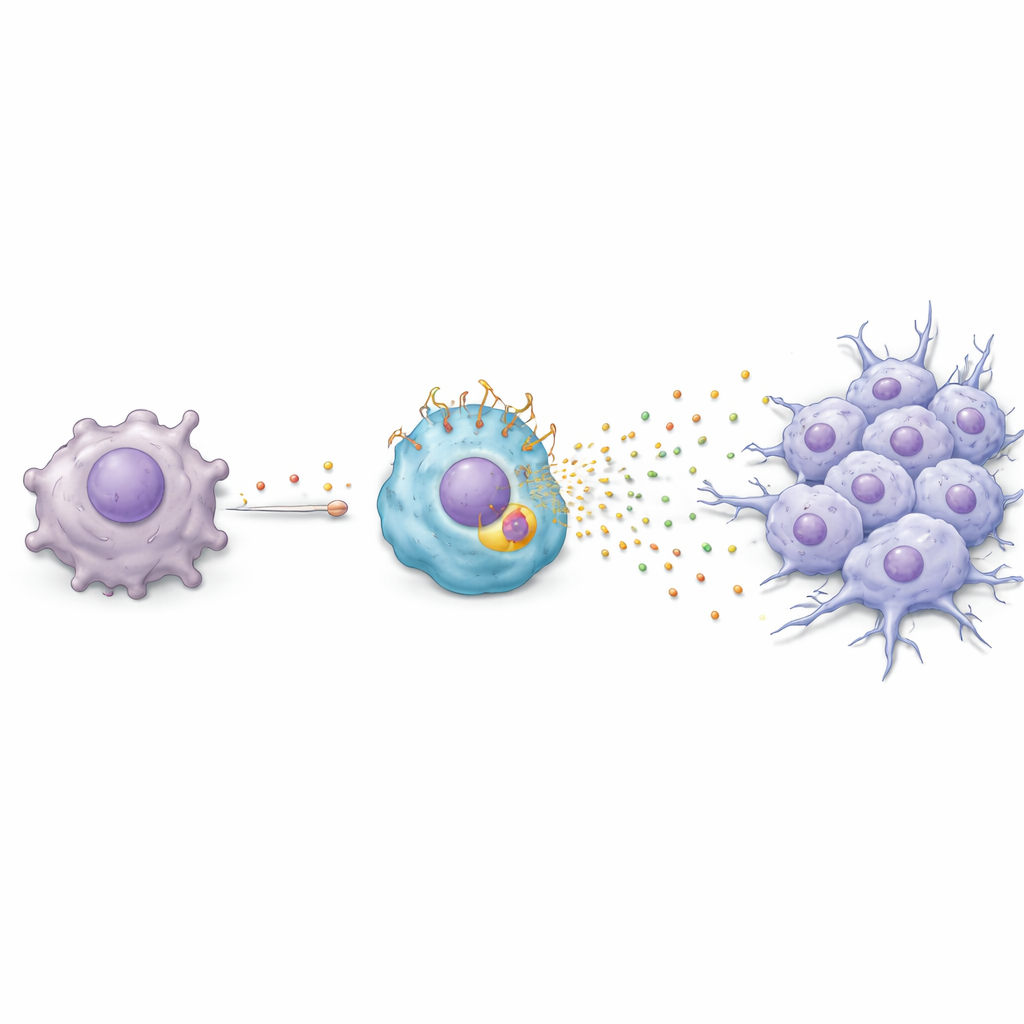
Een chemische kettingreactie van tumor naar immuuncel
Het team vroeg vervolgens hoe paclitaxel macrofagen in deze schadelijke, TREM2‑rijke toestand brengt. Ze ontdekten een kettingreactie: paclitaxel zet kankercellen aan tot activatie van een stresresponsgen genaamd ATF3, dat op zijn beurt de productie van een groeifactor genaamd FGF2 verhoogt. Kankercellen geven vervolgens FGF2 af aan hun omgeving, waar het inwerkt op nabije macrofagen. In die macrofagen activeert FGF2 een andere regulator, EGR1, die TREM2‑niveaus verhoogt. Zodra TREM2 hoog is, beginnen macrofagen een cocktail van eiwitten vrij te geven — waaronder Serpin E1, HGF, CCL3 en CXCL2 — die kankercellen aansporen om in een mobielere, invasieve vorm te gaan, bekend als epitheliaal‑mesenchymale transitie. In laboratoriumkweek en bij muizen maakte deze chemische wisselwerking tumorcellen vatbaarder om te migreren en binnendringen, cruciale stappen op weg naar metastase.
Van tweesnijdend zwaard naar veiliger hulpmiddel
In eenvoudige bewoordingen is de kernboodschap dat paclitaxel als een tweesnijdend zwaard kan werken: terwijl het tumoren aanvalt, instrueert het ook bepaalde immuuncellen om de kanker te helpen ontsnappen naar verre organen. Nab‑paclitaxel lijkt deze specifieke immuunmissturing te vermijden. Het bemoedigende nieuws is dat het blokkeren van TREM2 — of delen van de FGF2–EGR1–TREM2‑signaleringsketen — in diermodellen de tumorkrimpende voordelen van paclitaxel kan scheiden van de metastasebevorderende risico’s. Als vergelijkbare strategieën veilig en effectief blijken bij mensen, zouden artsen een vertrouwd, breed beschikbaar chemotherapeuticum kunnen blijven gebruiken terwijl ze het risico op kankerverspreiding beperken, wat kan leiden tot betere langetermijnresultaten voor patiënten.
Bronvermelding: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Trefwoorden: borstkanker, paclitaxel, tumormicro-omgeving, macrofagen, metastase