Clear Sky Science · nl
Betrouwbare herbestemming van het antilichaam‑interactoom binnen de cel
Antilichamen ombouwen tot kleine gereedschappen binnen onze cellen
Antilichamen staan bekend als de precisiewapens van het bloed, gericht op virussen en andere bedreigingen. Maar in veel ziekten — waaronder Alzheimer, Parkinson en sommige vormen van kanker — speelt het belangrijkste werk zich binnen cellen af, waar gewone antilichamen zelden komen of goed functioneren. Deze studie laat zien hoe bestaande antilichamen systematisch kunnen worden herbouwd tot kleinere “intrabodys” die betrouwbaar werken in levende menselijke cellen. Dat opent de deur naar nieuwe diagnostiek, onderzoeksgereedschappen en mogelijk toekomstige therapieën die direct ingrijpen op de kern van ziekteprocessen.
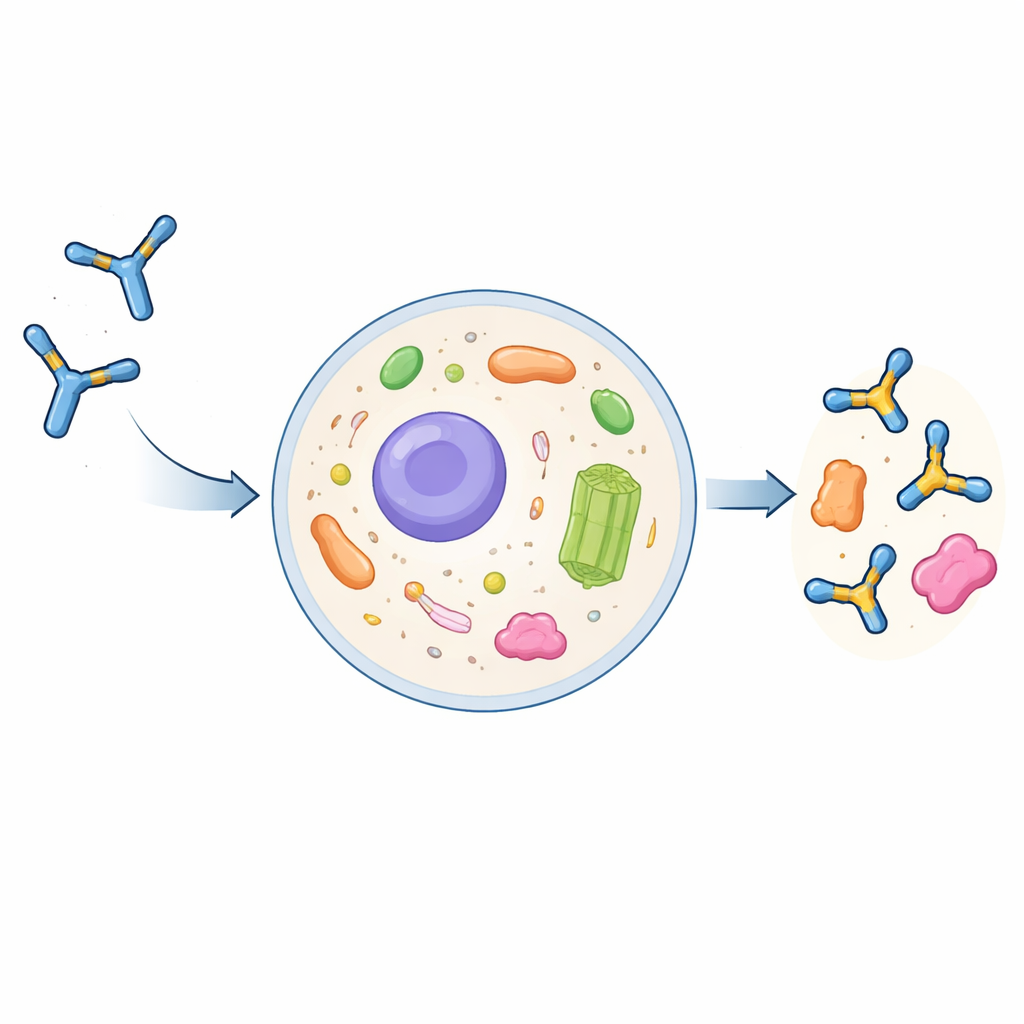
Waarom gewone antilichamen moeite hebben binnen cellen
Volledige antilichamen zijn grote, Y‑vormige eiwitten die geëvolueerd zijn om buiten cellen te werken. Ze worden gemonteerd en chemisch aangepast in het secretie‑pad van de cel en vervolgens vrijgegeven in de bloedbaan. Als ze door cellen worden opgenomen, belanden ze meestal in afbraakcompartimenten in plaats van in het vochtige binnenste van de cel, het cytoplasma. Wetenschappers kunnen antilichamen inkorten tot hun essentiële herkenningsdelen, de zogeheten single‑chain variable fragments (scFv), en deze binnen de cel tot intrabodys laten produceren. Deze intrabodys klonteren echter vaak samen, worden onoplosbaar en verliezen hun bindingsvermogen. Tot nu toe bestond er geen algemene, betrouwbare aanpak om een conventioneel antilichaam om te zetten in een goedgedragende intrabody.
De ontwerpregels voor oplosbare intrabodys vinden
De onderzoekers begonnen met het meten van hoe goed 45 verschillende intrabodys opgelost bleven wanneer ze in menselijke cellen werden geproduceerd. Ze vergeleken systematisch veel eiwiteigenschappen — zoals totale hydrofobiciteit, voorspelde structuurkwaliteit en de eigenschappen van de bindingslussen — om te zien welke factoren het best verklaarden of een intrabody oplosbaar bleef. Één eenvoudige factor stak eruit: de totale elektrische lading bij nabij‑fysiologische pH. Intrabodys met een sterk negatieve nettolading bleken veel vaker oplosbaar te blijven, terwijl neutrale of positief geladen varianten geneigd waren te aggregeren. Andere geavanceerde voorspellers, waaronder structuurvertrouwensscores van het AlphaFold‑systeem, correleerden niet met oplosbaarheid. Dit stelde het team in staat een praktisch, op lading gebaseerd model te bouwen dat kan inschatten welk deel van een intrabody in de oplosbare fractie van een cel‑extract zal zitten.
Linkers en domeinen herontwerpen voor beter gedrag
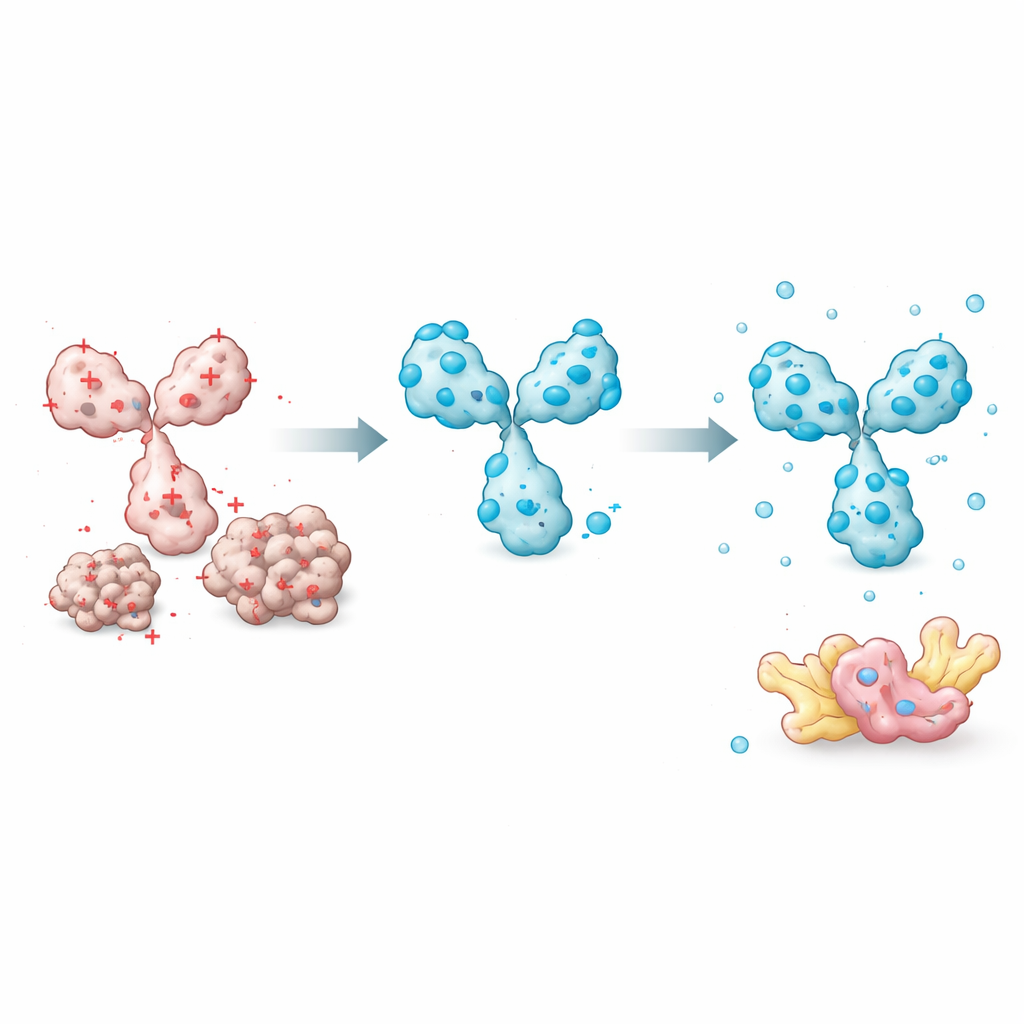
Met deze inzichten richtte het team zich op kenmerken die ze gemakkelijk konden aanpassen zonder te verstoren hoe een intrabody zijn doel herkent. Een sleutelelement is de korte peptide‑“linker” die de twee variabele domeinen verbindt. De meeste bestaande ontwerpen gebruiken neutrale linkers die de lading niet veranderen. Door op deze posities negatief geladen aminozuren in te brengen, konden de onderzoekers de totale lading van de intrabody verlagen, wat de oplosbaarheid drastisch verbeterde terwijl de doelbinding behouden bleef. Ze ontdekten ook dat de volgorde van de variabele domeinen (of het zware deel of het lichte deel eerst komt) en specifieke frameworkposities buiten de bindingslussen invloed hebben op hoe makkelijk het eiwit vouwt en oplosbaar blijft. Het kiezen van een domeinvolgorde die kwetsbare regio’s beschermt en het invoeren van zorgvuldig geplaatste lading‑wisselmutaties verhoogde de prestaties verder.
Artificiële intelligentie gebruiken om intrabodys op schaal te bouwen
Om verder te komen dan individuele trial‑and‑error combinerden de auteurs hun eenvoudige ladingsregels met geavanceerde eiwitontwerpsoftware op basis van deep learning. Vertrekkend van bekende antilichaam‑backbones gebruikten ze een “inverse folding”‑benadering om nieuwe sequenties voor te stellen die nog steeds de gewenste vorm aannemen, maar oppervlakteeigenschappen — vooral ladingspatronen — hebben die stabiliteit en oplosbaarheid bevorderen. Ze beperkten wijzigingen in de cruciale bindingslussen om herkenning te behouden, terwijl het algoritme omliggende oppervlakken mocht herontwerpen. Tests toonden aan dat veel van deze AI‑geleide intrabodys niet alleen zeer oplosbaar waren maar ook thermisch stabieler dan door mensen ontworpen varianten, en dat ze het vermogen behielden om aan ziektegerelateerde doelen te binden, zoals misgevouwen SOD1, p53, α‑synucleïne en andere eiwitten die met neurodegeneratie zijn verbonden.
Een bibliotheek bouwen van eiwitvangers voor binnenin de cel
Door deze regels en tools op grote schaal toe te passen, formatteerde het team computationeel 672 antilichamen om tot intrabodys die naar verwachting goed binnen cellen werken. Deze ontworpen moleculen bestrijken meer dan 60 verschillende intracellulaire doelen, inclusief eiwitten die betrokken zijn bij Alzheimer, Parkinson en Huntington, evenals kankergerelateerde factoren en post‑translationele modificaties zoals fosforylering en acetylatie. In experimenten konden geselecteerde intrabodys succesvolle specifieke ziekte‑geassocieerde eiwitvormen uitvissen, zoals mutant SOD1 of bepaalde conformaties van α‑synucleïne, terwijl normale versies werden genegeerd. Alle sequenties zijn openlijk vrijgegeven en de auteurs bieden een webtool waarmee anderen de oplosbaarheid van intrabodys vanuit sequentie kunnen schatten met hetzelfde op lading gebaseerde model.
Wat dit betekent voor toekomstige geneesmiddelen en onderzoek
Praktisch gezien verandert dit werk de enorme bestaande collectie antilichamen — velen al bestudeerd in klinische settings — in een toolkit die betrouwbaar kan worden aangepast voor gebruik binnen cellen. Door een eenvoudige set ontwerprichtlijnen te volgen, kunnen onderzoekers nu intrabodys maken die waarschijnlijk bij de eerste poging werken, wat tijd en kosten bespaart. Voor een leek is de kernboodschap dat wetenschappers een eenvoudige manier hebben gevonden om onze beste proteïne‑detectoren te “herbekabelen” zodat ze functioneren in het drukke binnenste van levende cellen, waar veel ziekten beginnen. Dit kan de ontwikkeling versnellen van nieuwe methoden om aandoeningen te volgen, te bestuderen en uiteindelijk te behandelen die worden veroorzaakt door misgevouwen of slecht functionerende eiwitten.
Bronvermelding: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
Trefwoorden: intrabodys, antilichaam‑engineering, eiwitoplosbaarheid, neurodegeneratieve ziekte, kunstmatige intelligentie in de biologie