Clear Sky Science · nl
Het reguleren van interfaciale waterlagen voor zuurstofoverdracht naar benzylic C(sp3)–H-bindingen via Ni-geactiveerde wolfraam–zuurstof covalentie
Water en olie omzetten in nuttige chemicaliën
Scheikundigen zoeken al lang naar schonere manieren om eenvoudige olie-afgeleide moleculen om te zetten in waardevollere bouwstenen voor kunststoffen, geneesmiddelen en alledaagse producten. Deze studie laat zien hoe het zorgvuldig "afstemmen" van de dunne waterlaag die een elektrode raakt, ervoor kan zorgen dat gewoon water zuurstof levert aan hardnekkige koolwaterstofmoleculen, waardoor afval en energieverbruik afnemen.
Waarom zuurstof uit water belangrijk is
Veel industriële chemicaliën worden gemaakt door zuurstof aan koolwaterstoffen te koppelen—moleculen die voornamelijk uit koolstof en waterstof bestaan. Vandaag de dag gebeurt dat vaak met sterke oxidatiemiddelen en hoge temperaturen, wat veel energie verbruikt en broeikasgassen produceert. Water is een goedkope, veilige en overvloedige zuurstofbron, maar het overtuigen van water om die zuurstof direct te delen met robuuste C–H-bindingen vereist doorgaans zeer hoge voltages. Onder zulke zware omstandigheden gaat een groot deel van de elektriciteit verloren aan het splitsen van water in zuurstofgas in plaats van aan het maken van nuttige producten.
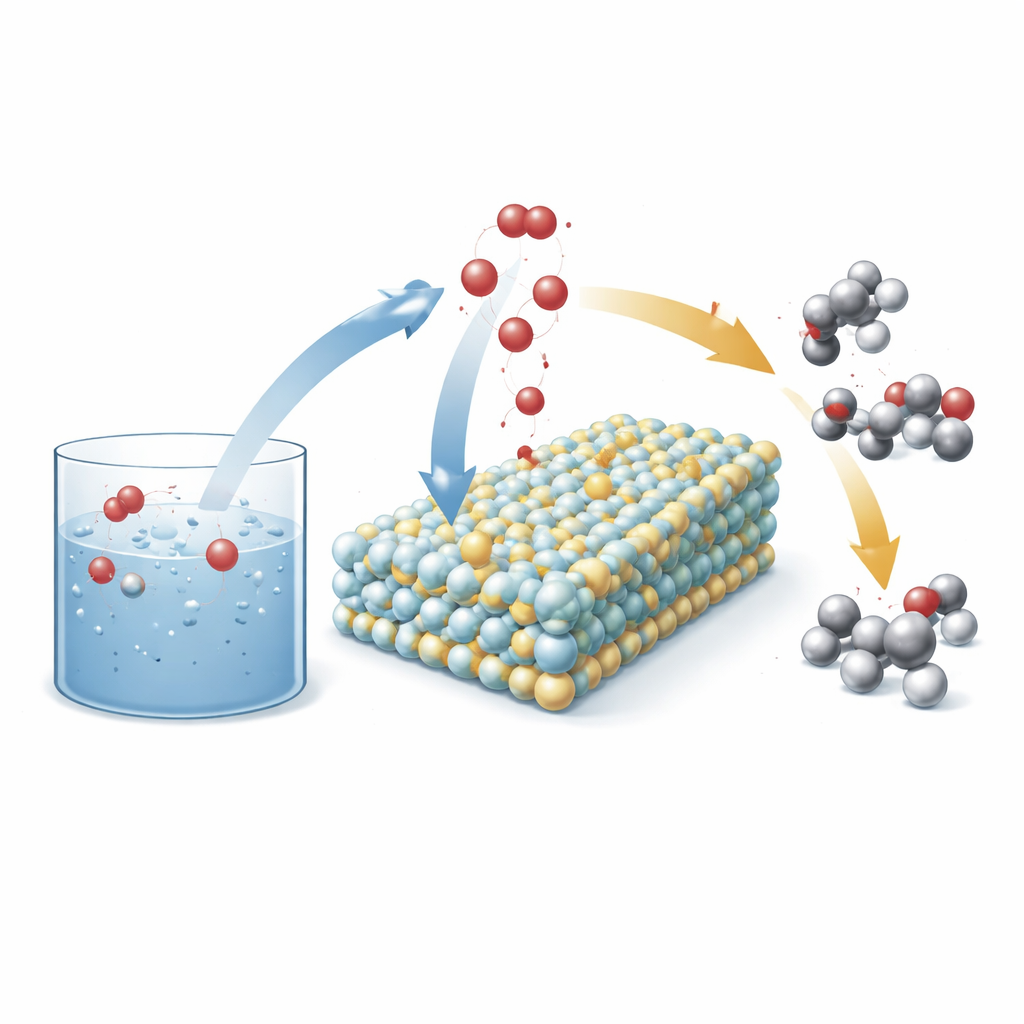
Een slimme elektrode die water herschikt
De onderzoekers ontwierpen een nieuw type anode (de positieve elektrode in een elektrochemische cel) opgebouwd uit kleine deeltjes wolfraamcarbide die tijdens gebruik transformeren naar een amorfe wolfraam–zuurstoffase. In dit netwerk verspreiden ze individuele nikkelatomen. Onder reactief omstandigheden migreert zuurstof uit water in het vaste materiaal en verandert het in een nikkel-geactiveerd wolfraamoxide-oppervlak met veel blootgestelde reactieve sites. Dit herbouwde oppervlak fungeert vervolgens als een platform waar water- en koolwaterstofmoleculen elkaar ontmoeten en zuurstof gecontroleerd uitwisselen, waarbij waardevolle producten zoals alcoholen en ketonen worden bevoordeeld boven overgeoxideerde zuren en andere bijproducten.
De waterkooi aan het oppervlak losser maken
Een belangrijke ontdekking is dat nikkelatomen subtiel verstoring veroorzaken in de manier waarop watermoleculen zich tegen de elektrode schikken. Normaal vormt water bij een geladen oppervlak een dicht web van waterstofbruggen, als een strak net dat beweging vertraagt. Computersimulaties en gevoelige infraroodmetingen tonen aan dat nabij nikkelbesmette regio’s dit netwerk losser wordt, met minder waterstofbruggen en meer “vrije” watermoleculen. Dit opent kanalen waardoor water gemakkelijker naar de reactieve wolfraam–zuurstofsites kan diffunderen. Daardoor kunnen zuurstofdragende fragmenten uit water het oppervlak sneller en vaker bereiken, en zo de reactie voeden in plaats van te ontsnappen als zuurstofgas.
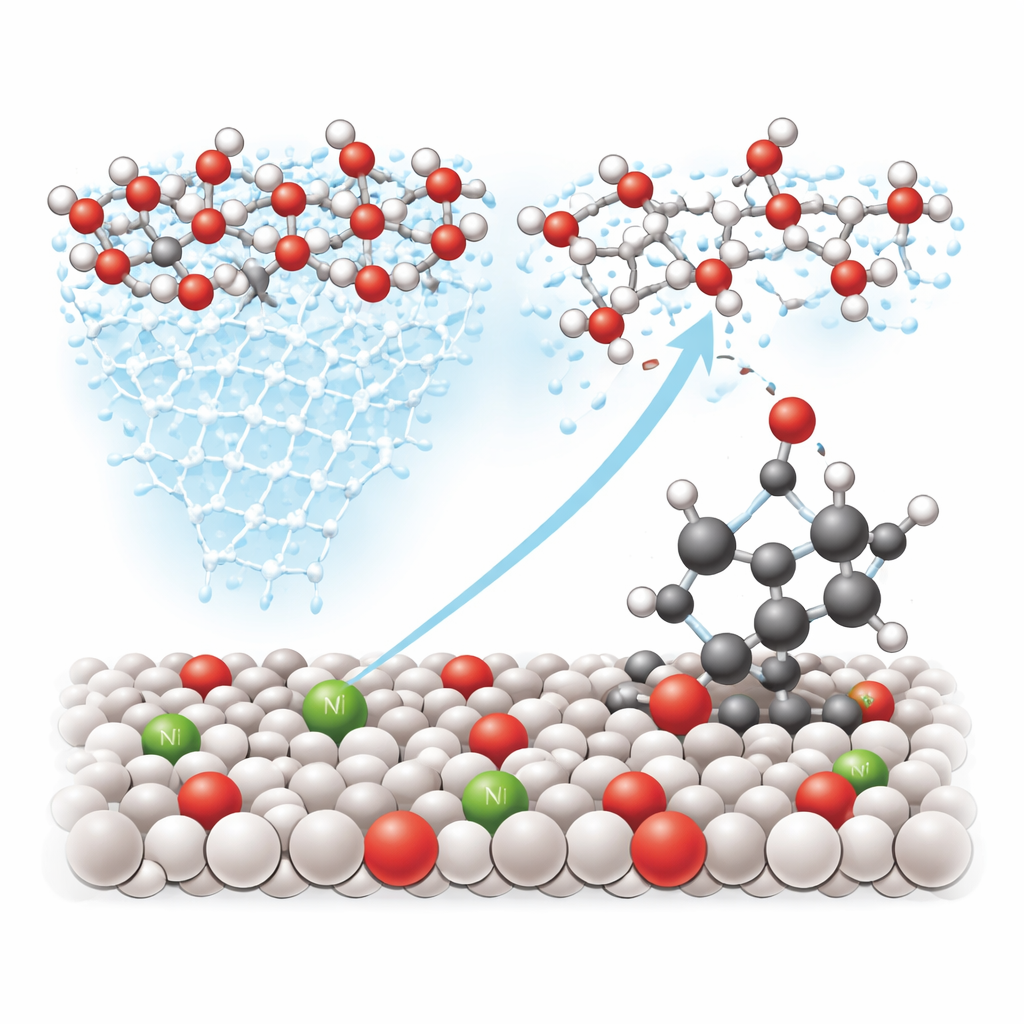
Zuurstof naar de juiste bindingen leiden
Buiten het verbeteren van het verkeer aan het oppervlak stemt nikkel ook de elektronische structuur van aangrenzende wolfraamatomen af, waardoor bepaalde plekken bijzonder geschikt worden om water te grijpen en te activeren. De experimenten van het team met isotopen—speciale versies van zuurstof en waterstof die te volgen zijn—tonen aan dat de actieve zuurstof afkomstig is van vers gesplitst water en niet van het bulkoxide zelf. Spectroscopische "momentopnamen" leggen een kortstondige brug vast tussen wolfraam, zuurstof en de benzyliche koolstof op moleculen zoals ethylbenzeen. Theoretische berekeningen bevestigen dat het op het nikkel-gemodificeerde oppervlak gemakkelijker is voor een zuurstofatoom om deze C–H-plaats aan te vallen dan de gebruikelijke watersplitsingsroute te volgen die zuurstofgas produceert, waardoor de reactie effectief wordt gestuurd naar nuttige geoxideerde producten.
Efficiënt, selectief en duurzaam gebouwd
In tests zet de nikkel-geactiveerde elektrode een reeks benzyliche C–H-bindingen om in alcoholen en ketonen met Faradaïsche rendementen—hoeveel van de elektrische lading in de gewenste chemie vloeit—typisch boven 50%, en in geoptimaliseerde gevallen meer dan 56%. Het systeem draait vele cycli zonder activiteit te verliezen, terwijl het zijn nikkel–wolfraamstructuur behoudt. Omdat het water als enige zuurstofbron gebruikt en toegevoegde chemische oxidanten vermijdt, biedt het concurrerende energie-efficiëntie en lagere materiaalkosten vergeleken met andere geavanceerde methoden. Hoewel de huidige toepassing gericht is op benzyliche sites, wijst het onderliggende principe—het gebruik van atomische toevoegingen om interfaciaal water te hervormen en reactiepadwijzen te herleiden—op een bredere gereedschapskist voor groenere, elektrisch aangedreven oxidatie van anders inert C–H-bindingen.
Wat dit betekent voor schonere chemie
Dit werk laat zien dat kleine veranderingen op atomair niveau grote effecten kunnen hebben op hoe water zich gedraagt bij een elektrode en waar zijn zuurstof terechtkomt. Door nikkelatomen te gebruiken om zowel de structuur van interfaciaal water losser te maken als reactieve sites fijn af te stemmen, zetten de auteurs water in als een efficiënte zuurstofdonor voor moeilijk te activeren koolwaterstofbindingen, terwijl ongewenste vorming van zuurstofgas wordt onderdrukt. Op de lange termijn zouden strategieën als deze kunnen helpen de oxidatiechemie in de chemische industrie te herontwerpen, waardoor die energiezuiniger en klimaatvriendelijker wordt door elektriciteit en water te gebruiken in plaats van harde oxidanten en fossiel-afgeleide reagentia.
Bronvermelding: Leng, BL., Lin, X., Dong, HY. et al. Regulating interfacial water for oxygen transfer to benzylic C(sp3)–H bonds via Ni-activated tungsten-oxygen covalency. Nat Commun 17, 2355 (2026). https://doi.org/10.1038/s41467-026-69054-3
Trefwoorden: elektrocatalyse, wateroxidatie, benzylic C–H activatie, nikkel-geďmpte wolfraamoxide, groene chemie