Clear Sky Science · nl
In vivo dual RNA-Seq onthult sleutel-effectoren van verstoring van de epitheliale barrière door een extracellulaire pathogeen
Hoe sommige microben langs onze cellulaire hekken glippen
Onze organen zijn bekleed met dicht opeengepakte cellen die als muren functioneren en bloed, microben en toxines op hun plaats houden. Toch weten bepaalde microben tussen deze cellen door te glippen en zich door het lichaam te verspreiden. Deze studie laat in levendig detail zien hoe de bacterie die leptospirose veroorzaakt, een ernstige wereldwijde ziekte, stilletjes organen zoals de lever en nieren bereikt en vervolgens een slimme truc gebruikt waarbij calcium in onze cellen wordt ingezet om deze beschermende barrières open te wrikken.
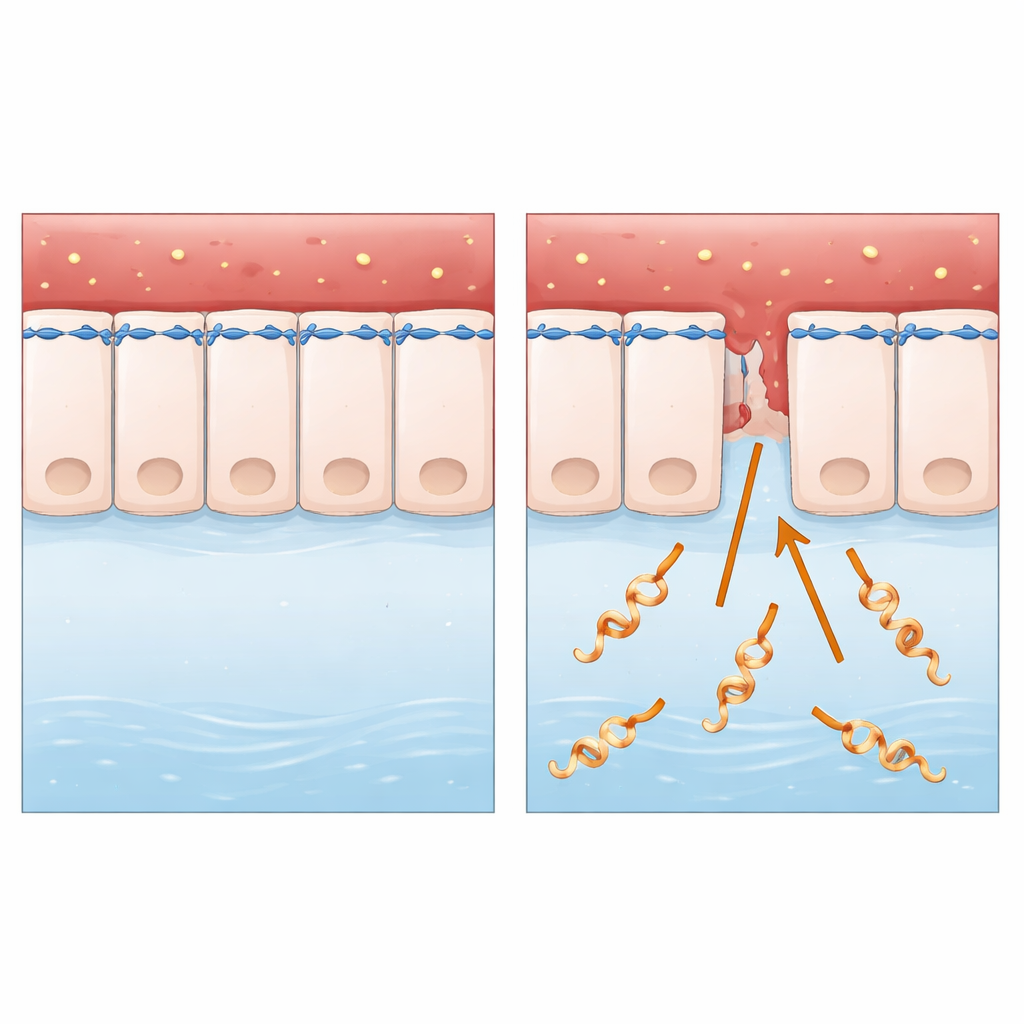
Een sluipende indringer van dierlijke en menselijke weefsels
Het onderzoek richt zich op Leptospira interrogans, een spiraalvormige bacterie die voornamelijk van dieren op mensen wordt overgedragen via besmet water of bodem. Na binnenkomst via kleine huidbeschadigingen of slijmvliezen reist ze via de bloedbaan en kan ernstige ziekte veroorzaken, waaronder lever- en nierfalen en inwendige bloedingen. In tegenstelling tot veel goed bestudeerde microben leeft Leptospira extracellulair en ontbreekt het aan sommige klassieke “moleculaire wapens” waar wetenschappers doorgaans op letten. Dat maakte het een ideaal proefmodel om een fundamentele vraag te stellen: hoe lukt het een ogenschijnlijk eenvoudige, vrijlevende bacterie zo efficiënt intacte cellagen te doorkruisen?
Host- en microbengenen tegelijk zien communiceren
Om het infectieproces in een levend dier vast te leggen, gebruikte het team dubbele RNA-sequencing in hamsters, een model voor acute leptospirose. Deze methode leest uit welke genen tegelijk in gastheer en pathogeen aan- of uitgezet zijn. De wetenschappers infecteerden hamsters en namen na één en drie dagen lever- en nierweefsel. Vroeg in de infectie, ondanks hoge aantallen bacteriën, veranderde de genactiviteit van de dieren nauwelijks, wat suggereert dat Leptospira aanvankelijk onder de radar van het immuunsysteem glipt. Op dag drie echter lieten beide organen een sterke reactie zien, vooral de lever: genen betrokken bij ontsteking, cel–cel verbindingen en het interne geraamte van cellen waren sterk veranderd, wat wijst op actieve herschikking van weefselbarrières.
Het cellulaire ritsslot van buitenaf loswrikken
Cellagen zijn afgesloten door tight junctions en adherens junctions, die naburige cellen met elkaar verbinden en verankeren aan een ring van actine en myosine, hetzelfde proteïnepaar dat spieren laat samentrekken. Microscopen van met Leptospira geïnfecteerde menselijke epitheelcellen toonden dat hun vorm veranderde, er openingen tussen cellen ontstonden en belangrijke verbindingsproteïnen verzwakten of op de verkeerde plaats terechtkwamen. Belangrijk is dat de cellen niet afstierven, wat betekent dat de barrière werd afgebroken, niet vernietigd. De onderzoekers zagen ook tekenen van stress in de eiwitvouwwerken van de cellen, maar het blokkeren van deze stress herstelde de junctions niet, wat hen op een andere verdachte wees.
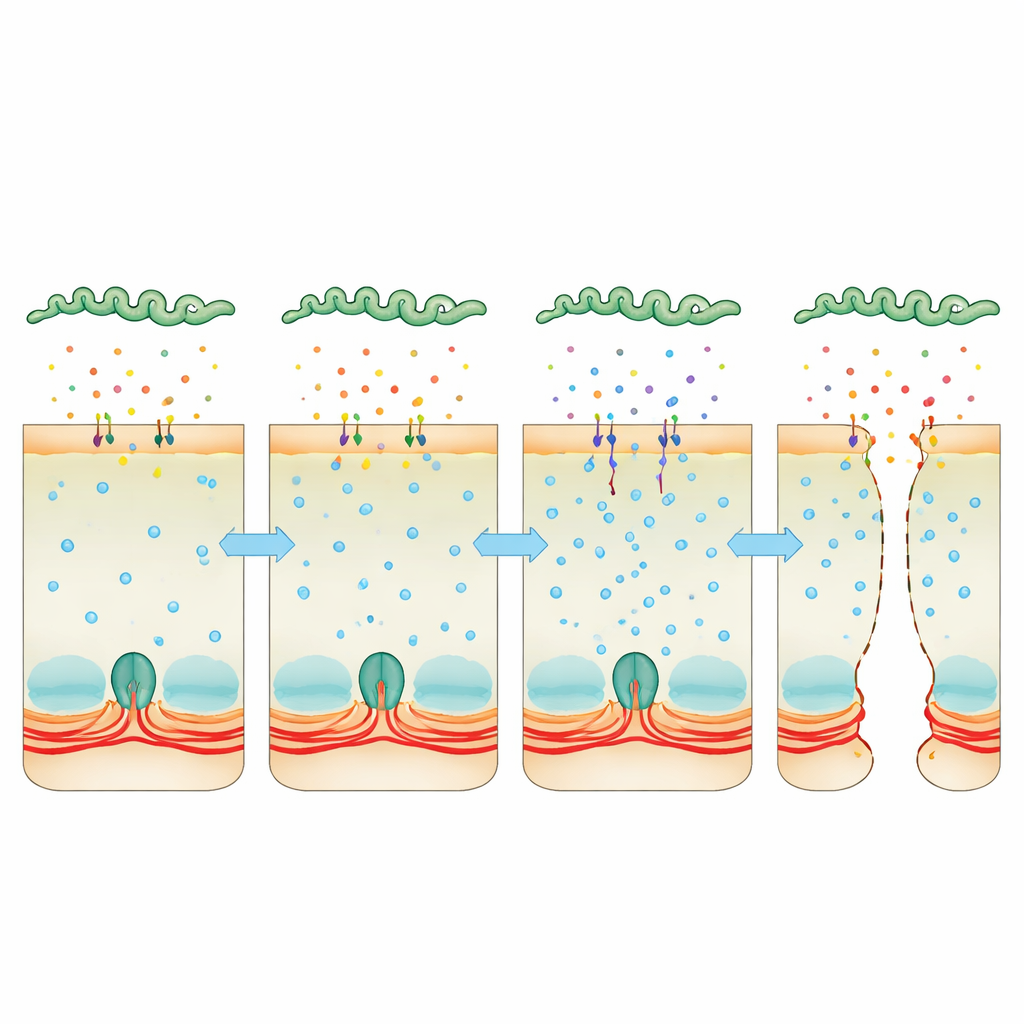
Calcium kapen als verborgen breekijzer
De aandacht verschoof naar calcium, een universeel signaal in cellen dat de actine‑myosine ring kan aanspannen of ontspannen. Geïnfecteerde cellen stapelden meer calcium op, en dit hing samen met verhoogde activiteit van myosine light chain kinase, een enzym dat de contractiele ring aan de junctions laat trekken. Toen het team een verbinding gebruikte die calcium wegvangt, of medicijnen die calmoduline of deze kinase remmen, bleven de cellagen beter intact en hadden bacteriën meer moeite om erdoorheen te persen. Tegelijkertijd toonde diepe sequencing van bacterieel RNA dat Leptospira in de gastheer de productie van twee “Virulence‑Modifying” eiwitten sterk opdrijft, die op toxines lijken. Deze eiwitten worden uitgescheiden in de omgeving, hechten aan gastheercellen en worden daarin teruggevonden. Wanneer bacteriën een of beide van deze eiwitten misten, waren ze veel minder goed in staat cellagen te passeren of dodelijke ziekte te veroorzaken, en hun uitgescheiden kweekvloeistof verhoogde de calciumspiegels of demonteerde junctions niet meer zo effectief.
Wat dit betekent voor ziekte en toekomstige verdedigingen
Gezamenlijk schetsen de resultaten een helder verhaal. Nadat Leptospira stilletjes het lichaam binnendringt, begint de bacterie toxine‑achtige Virulence‑Modifying eiwitten uit te scheiden. Deze eiwitten binden aan epitheelcellen en brengen de calciumbalans binnenin verstoord, wat op zijn beurt een contractiel pad activeert dat het cellulaire “ritsslot” tussen naburige cellen uit elkaar trekt. Naarmate tight junctions en adherens junctions verslappen, ontstaan microscopische openingen waardoor de bacteriën tussen cellen kunnen passeren, organen koloniseren en ernstige ziekte uitlokken. Door dit calciummedieerde mechanisme en de bacteriële eiwitten die eraan ten grondslag liggen te identificeren, opent de studie de weg naar nieuwe strategieën — zoals het blokkeren van deze eiwitten of hun signaalroute — om onze cellulaire hekken te versterken en de verspreiding van leptospirose en mogelijk andere infecties die vergelijkbare tactieken gebruiken, te beperken.
Bronvermelding: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Trefwoorden: leptospirose, epitheliale barrière, calciumsignaalgeving, bacteriële toxines, gastheer–pathogeen interacties