Clear Sky Science · nl
Supercharging-versterkte nDIA-MS maakt wereldwijde profilering van door geneesmiddelen veroorzaakte verschuivingen in proteoomoplosbaarheid mogelijk
Waarom eiwitgedrag verder gaat dan slechts aantallen
Geneesmiddelen kunnen niet alleen beïnvloeden hoeveel van een eiwit een cel produceert, maar ook waar dat eiwit naartoe gaat en of het vrij in oplossing blijft of aan cellulaire structuren vastklontert. Dergelijke verschuivingen in “waar” en “hoe” eiwitten in cellen bestaan, hangen nauw samen met ziekten zoals kanker en neurodegeneratie, maar zijn moeilijk op grote schaal te meten. Deze studie introduceert een snelle, krachtige methode om duizenden menselijke eiwitten tegelijk te screenen en te bepalen hoe hun oplosbaarheid — of ze vrij of juist meer vastzittend zijn — verandert wanneer cellen worden blootgesteld aan twee veelgebruikte experimentele geneesmiddelen.
Een snellere, scherpere manier om naar eiwitten te kijken
De auteurs bouwen voort op een kerentechniek van de moderne biologie: massaspectrometrie, een methode die eiwitfragmenten weegt en telt. Standaardmethoden blinken al uit in het bepalen hoeveel van elk eiwit aanwezig is, maar moeite hebben met het blootleggen van veranderingen in eiwittoestand, zoals binding aan DNA of het vormen van dichte assemblages. Hier verfijnen de onderzoekers een variant van massaspectrometrie genaamd narrow-window data-independent acquisition (nDIA-MS). Door kleine chemische hulpstoffen, zogenaamde supercharging-reagentia, toe te voegen aan de vloeistof die peptiden door het instrument voert, verhogen ze de elektrische ladingen van deze fragmenten en versterken ze het signaal aanzienlijk.
Na het testen van twee veelvoorkomende supercharging-additieven, dimethylsulfoxide (DMSO) en m-nitrobenzylalcohol (mNBA), constateren ze dat 3% DMSO de grootste algehele signaalversterking en het hoogste aantal gedetecteerde eiwitten geeft, terwijl mNBA beter is in het vergroten van het aantal en de lading van individuele peptidenfragmenten. Met de geoptimaliseerde opstelling kan het team ongeveer 9.600 menselijke eiwitten identificeren uit slechts één microgram van een standaard cellysaat in een run van 15 minuten — een opmerkelijke combinatie van snelheid en diepgang voor routinematige experimenten. Deze prestatie bereidt de weg voor het gebruik van nDIA-MS niet alleen om eiwitten te tellen, maar ook om te onderzoeken hoe hun fysische toestand reageert op stress.
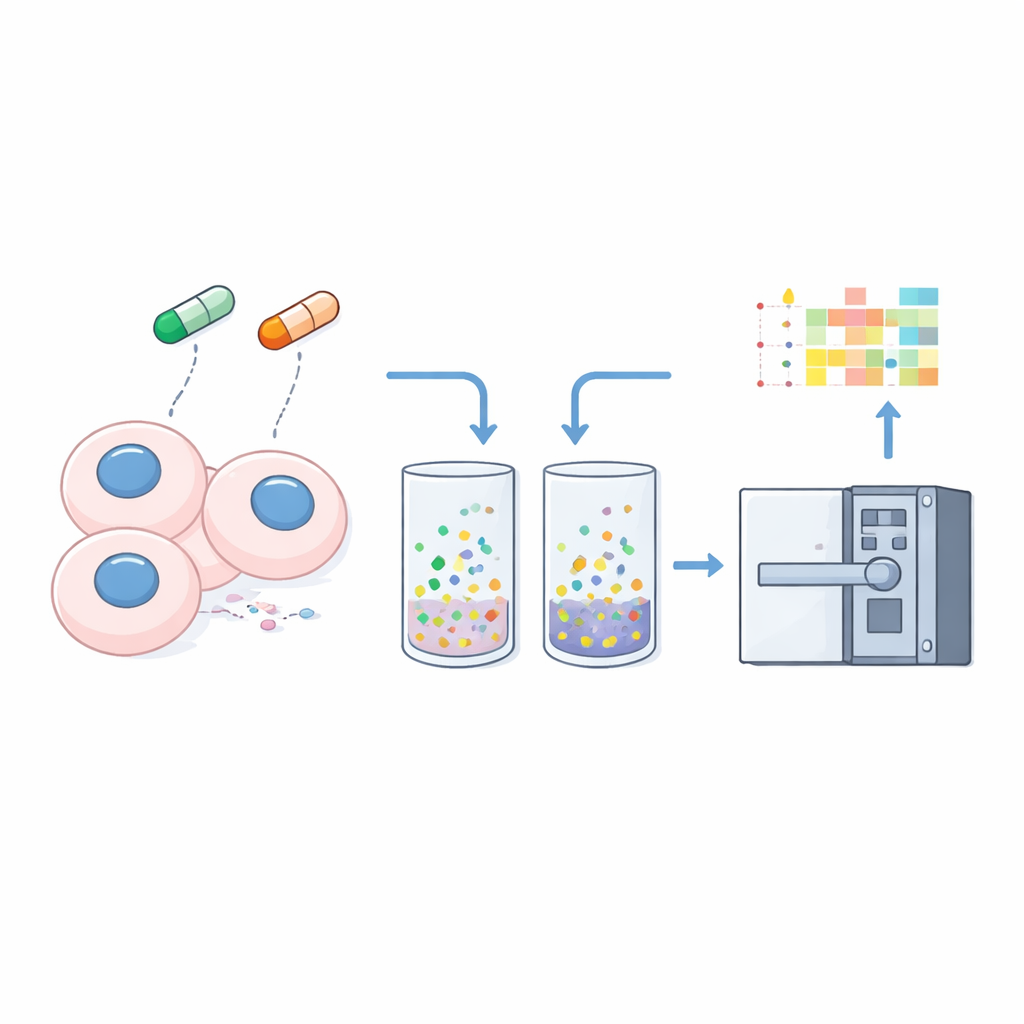
Oplosbaarheid vertalen naar een meetbare indicator van cellulaire verandering
Om oplosbaarheid in een meetbaar signaal om te zetten, behandelen de onderzoekers cellen voorzichtig met een mild detergent dat vrij oplosbare eiwitten extraheert, terwijl materiaal dat sterk aan DNA, membranen of andere structuren gebonden is, achterblijft. Ze analyseren zowel het volledige cellysaat als dit “onoplosbare” pellet van drie kankercellijnen met de geoptimaliseerde nDIA-MS-methode. Door de abundantie van elk eiwit in het pellet te vergelijken met die in het volledige celmonster, berekenen ze een simpele “onoplosbaarheidsratio” — hogere waarden wijzen op sterkere associatie met cellulaire structuren, lagere waarden op een meer oplosbare, vrije staat.
Het team stelt de cellen vervolgens slechts één uur bloot aan twee geneesmiddelen: MG132, een proteasoomblokker die voorkomt dat cellen ongewenste eiwitten afbreken, en ML-792, een remmer van SUMO-activatie die ingrijpt op een belangrijk eiwitlabelingssysteem. Deze korte blootstelling is bewust; ze is bedoeld om snelle, vroege verschuivingen in eiwitgedrag vast te leggen voordat veranderingen in genexpressie zich volledig hebben voltrokken. Zelfs in dit korte tijdsbestek kunnen ze oplosbaarheids- en abundantieveranderingen kwantificeren voor 8.694 eiwitten en bevestigen dat hun fractionering klassieke oplosbare eiwitten, zoals tubuline, duidelijk scheidt van chromatinegebonden eiwitten, zoals histonen.
Geneesmiddelen die het eiwitlandschap van de cel hervormen
MG132 en ML-792 veroorzaken wijdverspreide maar onderscheiden herstructureringen van eiwitoplosbaarheid. MG132 maakt in de drie cellijnen meer dan duizend eiwitten onoplosbaarder en meer dan zeshonderd juist oplosbaarder. Veel van de getroffen eiwitten bevinden zich op kruispunten van eiwitkwaliteitscontrole, DNA-schaderespons, genregulatie en autofagie — het zelfreinigingssysteem van de cel. Bijvoorbeeld, componenten van het proteasoomactivatorcomplex en adaptor-eiwitten die helpen defecte eiwitten te labelen, worden minder oplosbaar, wat suggereert dat wanneer afbraak wordt geblokkeerd, sleutelcomponenten van de kwaliteitscontrole zelf vast komen te zitten op structuren zoals chromatine of membranen. Autofagie-eiwitten en schade-responsspelers, waaronder de stressregelaar HSF1, verschuiven ook naar meer onoplosbare, condensaatachtige toestanden, wat consistent is met de vorming van nucleaire stresslichamen.
ML-792 daarentegen richt zich sterk op eiwitten die betrokken zijn bij transcriptie en op het SUMO-systeem zelf. Honderden eiwitten worden ofwel onoplosbaarder ofwel oplosbaarder wanneer SUMO-activatie wordt geblokkeerd, en kern-SUMO-eiwitten verplaatsen zich naar de oplosbare pool, zoals verwacht. De studie benadrukt opvallend gedrag: subunits van RNA-polymerase III worden onoplosbaarder, wat wijst op gewijzigde nucleaire import of chromatinebinding; belangrijke repressoren geassocieerd met nucleaire lichamen, zoals SP100 en DAXX, worden oplosbaarder, wat suggereert dat SUMO‑merken helpen hen in deze compartimenten te sekwestreren. Wanneer beide geneesmiddelen afzonderlijk of na elkaar worden toegepast, vertonen sommige eiwitten, waaronder NAB2, SMAD2 en RB1, gecoördineerde of zelfs tegengestelde oplosbaarheidsverschuivingen, wat een genuanceerde wisselwerking onthult tussen het ubiquitine- en het SUMO-labelsysteem in de controle van eiwitlokalisatie.
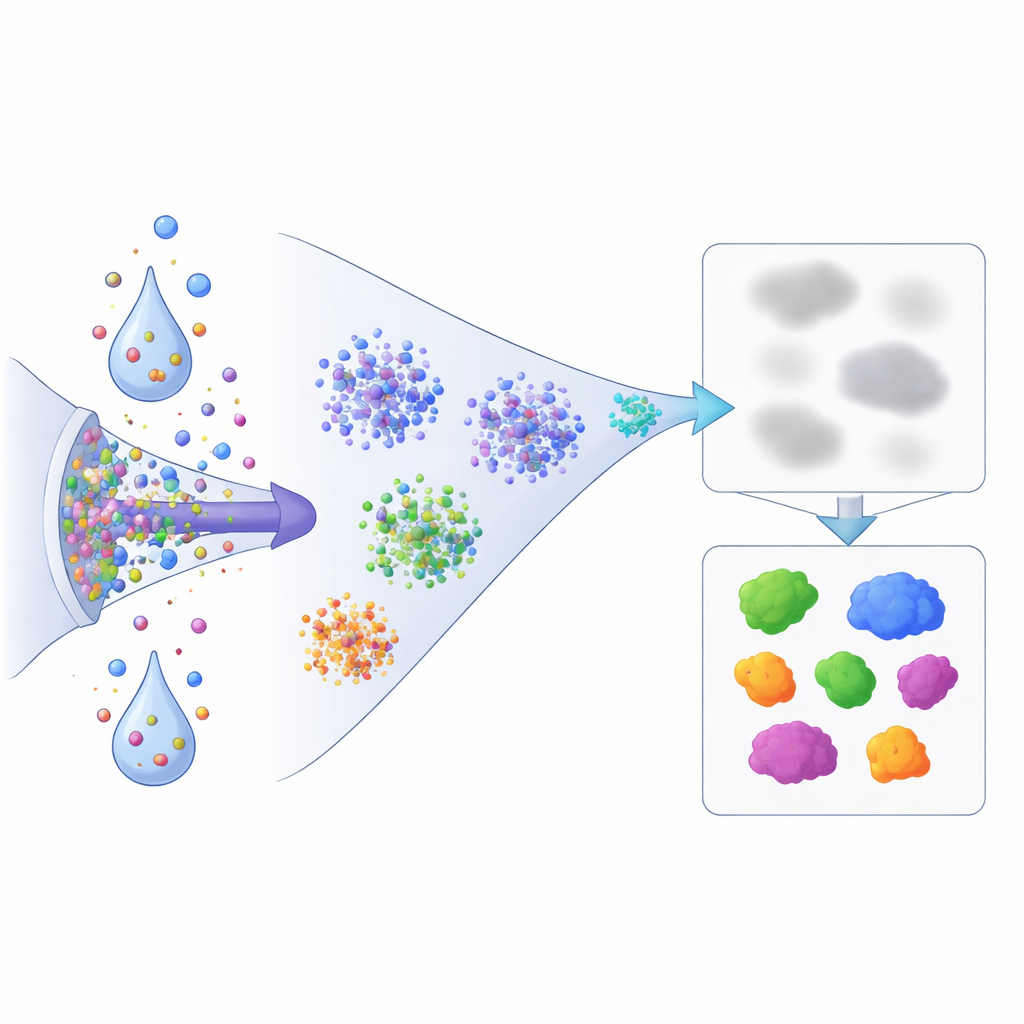
Wat dit betekent voor toekomstige geneesmiddelenontwikkeling
Voor niet‑specialisten is de kernboodschap dat eiwitten niet alleen in hoeveelheid omhoog of omlaag gaan wanneer cellen worden belast of behandeld met geneesmiddelen; ze verplaatsen zich ook, condenseren en veranderen hoe stevig ze aan cellulaire structuren gebonden zijn. Dit werk levert een hogesnelheids-, proteoomwijd gereedschap om die verschuivingen te volgen. Door een afgestemde massaspectrometrieworkflow te combineren met een eenvoudige vergelijking tussen oplosbaar en onoplosbaar, tonen de auteurs aan dat veelgebruikte experimentele geneesmiddelen snel het interne eiwitlandschap reorganiseren op manieren die standaard abundantiemetingen zou missen. De benadering opent de deur naar het in kaart brengen van hoe kandidaat-geneesmiddelen eiwittoestanden in de hele cel herschikken, en helpt onderzoekers onverwachte doelen, stressroutes en falenpunten te ontdekken die cruciaal kunnen zijn voor het begrijpen van zowel therapeutische werking als bijwerkingen.
Bronvermelding: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Trefwoorden: proteoomoplosbaarheid, massaspectrometrie, proteasoomremmer MG132, SUMOylatieremmer ML-792, eiwittoestandovergangen