Clear Sky Science · nl
Gere-engineerde interne architectuur van kern‑schaal lipidennanodeeltjes bevordert efficiënte mRNA‑endosomale vrijgave
Waarom deze nieuwe aflevertruc ertoe doet
Veel van de meest veelbelovende nieuwe medicijnen, van COVID‑19‑vaccins tot experimentele kankertherapieën, zijn opgebouwd uit boodschapper‑RNA, of mRNA. Maar er is een hardnekkig probleem: zodra deze fragiele strengs onze cellen binnendringen, raakt het grootste deel gevangen en vernietigd in kleine interne zakjes die endosomen worden genoemd. Deze studie introduceert een slimme herontwerping van de kleine vetbolletjes, bekend als lipidennanodeeltjes, die mRNA vervoeren. Door hun interne structuur rond een vaste goudkern te herschikken, verbeteren de onderzoekers dramatisch hoeveel mRNA ontsnapt naar de werkruimte van de cel, waar het daadwerkelijk nuttige eiwitten kan maken.
Kleine koeriers een beter lichaamsplan geven
Huidige mRNA‑vaccins en‑therapieën vertrouwen grotendeels op zachte, klonterige deeltjes die bestaan uit een mix van vetten die het mRNA omsluiten. In theorie zouden speciale ‘ioniseerbare’ vetten in deze deeltjes positief geladen moeten worden in het zure binnenste van endosomen en het endosomale membraan moeten openrukken, waardoor het mRNA vrijkomt. In de praktijk heft de negatieve lading van het mRNA veel van dit effect op, zodat slechts ongeveer 2 procent van het geleverde mRNA ooit de eiwitproducerende machinerie van de cel bereikt. De auteurs stelden een eenvoudige maar krachtige vraag: in plaats van alleen de chemie van de vetten te veranderen, wat als ze de interne architectuur van het deeltje her‑engineerden om te bepalen waar het mRNA en de lipiden zich ten opzichte van elkaar bevinden?
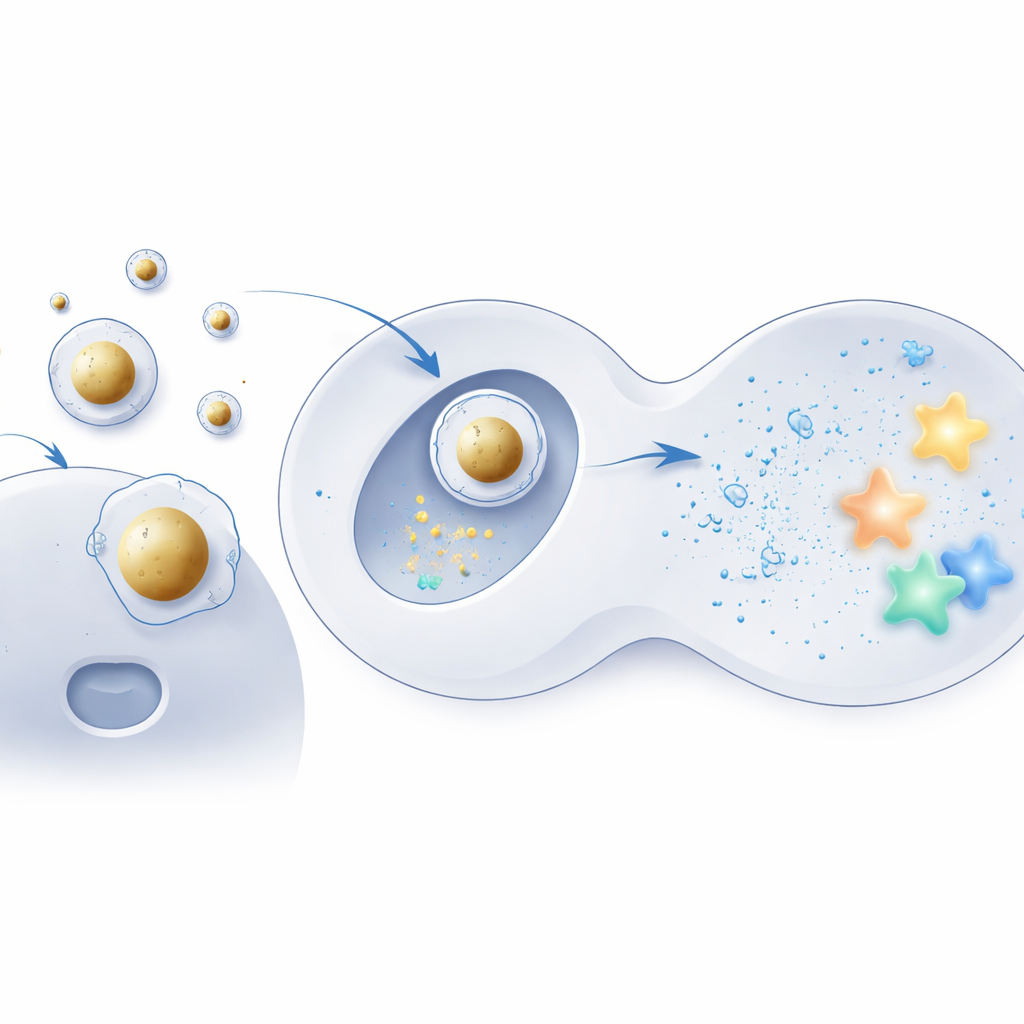
Een goudgecentreerde afleveringsschil bouwen
Om dit idee te testen, gebruikte het team kleine gouden bolletjes als stijve kernen en bedekte ze met dezelfde ioniseerbare lipiden die in conventionele formuleringen worden gebruikt. Het negatief geladen mRNA werd eerst op deze kernen gecondenseerd, en pas daarna werd de assemblage omwikkeld met een vertrouwde mix van hulpvetten en stabiliserende moleculen, waardoor een ordelijke kern‑schaalstructuur ontstond. Elektronenmicroscopie en computersimulaties toonden aan dat deze “Au‑LNP’s” zeer uniform, thermodynamisch stabiel en vormvast bleven onder waterige, lichaamachtige omstandigheden. Belangrijk was dat hun totale vetsamenstelling hetzelfde bleef als die van standaarddeeltjes, waardoor de interne structuur — niet de ingrediënten — als sleutelwijziging werd geïsoleerd.
Hoe een herschikt interieur de ontsnapping verbetert
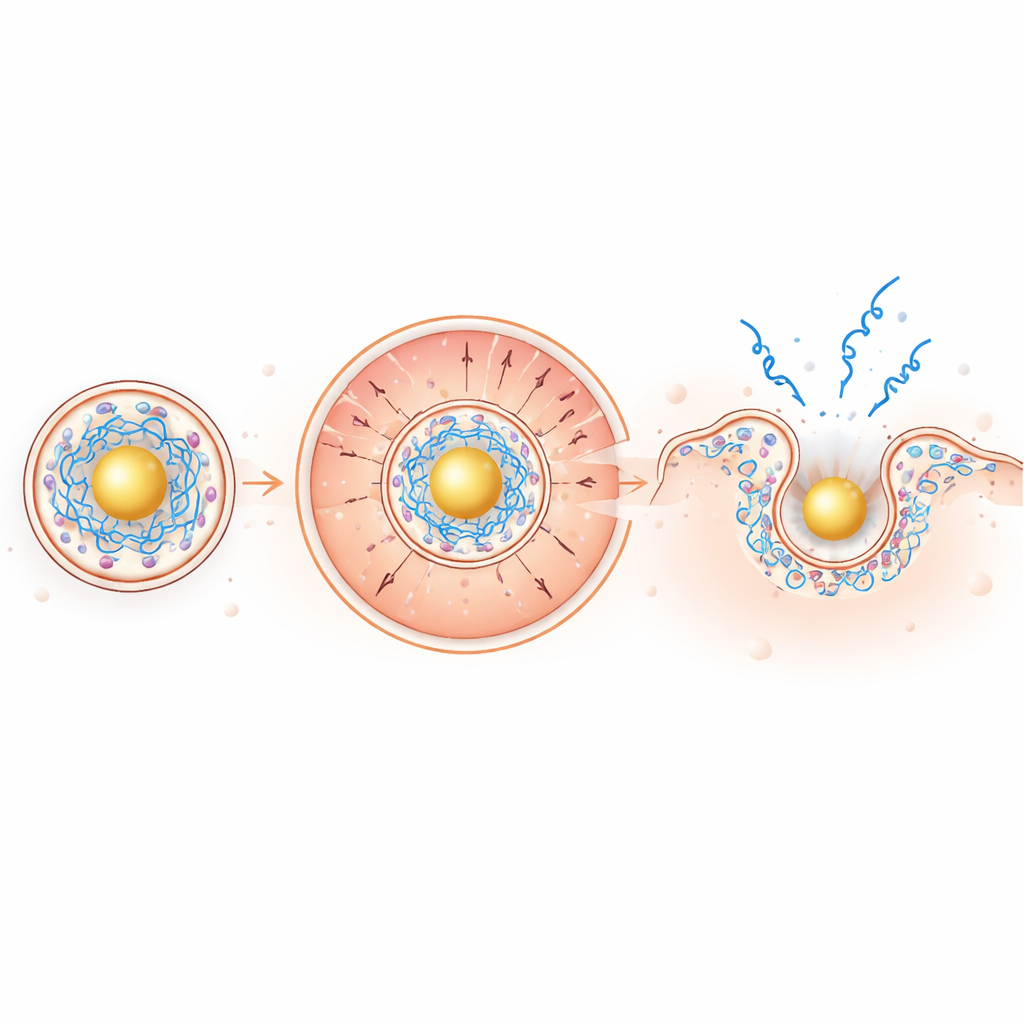
In de licht zure endosomale omgeving wordt de goudgebaseerde kern sterk positief, waardoor het negatief geladen mRNA naar binnen wordt getrokken terwijl de positief geladen ioniseerbare lipiden naar buiten worden geduwd richting het omringende membraan. Deze door lading aangedreven segregatie concentreert membraanschurende lipiden precies daar waar ze nodig zijn. In modelmembraantests en in rode bloedcellen waren de nieuwe deeltjes effectiever in het doorprikken van membranen bij lage pH terwijl ze bij neutrale pH rustig bleven — een wenselijke veiligheidskenmerk. In levende cellen liet beeldvorming van fluorescerend mRNA ongeveer een verdubbeling van endosomale ontsnapping zien en een verbazingwekkende ~100‑voudige toename in hoe ver mRNA zich door het cytoplasma verspreidde vergeleken met conventionele deeltjes.
Van schotels naar muizen: sterkere signalen en betere bescherming
Deze fysieke voordelen vertaalden zich in echte biologische winst. In meerdere celtypen zorgden de goudkerndeeltjes voor een veel hogere productie van rapportereiwitten dan standaardformuleringen, vooral bij lage doses. Bij muizen verhoogden ze de mRNA‑gestuurde eiwitproductie tot wel vijf‑ tot zevengvoud na injecties in spier of ader, zonder te veranderen waar in het lichaam de deeltjes de neiging hadden zich op te hopen. Bij gebruik voor de afgifte van een SARS‑CoV‑2‑spike mRNA‑vaccin verdubbelden de opnieuw ontworpen deeltjes ruwweg de antilichaamniveaus na de eerste prik en verhoogden die verder na een boosterdosis, terwijl ze ook krachtiger virusneutraliserende antilichamen produceerden. In een uitdagend triple‑negatief borstkankermodel krimpten door de nieuwe deeltjes gedragen mRNA‑kankervaccins tumoren effectiever, verlaagden ze tumortsignalen en verlengden ze opmerkelijk de overleving.
Veiligheid en een pad naar toekomstige geneesmiddelen
Ondanks het gebruik van goud in hun kern leken de deeltjes goed verdraaglijk bij muizen. Lichaamsgewichten, ontstekingsmarkers en weefselonderzoeken toonden geen grote toxiciteit, en de goudniveaus in organen daalden binnen twee dagen weer richting het uitgangsniveau. De auteurs benadrukken dat goud voornamelijk dient als proof‑of‑concept‑skelet: hetzelfde interne ontwerpprincipe kan worden toegepast op andere veilige of biologisch afbreekbare materialen. De kernboodschap voor niet‑specialisten is dat de manier waarop we mRNA in zijn kleine drager verpakken net zo belangrijk kan zijn als waarmee we het verpakken. Door lipidennanodeeltjes een meer geordende interne indeling te geven, biedt dit werk een nieuwe manier om een langdurige knelpunt in mRNA‑afgifte te overwinnen — het ontsluiten van effectievere vaccins en therapieën voor infectieziekten, kanker en verder.
Bronvermelding: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Trefwoorden: mRNA‑afgifte, lipidennanodeeltjes, endosomale ontsnapping, nanogeneeskunde, RNA‑vaccins