Clear Sky Science · nl
FGF13 functioneert als regulator van de ERK/aërobe glycolyse-as in de ontstekingsstaat tijdens sepsis-geïnduceerde longschade
Waarom deze studie belangrijk is voor patiënten met ernstige infecties
Sepsis is een levensbedreigende complicatie van een infectie die binnen enkele uren kan leiden tot longfalen, waardoor patiënten afhankelijk worden van beademing en een hoge kans op overlijden hebben. Deze studie onderzoekt een weinig bekend eiwit in onze cellen, FGF13, en onthult hoe het bijdraagt aan de ontspoorde ontsteking en energieoverschrijding die de longen tijdens sepsis ernstig beschadigen. Door dit verborgen regelcircuit te volgen, wijst het werk op nieuwe geneesmiddelendoelwitten die mogelijk de ontstekingsstorm in de longen kunnen temperen zonder het hele immuunsysteem stil te leggen.
Een verborgen speler bij longschade tijdens sepsis
De onderzoekers begonnen met het vergelijken van longweefsel van sepsis-muizen en menselijke patiënten met weefsel van niet-septische controles. Ze onderzochten een familie moleculen, de fibroblastgroeifactoren, die helpen de longgezondheid te behouden. Daarbinnen stak FGF13 eruit: de niveaus daarvan waren opvallend lager in de longen van septische patiënten en dieren. Bij het in kaart brengen van de lokalisatie van FGF13 vonden ze het vooral in twee belangrijke celtypen: endotheelcellen, die de binnenbekleding van bloedvaten vormen, en macrofagen, immuuncellen die ontsteking detecteren en versterken. In septische longen waren FGF13-positieve endotheelcellen en macrofagen sterk verminderd, wat suggereert dat veranderingen in dit molecuul verband kunnen houden met ernstige longschade.
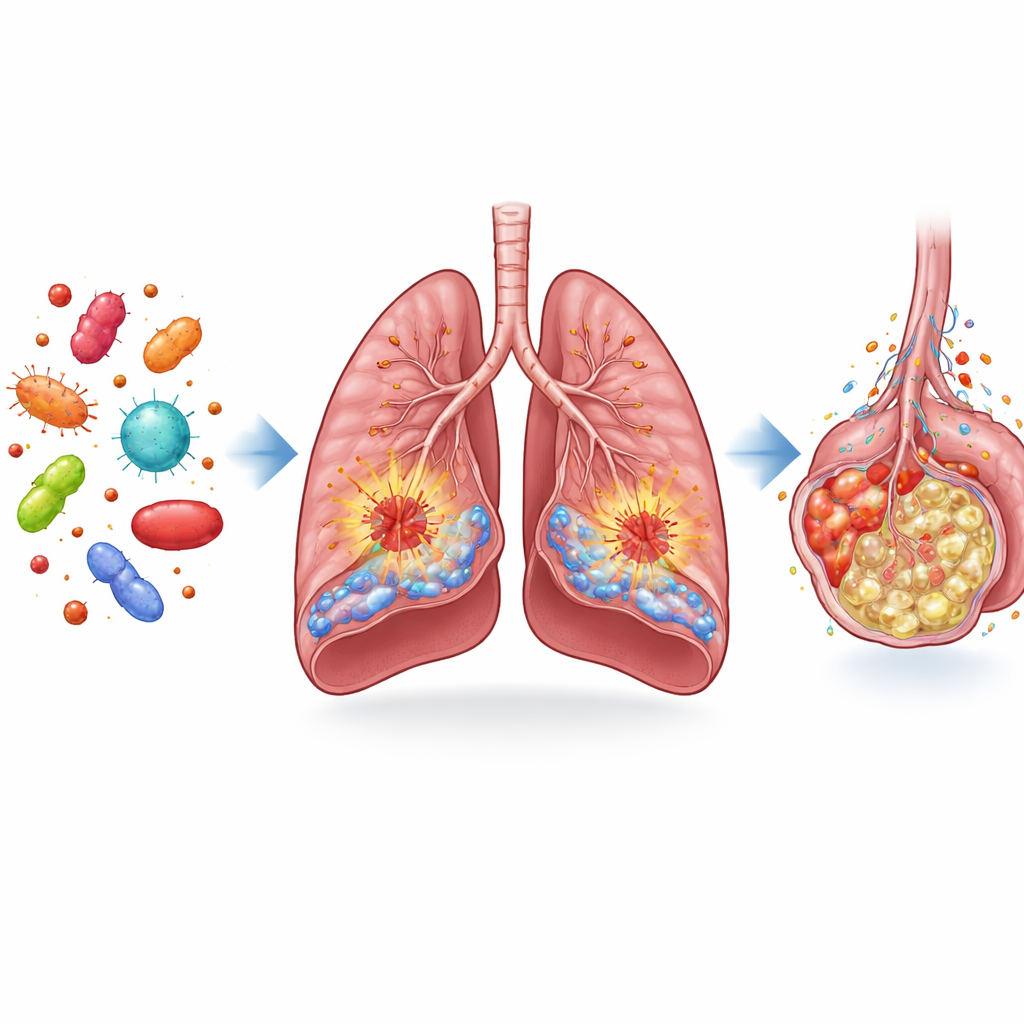
Hoe FGF13 longverdedigers verandert in aanjagers van schade
Om te testen wat FGF13 daadwerkelijk doet, gebruikte het team genetische technieken bij muizen om het eiwit ofwel uit specifieke cellen te verwijderen of die cellen juist te dwingen er meer van te maken. Wanneer FGF13 alleen in endotheelcellen werd verwijderd, hadden septische muizen minder lekkende, gezwollen longen, minder binnendringende immuuncellen en een betere overleving. Het omgekeerde gebeurde toen endotheelcellen werden gemanipuleerd om te veel FGF13 te produceren: longoedeem, bloedingen en ophoping van inflammatoire cellen verslechterden. Een soortgelijke uitkomst werd gezien in macrofagen. Muizen zonder FGF13 in deze immuuncellen vertoonden zwakkere ontstekingsreacties en minder longschade, terwijl macrofagen die extra FGF13 maakten meer ontstekingsbevorderende moleculen afscheidden en de schade verergerden. In celkweek maakte het verlagen van FGF13 bloedvatcellen en macrofagen minder 'kleverig', minder ontstoken en minder toxisch voor hun buren.
Ontstoken cellen schakelen over op een suikerhongerige modus
Ontstoken cellen verschuiven, net als kankercellen, vaak hun energiebalans: in plaats van brandstof langzaam met zuurstof te verbranden, breken ze snel suiker af in een proces dat aërobe glycolyse wordt genoemd, waarbij melkzuur ontstaat. De auteurs vonden dat FGF13 deze omschakeling sterk stimuleert. In septische muizen zonder FGF13 in endotheelcellen of macrofagen waren de lactaatwaarden in het bloed lager. In kweek namen cellen met verminderd FGF13 minder glucose op en produceerden ze minder lactaat na ontstekingsstimulatie, terwijl cellen met extra FGF13 juist verhoogde glycolyse lieten zien. Toen de onderzoekers glycolyse blokkeerden met een geneesmiddel, werd het ontstekingsbevorderende effect van teveel FGF13 grotendeels onderdrukt, wat de schadelijke rol van het molecuul direct verbindt met dit suikerverbrandingsprogramma.
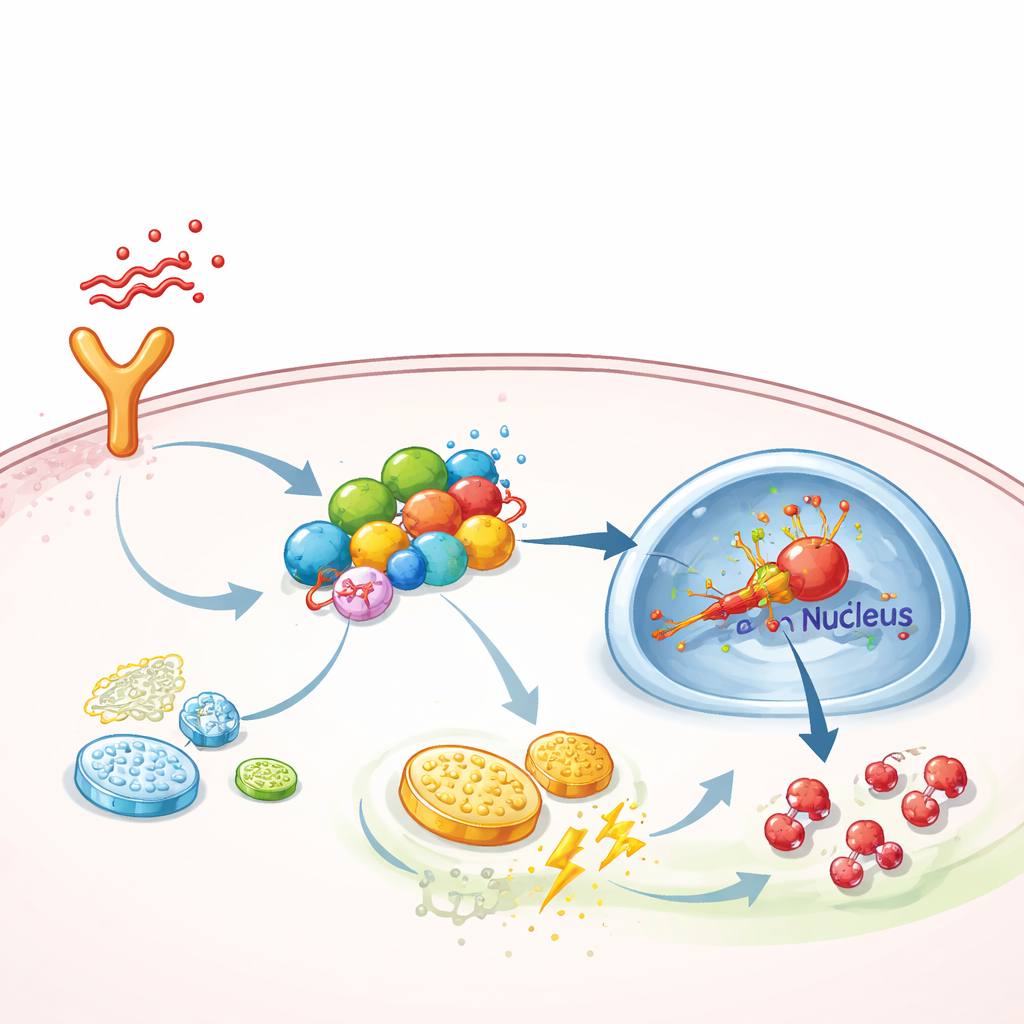
Een moleculair steigerwerk dat ontstekingssignalen versterkt
Dieper gravend vroegen de onderzoekers hoe FGF13 cellen naar deze hoge-standstofwisseling duwt. Ze ontdekten dat FGF13 fysiek bindt aan meerdere signaaleiwitten die een keten vormen van receptoren aan het celoppervlak naar de celkern—specifiek de TAK1–MEK–ERK-route, die bekendstaat als activator van een hoofdregelaar van lage-zuurstofreacties, HIF-1α. FGF13 werkt als een steiger of scaffold, die deze componenten bij elkaar houdt zodat signalen efficiënter doorgegeven worden. Wanneer FGF13 afnam, daalde de activatie van ERK en HIF-1α en verminderde de glycolyse; bij toename van FGF13 werd de route hyperactief. Overexpressie van HIF-1α in muizen maakte het beschermende effect van FGF13-verwijdering teniet, terwijl een selectieve ERK-remmer, SCH772984, de schade veroorzaakt door overproductie van FGF13 neutraliseerde en de longconditie bij septische dieren verbeterde.
Wat dit betekent voor toekomstige sepsistherapieën
Voor een lezer zonder specialistische achtergrond is de kernboodschap dat sepsis-geïnduceerde longschade niet louter willekeurige weefselvernietiging is; ze wordt aangedreven door een specifiek moleculair circuit binnen bloedvatcellen en macrofagen. FGF13 staat centraal in dit circuit en helpt een signaleringshub samen te stellen die cellen dwingt in een suikerverbrandende, sterk ontstekingsbevorderende staat te gaan. Hoewel FGF13-niveaus tijdens sepsis dalen—waarschijnlijk als onderdeel van een bredere stressrespons—laat deze studie zien dat het resterende eiwit nog steeds een krachtige aanjager van schade is. Door ofwel de signaalpartners van FGF13 of de door het eiwit bevorderde glycolytische omschakeling te blokkeren, zou het mogelijk zijn longzwelling, lekkage en ontsteking te verminderen zonder het vermogen van het lichaam om infecties te bestrijden volledig lam te leggen. Dit werk benadrukt daarmee FGF13 en de ERK–HIF‑1α–glycolyse-as als veelbelovende aanknopingspunten voor het ontwikkelen van meer gerichte, veiligere behandelingen voor sepsis-gerelateerd longfalen.
Bronvermelding: Zhu, J., Wang, J., Jiang, C. et al. FGF 13 functions as a regulator of the ERK/aerobic glycolysis axis in the inflammatory state during septic lung injury. Nat Commun 17, 2383 (2026). https://doi.org/10.1038/s41467-026-69014-x
Trefwoorden: sepsis-geïnduceerde longschade, FGF13, endotheliale ontsteking, aërobe glycolyse, ERK-signaaltransductie