Clear Sky Science · nl
Gecombineerde gerichte en epigenetische therapie versterkt antitumorimmuniteit door stabilisatie van GATA6-afhankelijke MHCI-expressie in pancreatische ductale adenocarcinomen
Waarom dit onderzoek belangrijk is voor pancreaskanker
Pancreatisch ductaal adenocarcinoom behoort tot de dodelijkste vormen van kanker, grotendeels omdat het zich aan het immuunsysteem onttrekt en ongevoelig is voor de meeste middelen. Deze studie onthult een specifiek tumorcellen‑toestand, gestuurd door het gen GATA6, die pancreaskankercellen kwetsbaarder maakt voor immuunaanvallen. De auteurs tonen ook aan hoe de combinatie van twee soorten geneesmiddelen deze kwetsbare toestand kan behouden en de capaciteit van cytotoxische T‑cellen om tumoren aan te vallen in experimentele modellen kan versterken.
Een tumorcellen‑toestand die het immuunsysteem uitgenodigd
Niet alle pancreaskankercellen gedragen zich hetzelfde. Sommige behouden een meer ordelijke, epitheliale identiteit, terwijl andere verschuiven naar een meer mobiele, agressieve, mesenchymale toestand. De transcriptiefactor GATA6 helpt de epitheliale identiteit te handhaven en wordt geassocieerd met betere uitkomsten bij patiënten. In grote patiëntencohorten bevatten tumoren met hoge GATA6‑waarden meer immuuncellen, waaronder CD8 “killer” T‑cellen, dan tumoren met weinig of geen GATA6. Met geavanceerde ruimtelijke beeldvorming van menselijke tumorstalen vonden de onderzoekers dat GATA6‑positieve kankercellen vaker naast CD8‑T‑cellen lagen en hogere niveaus van een molecuul genaamd MHCI vertoonden, dat fungeert als een vlag die T‑cellen laat zien wat zich in de cel bevindt. Deze waarnemingen suggereren dat GATA6 een tumorcelpopulatie markeert die van nature beter zichtbaar is voor het immuunsysteem. 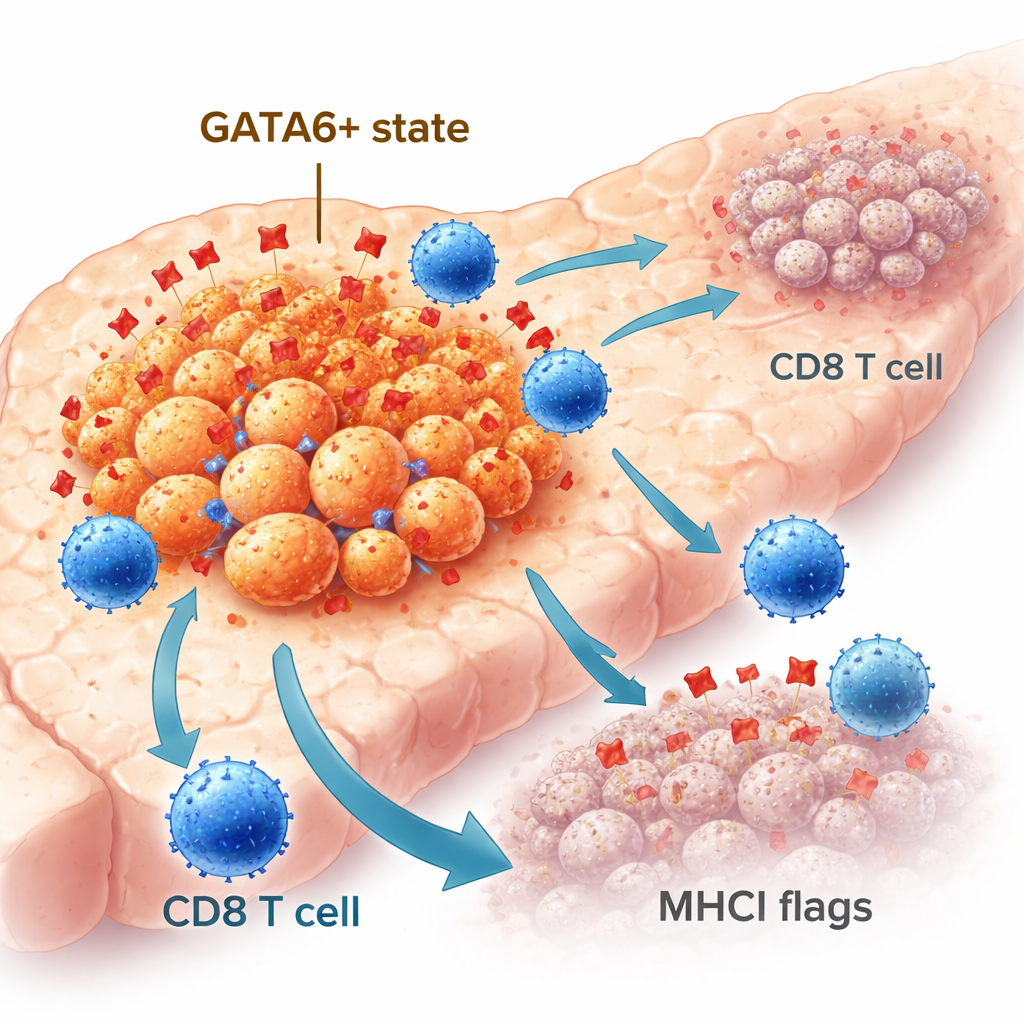
Gerichte therapie die tumorzichtbaarheid vergroot—maar met een prijs
Het team onderzocht vervolgens of gerichte geneesmiddelen deze zichtbaarheid verder konden verbeteren. Ze concentreerden zich op MEK‑remmers, een klasse geneesmiddelen die een groeisignaleringsroute blokkeren die vaak actief is bij pancreaskanker. In muis‑pancreaskankercellijnen en in tumoren die in muizen en in patiënt‑afgeleide xenografts werden gekweekt, verhoogde MEK‑inhibitie MHCI op het oppervlak van GATA6‑rijke tumorcellen, waardoor ze potentiëel betere doelwitten voor T‑cellen werden. Wanneer tumoren met hoge GATA6‑expressie in muizen werden behandeld met MEK‑remmers, vertraagde de tumorgroei, nam MHCI toe en drongen meer CD8‑T‑cellen met cytotoxische componenten de tumoren binnen. Het direct blokkeren van GATA6, hetzij door genuitval hetzij door snelle afbraak van het eiwit, maakte deze door MEK‑remmer geïnduceerde stijging van MHCI en de bijbehorende tumorcontrole ongedaan, wat aantoont dat GATA6 essentieel is voor dit gunstige effect.
Hoe tumoren zich aanpassen: overgaan naar een moeilijker te doden toestand
Het verhaal kreeg echter een wending. Langdurige behandeling met MEK‑remmers dreef veel tumorcellen om te verschuiven van de GATA6‑positieve epitheliale toestand naar een meer mesenchymale, GATA6‑arme toestand die is geassocieerd met behandelingsresistentie. In zowel muismodellen als patiënt‑afgeleide xenografts toonden MEK‑remmer‑behandelde tumoren na verloop van tijd minder GATA6‑positieve cellen, meer markers van epitheel‑naar‑mesenchymale transitie en in het algemeen minder duurzame voordelen. Hoewel individuele GATA6‑positieve cellen nog steeds MHCI opreguleerden als reactie op het geneesmiddel, beperkte de krimpende omvang van deze populatie de algehele verbetering in tumorantigeenpresentatie en verklaart dit mede waarom MEK‑remmers alleen teleurstellende resultaten hebben laten zien in klinische onderzoeken bij pancreaskanker.
Epigenetische middelen die tumoren in de kwetsbare toestand houden
Om deze adaptieve ontsnapping tegen te gaan, wendden de onderzoekers zich tot histon‑deacetylaseremmers, of HDAC‑remmers, een klasse epigenetische middelen waarvan bekend is dat ze de celidentiteit en immuunzichtbaarheid beïnvloeden. In celkweken en muismodellen herstelde de combinatie van MEK‑remmers met klasse I HDAC‑remmers zoals domatinostat de GATA6‑expressie die was onderdrukt door MEK‑inhibitie, keerde tekenen van epitheel‑naar‑mesenchymale transitie om en verhoogde verder de MHCI‑niveaus op tumorcellen. Belangrijk was dat deze combinatietherapie leidde tot sterkere infiltratie en activatie van CD8‑T‑cellen en meer tumorceldood in orthotopische muizentumoren en in een genetisch gemodificeerd muismodel dat nauw menselijk pancreaskanker nabootst. Uitputting van CD8‑T‑cellen maakte een groot deel van het voordeel ongedaan, wat bevestigt dat de combinatie grotendeels werkt door het krachtiger maken van killer T‑cellen.
Richting slimmere combinatiebehandelingen voor een hardnekkige kanker
Samengevat stelt de studie een strategie voor waarbij gerichte MEK‑inhibitie en epigenetische HDAC‑inhibitie samen worden gebruikt om een door GATA6 aangedreven tumorcellen‑toestand te stabiliseren die rijk is aan MHCI en daardoor goed herkenbaar is voor het immuunsysteem. Door zowel het aantal GATA6‑positieve cellen te vergroten als hun MHCI‑“vlaggen” te versterken, bevordert de combinatie diepere CD8‑T‑celinfiltratie, sterkere cytotoxische activiteit en langere overleving in agressieve muismodellen van pancreaskanker. Hoewel HDAC‑remmers aanzienlijke bijwerkingen kunnen hebben en het werk preklinisch is, wijst dit onderzoek op toekomstige behandelstrategieën die pathway‑gerichte middelen en zorgvuldig gekozen epigenetische modulatoren kunnen combineren om pancreastumoren kwetsbaarder te maken voor de eigen immuunverdediging van het lichaam. 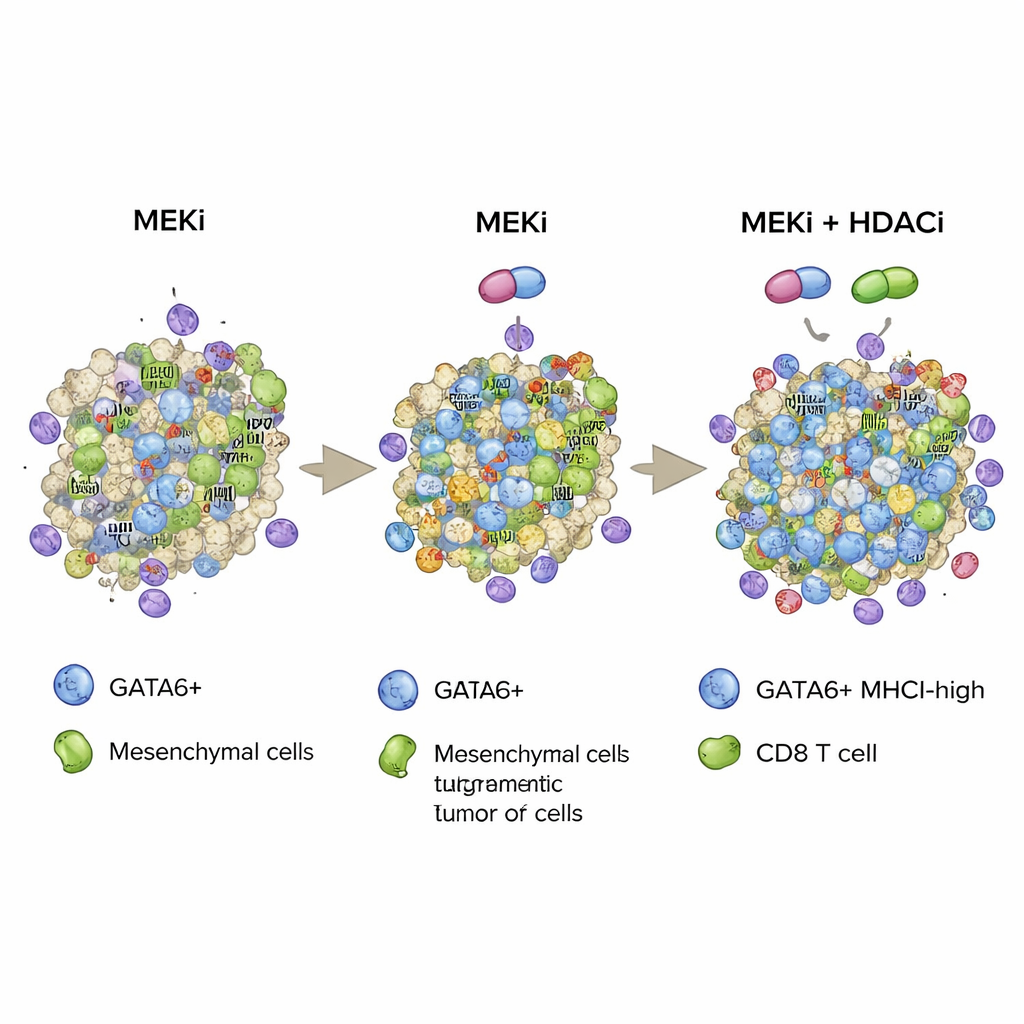
Bronvermelding: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
Trefwoorden: pancreaskanker, tumorimmuniteit, GATA6, MEK-remmer, HDAC-remmer