Clear Sky Science · nl
AACRNL geëvolueerd van virulentiefactor naar epigenetische parasiet die genoomexpansie aandrijft in vrijlevende eukaryoten
Wanneer oude toxines nieuwe trucs leren
Onze genomen zijn geen stille instructiehandleidingen. Het zijn drukke arena’s waar genen, virussen en mobiel DNA constant om ruimte en controle wedijveren. Deze studie onthult een verrassende speler in die strijd: een eiwit dat begon als een toxine dat microben gebruikten om gastheren aan te vallen, maar dat sindsdien in vrijlevende dieren is herbestemd tot een soort „epigenetische parasiet” die helpt zijn eigen voetafdruk in het genoom uit te breiden.
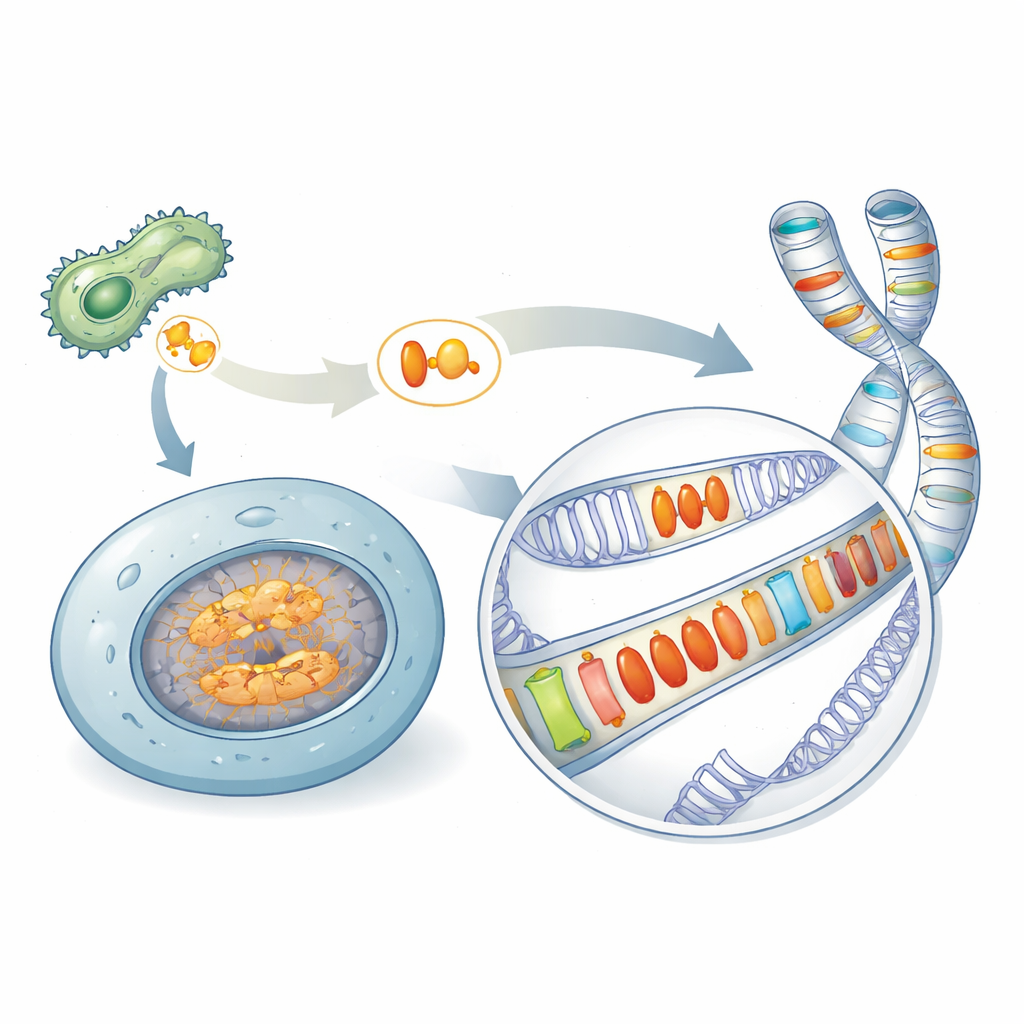
Een verborgen erfenis van microbiele wapens
Veel ziekteverwekkende microben vertrouwen op speciale eiwitten, effectors genoemd, om de verdediging van de organismen die ze infecteren te saboteren. Een beroemde familie, bekend als Crinklers, werd gedacht alleen in pathogenen voor te komen. Door een groot aantal soorten te scannen ontdekten de auteurs verwante eiwitten—hier gegroepeerd onder de naam AACRNL—op onverwachte plaatsen, waaronder sponzen, koralen, zee-egels en beenvissen die geen klassieke ziekteverwekkers zijn. Deze AACRNL-eiwitten behouden de toxine‑achtige kern die andere eiwitten chemisch kan modificeren, maar hun voorste ‘‘bezorg’’deel, dat pathogenen gebruiken om gastheercellen binnen te dringen, is grotendeels vergaan. Die structurele verandering wijst op een verschuiving van het aanvallen van andere organismen naar het handelen binnen de eigen cellen van de gastheer.
Een egoïstische omschakeling in het genoom
Bij beenvissen komen AACRNL-genen in meerdere kopieën voor, verspreid over verschillende chromosomen. Door aangrenzende DNA-stukken te vergelijken lieten de onderzoekers zien dat sommige AACRNL-lijnen zijn gestopt met zichzelf te kopiëren, terwijl andere zijn vermenigvuldigd met hulp van nabije springende DNA-segmenten die transposons worden genoemd. Deze transposons werken als genomische shuttles: wanneer ze bewegen of dupliceren, kunnen ze AACRNL mee slepen. Het resultaat is een lappendeken van herhaalde AACRNL-kopieën ingebed tussen transposon-sequenties, een kenmerk van een gen dat zich verspreidt voor zijn eigen voordeel in plaats van dat van de gastheer.
Het doorbreken van de dempknop van het genoom
Normaal houden cellen dergelijk mobiel DNA goed onder controle. Een belangrijke beveiliging is een chemische markering op eiwitten rond het DNA, bekend als H3K27me3, die gevaarlijke of rumoerige regio’s stil helpt houden. De auteurs vonden dat een actieve versie van AACRNL bij vissen, genoemd AACRNLβ, EZH2—het enzym dat deze repressieve markering aanbrengt—chemisch kan modificeren. Wanneer AACRNLβ EZH2 verandert, daalt de hoeveelheid H3K27me3 op zijn eigen genetische locatie en bij nabijgelegen transposons, opent het lokale DNA zich, en worden zowel AACRNLβ als zijn transposonburen sterker tot expressie gebracht. In feite drukt het eiwit zijn eigen ‘‘aan’’-knop en haalt het de remmen weg van de mobiele elementen die het naar nieuwe plekken in het genoom kunnen brengen.
Het ontwijken van de immuunwachters
Het loslaten van transposons en ongebruikelijke genetische activiteit brengt het risico met zich mee de aandacht van het immuunsysteem te trekken. De studie toont aan dat AACRNLβ ook dit probleem aanpakt. Het hecht een kleine chemische markering aan TRAF6, een centraal hub-eiwit dat helpt antivirale en inflammatoire signalen aan te zetten. Op deze manier gemarkeerd wordt TRAF6 minder stabiel en steeds vaker bestempeld voor afvoer door het afvalverwerkende systeem van de cel. Met dit signaalcentrum verzwakt, vuren belangrijke verdedigingsroutes minder sterk, waardoor een toleranter milieu ontstaat waarin AACRNLβ en de bijbehorende transposons kunnen blijven bestaan en zich kunnen kopiëren met minder risico op detectie.
Een kwetsbare wapenwedloop binnen de cel
Het verhaal eindigt niet met AACRNLβ die ongehinderd tekeergaat. Hetzelfde TRAF6-eiwit dat door AACRNLβ wordt gericht kan op zijn beurt weer eigen markeringen aan AACRNLβ toevoegen, waarmee het parasiet‑achtige eiwit wordt bestempeld voor afbraak. Dit heen en weer lijkt op een moleculaire wapenwedloop: AACRNLβ gebruikt toxine-afgeleide chemie om chromatine en immuniteit in zijn voordeel te buigen, terwijl gastheereiwitten tegenprikken door het te degraderen en zijn activiteit sporadisch en riskant te houden. De auteurs beweren dat dit touwtrekken een voormalig microbieel wapen in staat heeft gesteld te overleven als een egoïstige bewoner van vrijlevende genomen, DNA-inhoud uit te breiden en de regels van genetisch conflict van binnenuit te herschrijven.
Waarom dit belangrijk is voor ons beeld van genomen
Voor een niet‑specialist is de belangrijkste boodschap dat genomen niet alleen blauwdrukken zijn die geoptimaliseerd zijn voor het overleven van de gastheer. Ze herbergen ook opportunisten. Dit werk laat zien dat zelfs klassieke toxines kunnen worden getemd tot zulke elementen, hun oorspronkelijke destructieve chemie gebruikend om epigenetische sloten en immuunalarmen te omzeilen en zich over het genoom te verspreiden in de loop van de evolutie. Het begrijpen van dit type verborgen conflict helpt verklaren waarom genomen zo groot, complex en dynamisch zijn—en suggereert dat andere “gepensioneerde” toxines mogelijk stilletjes DNA herschrijven in vele soorten, misschien ook in die van ons.
Bronvermelding: Xu, T., Geng, S., Lv, X. et al. AACRNL evolved from virulence factor to epigenetic parasite driving genome expansion in free-living eukaryotes. Nat Commun 17, 2130 (2026). https://doi.org/10.1038/s41467-026-69012-z
Trefwoorden: egoïstische genetische elementen, genoomevolutie, epigenetische regulatie, transposons, aangeboren immuniteit