Clear Sky Science · nl
Multicomponent synergetische immobilisatie via in-situ en dynamische uitwisselingsstrategieën voor het bouwen van hiërarchische biopharmaca
Waarom het bouwen van slimmere geneesmiddelen ertoe doet
Veel van de krachtigste geneesmiddelen van vandaag zijn grote, fragiele biologische moleculen zoals eiwitten en enzymen. Ze kunnen kanker bestrijden, schadelijke bacteriën doden en het herstel versnellen, maar ze zijn gemakkelijk beschadigbaar en moeilijk op de juiste plek in het lichaam af te leveren. Dit artikel beschrijft een nieuwe manier om meerdere van deze delicate componenten samen te "verpakken" in een beschermend, sponsachtig materiaal, zodat ze achtereenvolgens krachtiger kunnen werken met minder bijwerkingen.
Een kristal veranderen in een moleculair appartementencomplex
De onderzoekers beginnen met een speciaal poreus materiaal gemaakt van metaalionen en kleine organische bouwstenen. Het gedraagt zich een beetje als een klein, flexibel appartementencomplex vol kamers en gangen. Ze tonen aan dat dit raamwerk, een zeolitisch pyrimidine-raamwerk genoemd, rond eiwitten kan groeien zodat de eiwitten beschermd in het kristal terechtkomen. Deze "in-situ" insluiting verplettert of inactiveert de eiwitten niet, en zorgvuldige beeldvorming bevestigt dat ze gelijkmatig door het interieur zijn verdeeld, net als bewoners op elke verdieping van een gebouw.
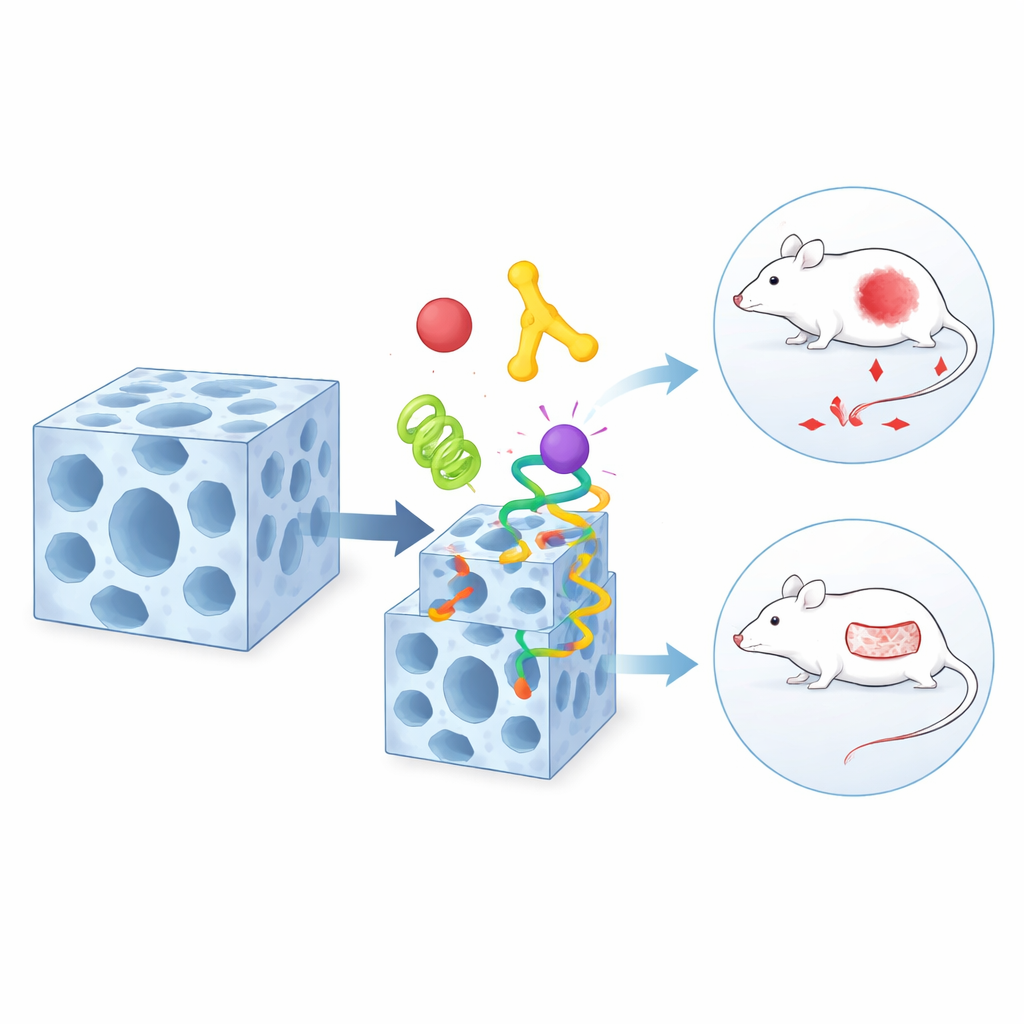
Een vormveranderende gastheer voor oppervlakte-decoratie
Hetzelfde materiaal heeft een verrassende tweede truc: het kan zijn interne structuur reversibel veranderen wanneer het wordt blootgesteld aan bepaalde oplosmiddelen of water. Tijdens deze zachte vormverandering verslappen sommige chemische verbindingen in het raamwerk en vormen zich daarna opnieuw. Het team ontdekte dat bepaalde chemische groepen op eiwitoppervlakken — zoals die in sommige aminozuren — van dit moment van kwetsbaarheid kunnen profiteren. Ze concurreren tijdelijk met de oorspronkelijke bouwblokken van het raamwerk en glippen in nieuw gevormde "defecten" nabij het oppervlak. Daardoor wordt een laag eiwitten voornamelijk aan de buitenkant van het kristal verankerd, terwijl de binnenste eiwitten op hun plaats blijven. Dit dynamische uitwisselingsproces stelt de wetenschappers in staat te bepalen welke componenten diep binnenin wonen en welke de buitenste schil decoreren.
Ontwerpen van enzymatische assemblagelijnen
Met zowel de binnen- als de buitenruimtes onder controle bouwen de auteurs kleine enzymatische "assemblagelijnen." In één voorbeeld wordt een enzym dat suiker omzet in een agressief tussenproduct opgesloten in het raamwerk, terwijl een tweede enzym dat dat tussenproduct veilig afbreekt nabij het oppervlak is bevestigd. Deze binnen–buitenindeling laat de reactie sneller en efficiënter verlopen dan meer traditionele kern–schilontwerpen of willekeurige mengsels van enzymen. Omdat de buitenste enzymen makkelijker door moleculen te bereiken zijn en het schadelijke tussenproduct snel wordt verwijderd, blijft het systeem actief over veel cycli en is het beter bestand tegen warmte, agressieve omstandigheden en herhaald gebruik.
Slimme anti-kanker- en anti-bacteriële pakketten
De echte kracht van deze aanpak blijkt wanneer ze op geneeskunde wordt toegepast. Het team combineert een tumor-gerichte protein, een glucose-etend enzym en een standaard chemotherapeutisch middel in één gelaagd deeltje. De targetende component op het oppervlak leidt het deeltje naar kankercellen, het enzym droogt hun energievoorziening uit door lokale suiker te consumeren, en het klein-molecuul geneesmiddel levert een extra dodelijke klap. Bij muizen met menselijke tumorimplantaten krimpt dit drieledige pakket tumoren veel effectiever dan elk van de componenten alleen of dan eenvoudiger gerangschikte mengsels. In een apart ontwerp passen de auteurs het raamwerk aan voor geïnfecteerde huidwonden door een antibacterieel peptide en een weefsel-remodellerend enzym in verschillende regio's van dezelfde drager te plaatsen. In ratmodellen verminderen deze deeltjes de infectie sterk en versnellen ze het sluiten van moeilijke wonden vergeleken met conventionele behandelingen.

Hoe dit werk de geneeskunde vooruit helpt
Voor een niet-specialist is de kernboodschap dat deze studie één poreus kristal verandert in een programmeerbaar huis voor veel soorten therapeutische moleculen. Door te bepalen wie binnen woont, wie op het oppervlak verblijft en in welke verhouding, kunnen de onderzoekers trap-voor-trap behandelingen orkestreren — eerst richten, dan aanvallen, dan herstellen — binnen één klein object. Deze strategie beschermt niet alleen fragiele biologische geneesmiddelen maar laat ze ook elkaar helpen, wat leidt tot krachtigere, preciezere anti-kanker- en anti-bacteriële therapieën. Dezelfde ontwerpprincipes kunnen worden aangepast voor veel toekomstige "slimme geneesmiddelen" die meerdere componenten nodig hebben om samen te werken op de juiste plek en het juiste moment.
Bronvermelding: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Trefwoorden: metaal-organische netwerken, enzymimmobilisatie, kanker-nanomedicine, wondgenezing, levering van biopharmaca