Clear Sky Science · nl
De extracellulaire matrix bemiddelt clustering van circulerende tumorcellen bij metastase van triple-negatieve borstkanker
Hoe verraderlijke borstkankercellen zich in de bloedbaan organiseren
Wanneer borstkanker uitzaait, komt dat vaak doordat losse kankercellen in de bloedbaan terechtkomen en zich in verre organen nestelen. Deze studie stelt een misleidend eenvoudige vraag met grote gevolgen: hoe slagen de meest agressieve borstkankercellen, die hun gebruikelijke “klittenband” om aan elkaar te blijven plakken zijn kwijtgeraakt, er toch in om in hechte clusters te reizen — en waarom maakt dat hen zo dodelijk?
Een plakkend suikerlaagje als vervanging van het klassieke cel‑lijm
De auteurs richten zich op triple-negatieve borstkanker (TNBC), een bijzonder agressieve vorm die vaak circulerende tumorcellen (CTC’s) produceert. In veel kankers hebben clusters van CTC’s veel meer kans om uitzaaiingen te vormen dan losse cellen. Gewoonlijk worden zulke clusters bijeengehouden door epitheliale adherens junctions — speciale eiwitcomplexen die als moleculaire klinknagels tussen aangrenzende cellen fungeren. Maar TNBC‑cellen verliezen deze junction‑eiwitten vaak, waardoor er een paradox ontstaat: zonder het gebruikelijke plakmiddel, wat houdt hun clusters dan bij elkaar? Door grote kanker‑genbanken te doorzoeken, vonden de onderzoekers dat TNBC‑tumoren verrijkt zijn voor genen die betrokken zijn bij het buitenste geraamte van de cel, de zogenaamde extracellulaire matrix. Een opvallend gen, HAS2, codeert voor een enzym dat hyaluronan (HA) maakt, een lange suikerpolymeer die cellen omhult. Hoge HAS2‑ en HA‑waarden waren sterk gekoppeld aan agressieve, metastatische tumoreigenschappen.
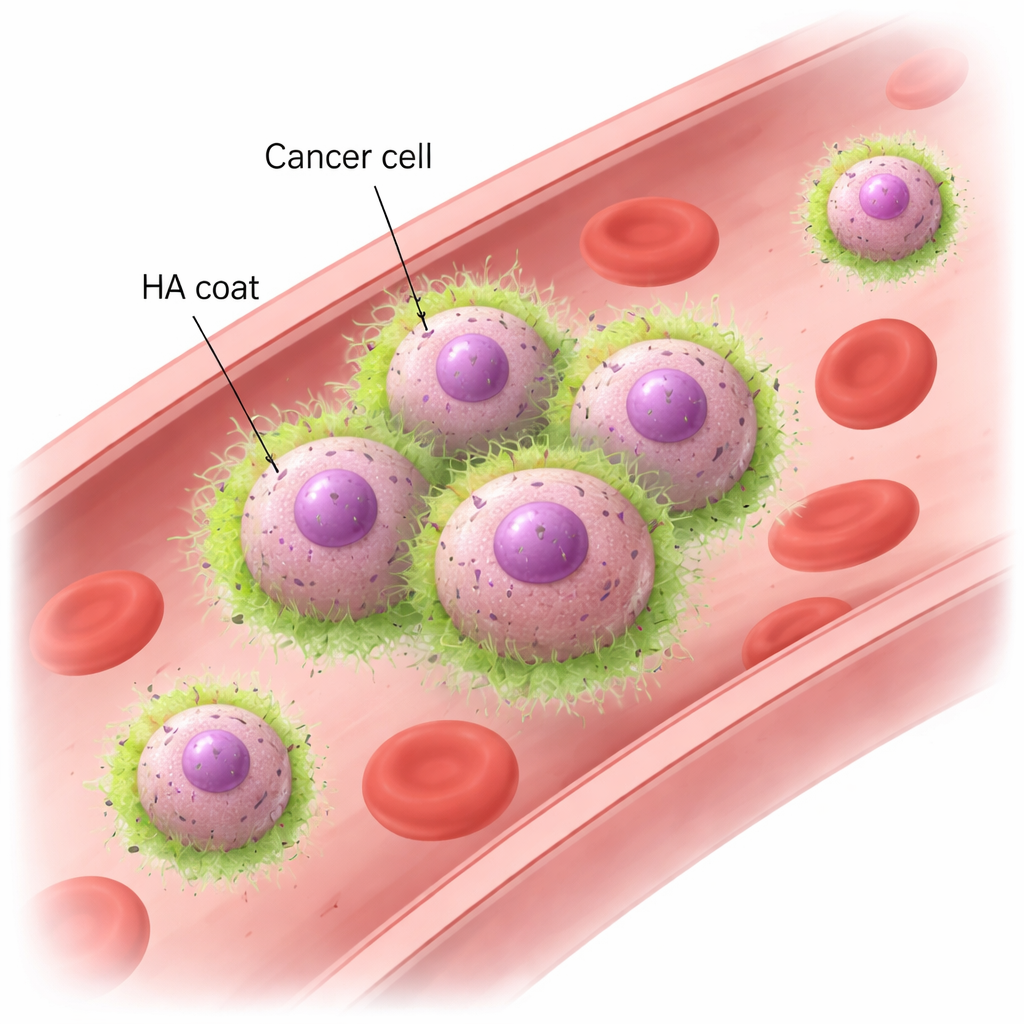
Hyaluronan en CD44: een nieuwe manier waarop cellen elkaars handen vasthouden
Met muismodellen en menselijke borstkankercellijnen toonden de onderzoekers aan dat metastatische TNBC‑cellen snel clusters vormen wanneer ze worden blootgesteld aan ronddraaiende stroming die het bloed nabootst. Deze clusters blijven intact, zelfs bij krachten vergelijkbaar met die in echte bloedvaten, terwijl minder agressieve borstkankercellen uit elkaar vallen en als enkelingen wegdrijven. Microscopen lieten zien dat de metastatische cellen gewikkeld zijn in een HA‑“mantel”, die zich precies concentreert op de plaatsen waar cellen elkaar raken. Het verwijderen van HA met enzymen, of het terugschroeven van HAS2, zorgde ervoor dat de cellen hun vermogen om onder stroming te clusteren verloren, ook al konden ze nog wel samen bezinken wanneer ze ongemoeid werden gelaten. De belangrijkste partner aan de celzijde is CD44, een veelvoorkomende oppervlakte‑receptor die HA bindt. Cellen zonder CD44 konden HA niet langer op hun oppervlak houden of clusters vormen. Omgekeerd kregen niet‑clusterende cellen die werden gemodificeerd om zowel HAS2 als CD44 te produceren een sterk vermogen om te clusteren. Deze experimenten toonden aan dat HA‑interactie met CD44 zowel noodzakelijk als voldoende is om kankercellen in snelstromend bloed aan elkaar te laten plakken.
Fijne uitsteeksels en mechanische sluitingen bouwen sterke clusters
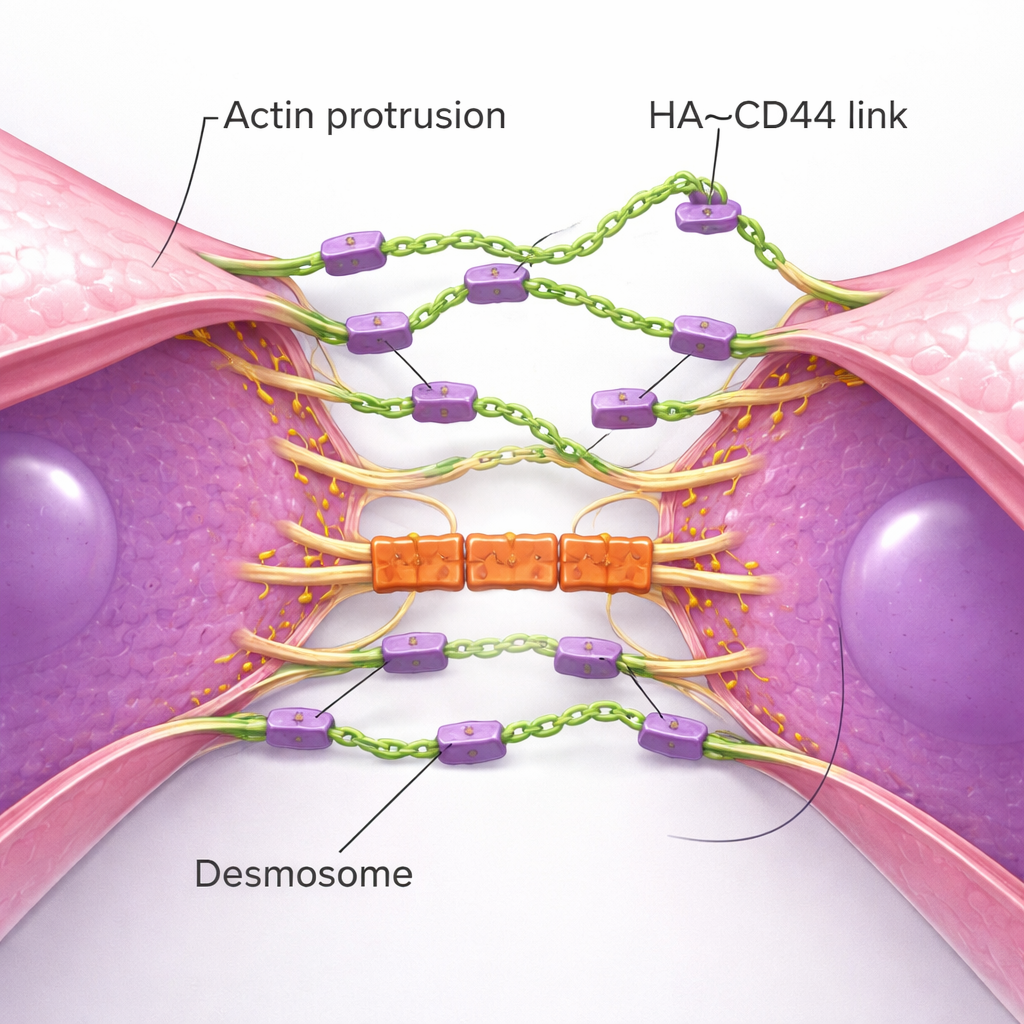
Hogeresolutiebeeldvorming onthulde de fysieke choreografie van hoe clusters ontstaan. Enkelvoudige TNBC‑cellen strekken talrijke dunne, actine‑gebaseerde membraanuitsteeksels uit — als voelers — bezaaid met CD44 en bekroond met HA. Wanneer twee cellen dicht bij elkaar drijven, ontmoeten deze voelers elkaar eerst en vormen ze initiële HA–CD44‑bruggen. In de loop van de tijd glijden de uitsteeksels langs elkaar, trekken de hele cellichamen dichter naar elkaar toe totdat brede gebieden van de membranen bijna naast elkaar liggen. Dit proces weerspiegelt hoe normale epitheliale cellen adherens junctions vormen, maar hier wordt het aangedreven door een flexibele suikerlaag in plaats van stijve proteïneketens. Terwijl de contactzone rijpt, doet een andere reeks structuren mee: desmosomen, robuuste junctions die celmembranen met het interne cytoskelet verbinden. Desmosomale eiwitten hopen zich alleen op nadat HA‑gebaseerd contact is gelegd en fungeren als mechanische “sloten” die helpen dat clusters weerstand bieden aan de scheurende krachten van de bloedstroom. Wanneer desmosomale componenten werden verminderd, vormden clusters zich wel, maar vielen ze bij hogere schuifspanning uit elkaar.
Waarom clustering belangrijk is voor overleving en metastase
Het HA‑gebaseerde clustersysteem bleek meer te zijn dan een manier om bij elkaar te blijven; het verhoogde direct de overleving. Bij langdurige gesimuleerde bloedstroom vertoonden HA‑rijke clusters veel lagere niveaus van schadelijke reactieve zuurstofsoorten en aanzienlijk minder celdood dan HA‑arme losse cellen. In muismodellen produceerden TNBC‑cellen zonder HAS2 veel minder CTC’s, vormden ze slechts kleine clusters en genereerden ze dramatisch minder longmetastasen — ondanks dat hun primaire tumoren even hard groeiden. Wanneer voorgevormde clusters van controlecellen en HAS2‑deficiënte cellen in muizen werden geïnjecteerd, koloniseerden de HA‑arme cellen de longen veel minder succesvol. Bovendien konden HA‑omhulde CTC’s andere cellen ‘aantrekken’ — zowel kankercellen die zelf geen HA hadden als normale immuuncellen zoals neutrofielen — in gemengde clusters, mits die partners CD44 tot expressie brachten. Bloedmonsters van patiënten met metastatische TNBC toonden hetzelfde patroon: CTC’s droegen vaak een HA‑mantel, met HA verrijkt op contactpunten tussen tumorcellen en tussen tumor‑ en niet‑tumorcellen.
Wat dit betekent voor patiënten en toekomstige therapieën
Voor niet‑specialisten is de belangrijkste conclusie dat sommige van de dodelijkste borstkankercellen niet als eenlingen reizen maar als kleine, samenwerkende teams die bijeengehouden worden door een suikerig buitenlaagje en de bijbehorende receptor, in plaats van door de klassieke cel‑cel “klinknagels” die in normale weefsels voorkomen. Dit HA–CD44‑mechanisme helpt tumorcellen om de harde omstandigheden van de bloedstroom te overleven, samen te gaan met andere tumorcellen en ondersteunende bloedcellen, en efficiënter nieuwe tumoren in verre organen te vestigen. Het remmen van HA‑productie (bijvoorbeeld door HAS2 te remmen) of het blokkeren van de interactie met CD44 zou in principe deze clusters kunnen verzwakken en het voor TNBC moeilijker kunnen maken te metastaseren, wat een nieuw aanvalsplan biedt voor toekomstige anti‑metastatische behandelingen.
Bronvermelding: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
Trefwoorden: triple-negatieve borstkanker, circulerende tumorcellen, hyaluronan, CD44, metastase