Clear Sky Science · nl
Escherichia coli bevordert metastase van colorectale kanker door enhancer-promoter-lussen in stand te houden via het vrijkomen van neutrofiele extracellulaire vallen
Darmbacteriën en de geheime snelweg van kanker
Colorectale kanker is vaak dodelijk niet vanwege de oorspronkelijke tumor in de darm, maar omdat kankercellen naar de lever reizen en zich daar vestigen. Deze studie onthult een onverwachte medeplichtige in die reis: een veelvoorkomende darmbacterie, Escherichia coli. Door de keten van gebeurtenissen te volgen van bacteriën in de darm naar agressieve tumoren in de lever, laten de onderzoekers zien hoe microben, immuuncellen en de DNA‑architectuur binnen kankercellen samen kunnen werken om metastase te bevorderen — en wijzen ze op nieuwe manieren om deze keten te doorbreken.
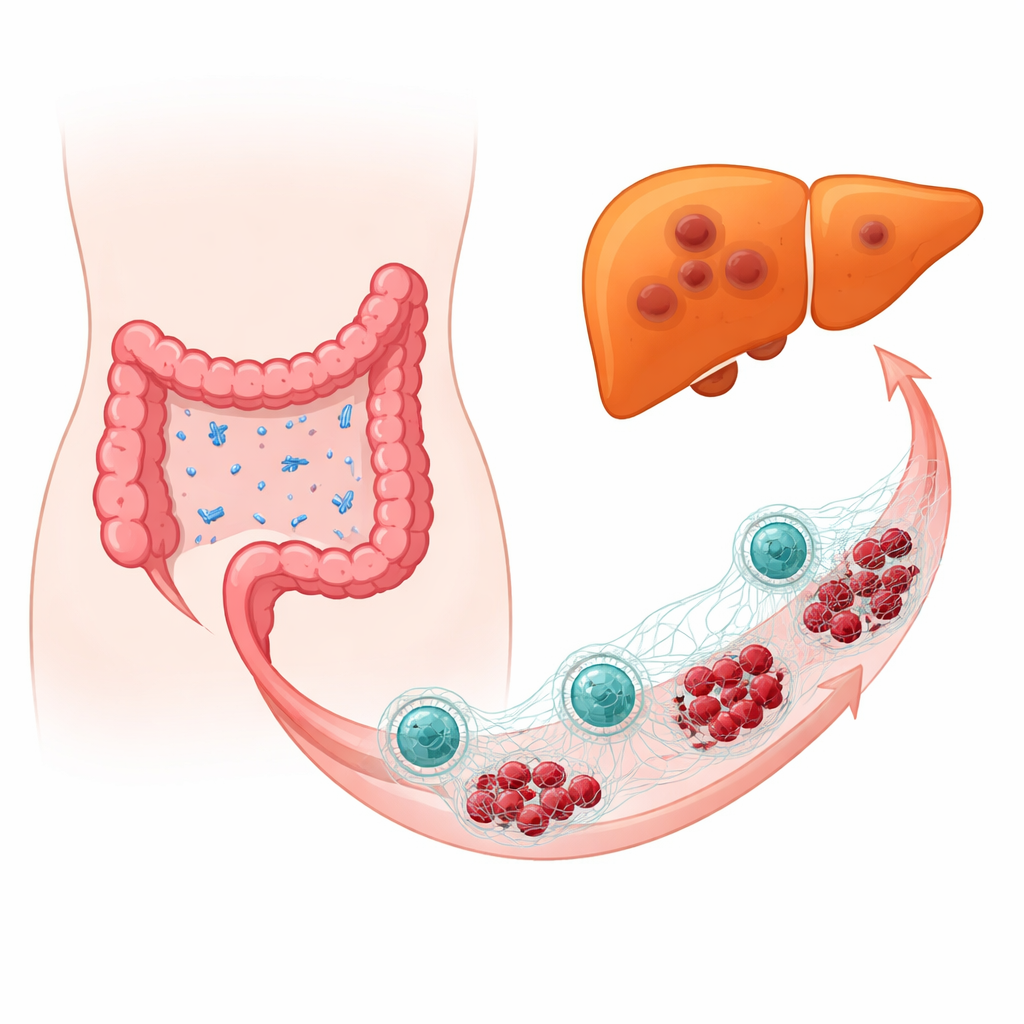
Wanneer vriendelijke bacteriën vijandig worden
Het team onderzocht tumormonsters van mensen met colorectale kanker en vergeleek monsters van patiënten waarvan de kanker naar de lever was uitgezaaid met monsters van patiënten zonder leveruitzaaiingen. Met behulp van hoogresolutie DNA‑gebaseerde microbieel profielonderzoek vonden ze dat E. coli veel meer aanwezig was in kankers die al de lever hadden geïnfiltreerd. In muismodellen en in muizen met gehumaniseerde immuunsystemen leidde het doelbewust toevoegen van E. coli nabij colorectale tumoren tot grotere en frequentere levermetastasen, en zette het tumorcellen aan tot een mobielere, invasievere toestand. Zelfs wanneer het merendeel van de normale darmflora met antibiotica werd verwijderd en alleen E. coli opnieuw werd ingebracht, bevorderde de bacterie nog steeds tumorgroei en -uitzaaiing, wat wijst op een directe rol van E. coli in plaats van een algemene verstoring van het microbioom.
Immuunnetten die kanker helpen ontsnappen
Neutrofielen — de voorste immuuncellen die normaal microben vangen en doden — kwamen naar voren als cruciale tussenschakels. Als reactie op E. coli gaven neutrofielen webachtige structuren vrij, zogenaamde extracellulaire vallen, opgebouwd uit DNA en toxische eiwitten. Deze netten zijn bedoeld om bacteriën te vangen, maar in deze situatie beschermden en versterkten ze onbedoeld kankercellen. Wanneer de onderzoekers de netten afbraakten met enzymen of sleutelenzymen blokkeerden die nodig zijn voor hun vorming, krompen levermetastasen en werden tumoren minder agressief. Het uitputten van neutrofielen had een vergelijkbaar beschermend effect, wat een paradox oplevert: de immuunreactie die infecties bestrijdt, wordt gekaapt om kankeruitzaaiing te helpen.
Van elektrische signalen naar genschakelaars
Hoe konden plakkerige DNA‑netten buiten een tumorcel veranderen wat er diep in de kern gebeurt? Het antwoord lag in calcium, een eenvoudige ion die fungeert als elektrisch signaal in cellen. De studie toonde aan dat neutrofiele netten het niveau van een kanaaleiwit, TRPC1, op colorectale kankercellen verhoogden. TRPC1 liet extra calcium de cel binnenstromen, wat op zijn beurt een calcium‑gevoelige regulator genaamd NFATC3 activeerde en een zelfversterkende lus creëerde die de TRPC1‑niveaus hoog hield. Deze calciuminflux stimuleerde twee kleine eiwitten, S100A8 en S100A9, om aan elkaar te hechten en vervolgens te binden aan een belangrijke groeiregulator, STAT3. Het drietal trok de kern in, waar het iets opvallends deed: het hielp DNA buigen en lussen zodat verre regulatorische gebieden en genstarters elkaar raakten, waardoor de zogenaamde enhancer–promoter‑lussen fysiek gestabiliseerd werden en bepaalde genen sterker werden ingeschakeld.
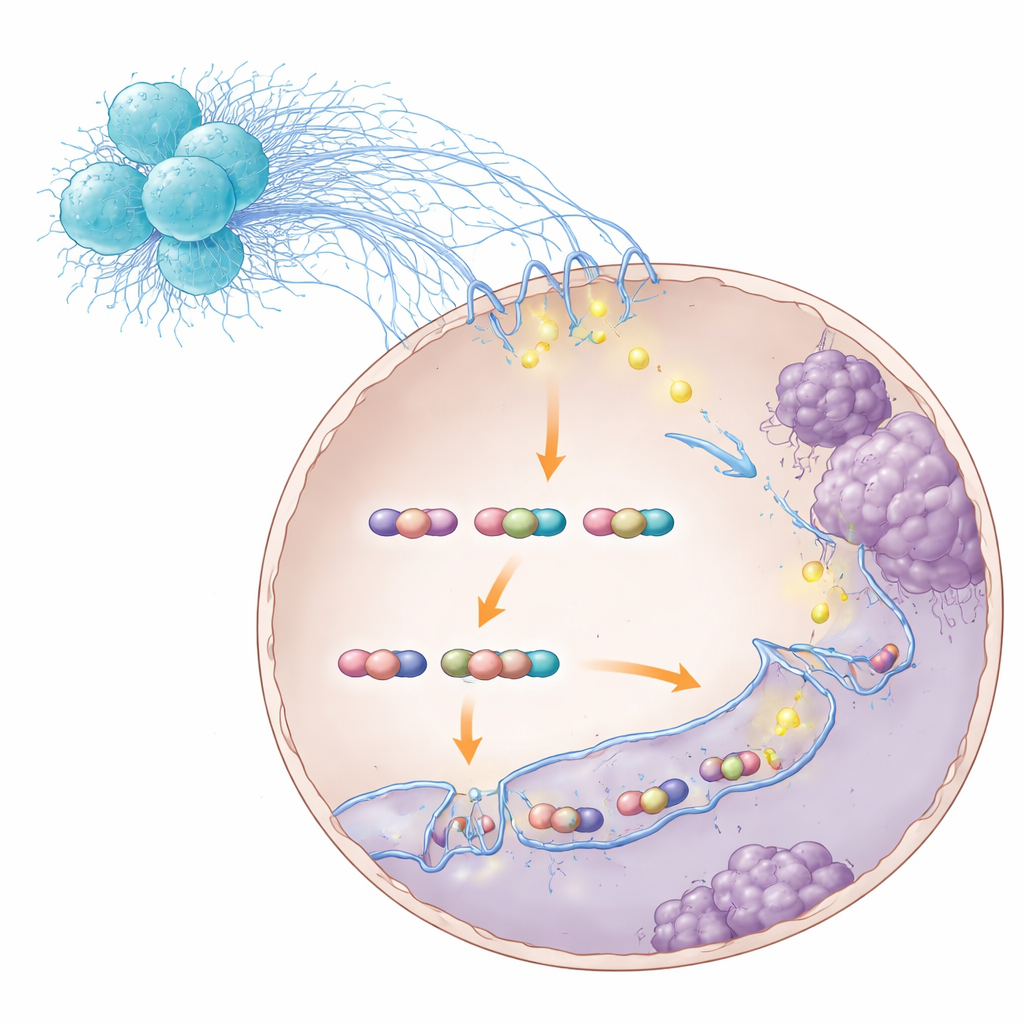
Het herschakelen van kankercellen voor metastase
Door de driedimensionale contacten langs het genoom in kaart te brengen, vonden de onderzoekers dat het STAT3–S100A8/9‑complex lussen bevorderde die genen in de richting van celbeweging en invasie activeerden. Eén opvallend gen was TNS1, dat cellen aanzet hun hechtingen los te laten en makkelijker te migreren. Toen het STAT3–S100A8/9‑complex werd verstoord, verzwakten of verdwenen veel van deze lussen, daalden de TNS1‑niveaus en verloren kankercellen een deel van hun vermogen om te invaseren en de lever te koloniseren. Belangrijk is dat deze verstoring STAT3 niet volledig van DNA afhield — het destabiliseerde specifiek de lusarchitectuur die metastatische programma’s krachtig maakte. In diermodellen verminderde het blokkeren van verschillende stappen in deze keten — van de bacteriële sensorsignaalweg RIPK2 in neutrofielen, tot S100A8/9, tot STAT3 zelf — de levermetastase en verbeterde het de overleving.
De keten tussen microben en tumoren doorbreken
Voor niet‑specialisten is de kernboodschap dat een veelvoorkomende darmbacterie kan helpen colorectale kanker te laten uitzaaien door eerst immuuncellen aan te zetten DNA‑netten te werpen, en vervolgens die netten te gebruiken om een calcium‑gestuurde keten op gang te brengen die de manier waarop kankergenen worden ingeschakeld, herbedraadt. In plaats van te vertrouwen op brede antibiotica, die nuttige microben kunnen beschadigen en kankerimmunotherapie kunnen ondermijnen, wijst dit werk op meer gerichte medicinale doelwitten: bacteriële sensors zoals RIPK2, de TRPC1–calcium–S100A8/9‑cascade en de STAT3‑gedreven DNA‑lussen die metastaserelated genen op volle kracht zetten. Het onderbreken van deze keten op één of meerdere punten zou een nieuwe strategie kunnen bieden om te voorkomen dat colorectale kanker een lokaal probleem in de darm verandert in een dodelijke ziekte in de lever.
Bronvermelding: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Trefwoorden: uitzaaiing van colorectale kanker, darmmicrobioom, neutrofiele extracellulaire vallen, STAT3-signaalweg, epigenetische genregulatie