Clear Sky Science · nl
Ontwerp van covalente remmers geeft activiteit tegen zowel GDP- als GTP‑gebonden vormen van KRAS G12C
Waarom dit ertoe doet voor toekomstige kankerbehandelingen
Kankers die worden aangedreven door mutaties in het gen KRAS gelden al lange tijd als enkele van de moeilijkst behandelbare. Recentelijk zijn nieuwe geneesmiddelen die één veelvoorkomende mutante vorm, KRAS G12C, uitschakelen bij patiënten gekomen en hebben ze dat beeld gedeeltelijk veranderd. Dit artikel onderzoekt een nog ambitieuzer idee: kunnen we geneesmiddelen ontwerpen die KRAS G12C in beide belangrijkste werkmodi in de cel blokkeren, en zou dat de behandeling van kanker sneller, krachtiger of duurzamer maken?
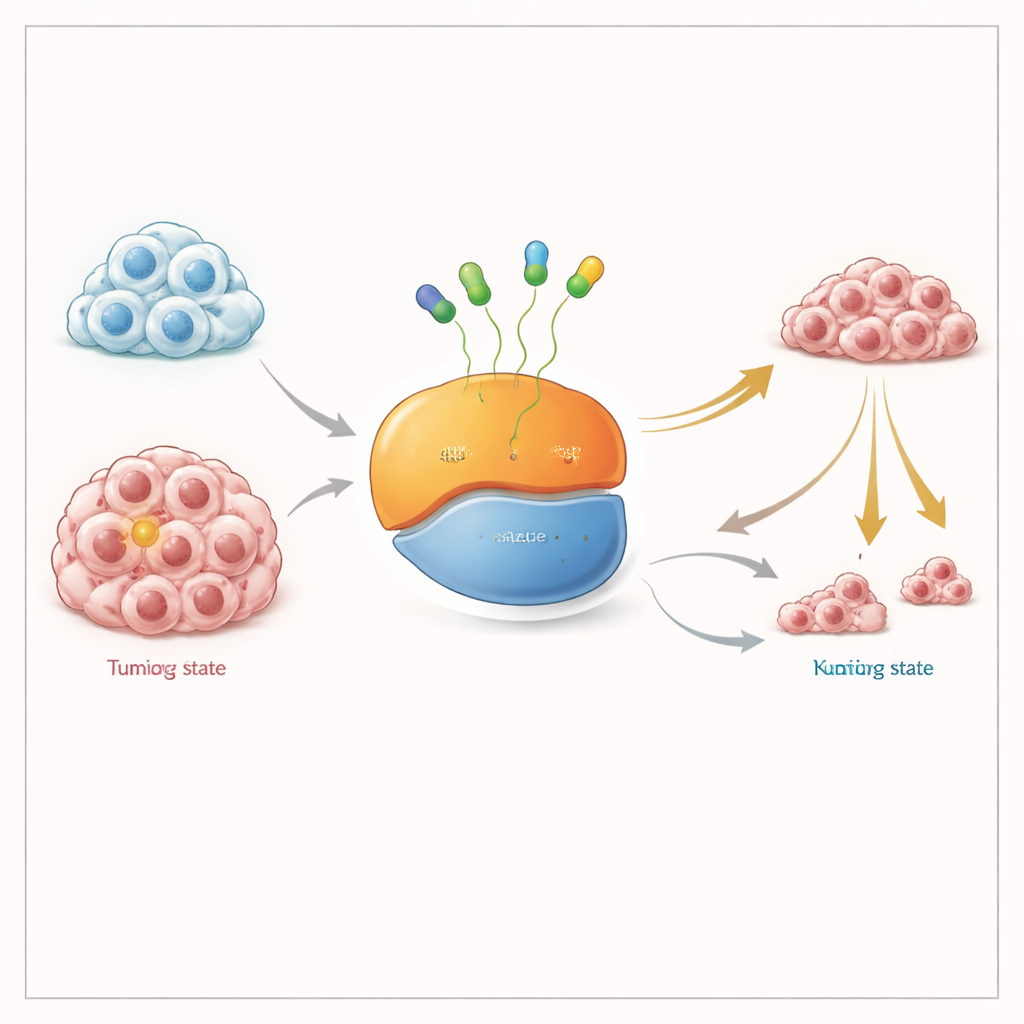
Een moleculaire lichtschakelaar uitschakelen in twee posities
KRAS werkt als een klein aan‑/uitschakelaartje voor groeisignalen in de cel. Het wisselt tussen een „uit”‑toestand, waarin het het ene energiedragende molecuul (GDP) draagt, en een „aan”‑toestand, waarin het een ander draagt (GTP). De KRAS G12C‑mutatie houdt deze schakelaar gedeeltelijk aan en voedt zo tumorgroei. Bestaande door de FDA goedgekeurde middelen hechten zich aan de „uit”‑vorm en vergrendelen die; na verloop van tijd, naarmate meer KRAS door die vorm cycled, wordt het totale reservoir van mutant eiwit uitgeschakeld. Veel onderzoekers hebben betoogd dat een middel dat KRAS in zowel de aan‑ als uit‑vorm kan grijpen beter zou moeten werken, vooral in tumoren die zich aanpassen door meer KRAS in de aan‑toestand te houden.
Ontwerpen van een nieuw soort moleculaire haak
De auteurs stelden zich ten doel zulke dubbelwerkende middelen te bouwen. Ze concentreerden zich op een klein groefje nabij een flexibele regio van KRAS die Switch II wordt genoemd, waar huidige middelen al binden. In plaats van te veranderen hoe strak hun moleculen in dat groefje pasten, herontwierpen ze het „warhead”-deel dat een permanente chemische binding vormt met de mutante cysteïne op positie 12. Via computermodellering en synthese van tientallen varianten ontdekten ze een speciale driedelige warhead die de cysteïne vanuit een iets andere hoek benadert. Deze subtiele verschuiving schept genoeg ruimte voor het omvangrijkere GTP‑molecuul, waardoor de nieuwe verbindingen aan KRAS kunnen binden ongeacht of het GDP of GTP draagt. Biochemische tests bevestigden dat leidende verbindingen de interactie van KRAS met een belangrijke signaalpartner, RAF, in beide toestanden konden verstoren.
Zien hoe het eiwit zichzelf hervormt
Om te begrijpen waarom deze moleculen werkten, bepaalde het team kristalstructuren met hoge resolutie van het geneesmiddel gebonden aan KRAS. Deze momentopnames toonden dat de nieuwe warhead reageert op een ongebruikelijke plaats op het chemische raamwerk, waarbij een fluoride‑atoom losbreekt en een covalente binding vormt op een ander koolstofatoom dan gebruikelijk is bij kankerremmers die cysteïnes targeten. Deze gewijzigde chemie helpt het middel in het Switch II‑pocket te passen, zelfs wanneer GTP aanwezig is. De structuren onthulden ook dat wanneer de remmer bindt, hij een klein watermolecuul verschuift en subtiel een andere lus, Switch I, herschikt, die normaal gesproken contact maakt met downstream signaaleiwitten. Deze allosterische hervorming trekt twee aminozuren dichter naar elkaar om een sterke zoutbrug te vormen, waardoor het oppervlak vervormt en RAF niet langer kan aanliggen en groeisignalen kan doorgeven.
Snelle uitschakeling, maar geen sterkere langetermijneffecten
Gewapend met deze structurele inzichten verfijnden de onderzoekers twee leidende moleculen die efficiënt en selectief aan KRAS G12C hechten, terwijl ze grotendeels andere eiwitten met cysteïnes spaarden. In kankercellijnen blokkeerden deze dubbeltoestandremmers snel een belangrijke signaaloverdrachtsketen, bekend als het MAPK‑pad, gemeten door verlies van een chemische markering op het ERK‑eiwit en sterke onderdrukking van celgroei. Ze inactiveren KRAS in cellen sneller dan een referentiegeneesmiddel dat alleen de inactieve toestand target. In muismodellen met tumoren toonde één leidende verbinding goede orale beschikbaarheid, vormde snel covalente bindingen met het doelwit en deed tumoren krimpen of vertraagde hun groei. Toch, wanneer het team dubbeltoestand‑ en inactieve‑toestandmiddelen over langere tijd vergeleek, bereikten beide klassen uiteindelijk vergelijkbare niveaus van KRAS‑uitschakeling, padonderdrukking en tumorgroeicontrole.
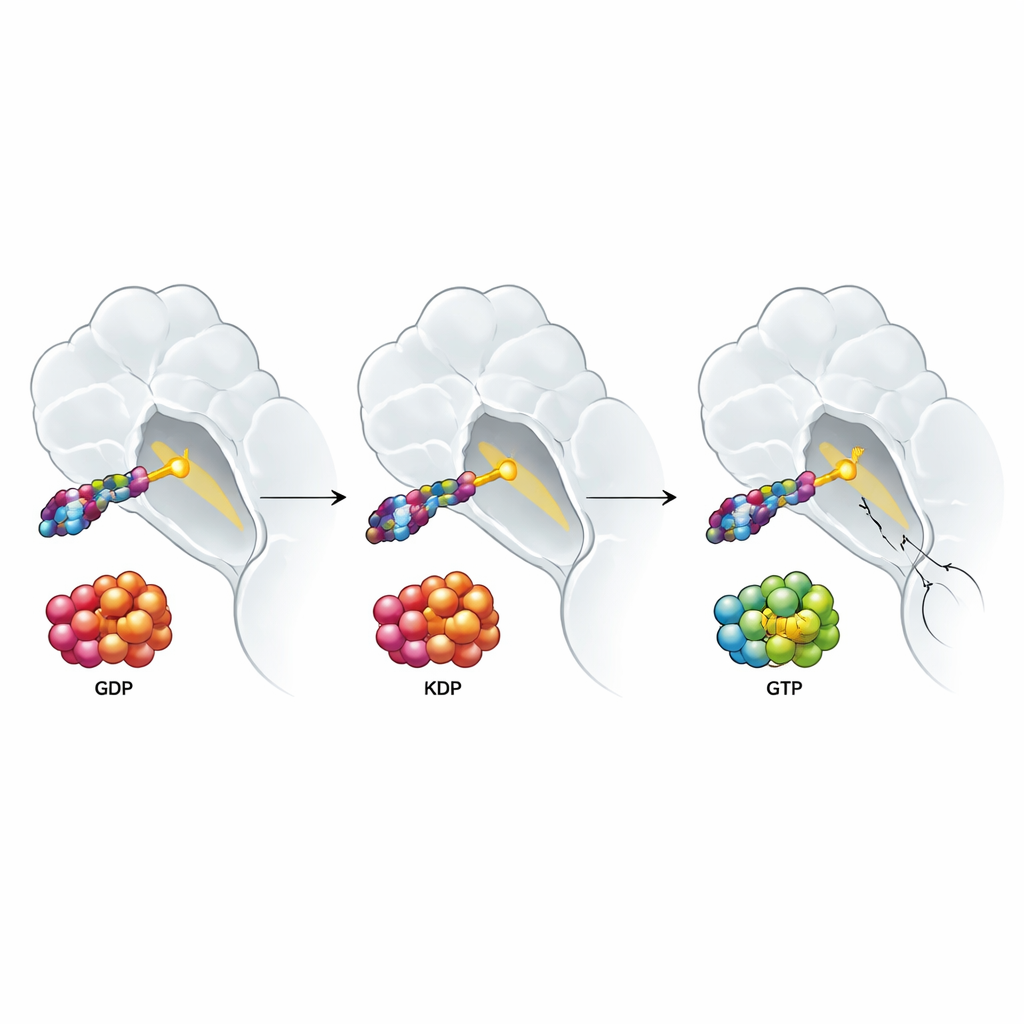
Waarom groeisignalen uit de tumoromgeving toch winnen
De studie onderzocht ook hoe signalen uit de tumoromgeving deze middelen beïnvloeden. Groeifactoren zoals EGF en HGF, die rond veel tumoren overvloedig zijn, duwen RAS‑eiwitten richting de actieve GTP‑geladen vorm en staan erom bekend dat ze reacties op gerichte therapieën verzachten. Men zou verwachten dat een middel dat zich aan de actieve vorm van KRAS G12C bindt dit probleem kan omzeilen. In plaats daarvan vonden de auteurs dat zowel dubbeltoestand‑ als inactieve‑toestandremmers aan kracht verloren wanneer dergelijke groeifactoren aanwezig waren. Gedetailleerde experimenten wezen op een verrassende schuldige: activatie van de normale, niet‑gemuteerde vormen van RAS (H‑RAS en N‑RAS), die KRAS G12C kunnen omzeilen en de groeisignalen laten doorgaan. Toen de onderzoekers H‑RAS en N‑RAS verwijderden in een longkankercellijn, verdween de door groeifactoren aangedreven resistentie grotendeels voor alle soorten KRAS G12C‑gerichte middelen, terwijl een geneesmiddel dat een downstream stap in het pad blokkeert in de eerste plaats minder werd beïnvloed.
Wat dit betekent voor patiënten en geneesmiddelenontwikkeling
Samengevat laat het werk zien dat het chemisch en structureel haalbaar is om covalente KRAS G12C‑middelen te bouwen die het eiwit in zowel zijn aan‑ als uit‑toestand grijpen, en dat deze dubbeltoestandremmers signalering sneller kunnen stilleggen dan bestaande middelen. De snelle betrokkenheid vertaalde zich echter niet duidelijk naar betere tumorgroei‑controle of een oplossing voor door groeifactoren aangedreven resistentie in preklinische modellen. Voor patiënten suggereert dit dat het simpelweg toevoegen van activiteit tegen de actieve KRAS‑vorm mogelijk niet voldoende is; combinatiestrategieën die ook andere RAS‑familieleden of downstream signaalpunten aanpakken, kunnen nodig zijn. De nieuwe warhead en het structurele stappenplan dat hier wordt gepresenteerd, breiden desalniettemin de gereedschapskist voor targeting van KRAS uit en zullen toekomstige generaties van precisiekankertherapieën informeren.
Bronvermelding: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
Trefwoorden: KRAS G12C, covalente remmer, remming in twee toestanden, MAPK‑signaaltransductie, drugresistentie