Clear Sky Science · nl
Door microbiota geïnduceerde EI24 verbetert homeostase maar belemmert de functie van alveolaire macrofagen via metabole regulatie
Waarom kleine longwachters ertoe doen
Elke ademhaling brengt niet alleen zuurstof in je longen, maar ook stof, microben en andere indringers. Patrouillerend op deze grens staan alveolaire macrofagen—gespecialiseerde immuuncellen die afval insluiten en helpen bij het afweren van infecties en kanker. Deze studie onthult een verrassende manier waarop onze alledaagse microben deze cellen "trainen": een molecule genaamd EI24, aangezet door de microbiota, houdt de longwachten stabiel en rustig, maar ten koste van hun vermogen om virussen en tumoren effectief te bestrijden. Begrijpen van deze afweging kan nieuwe wegen openen voor veiligere, effectievere immunotherapieën.
Maak kennis met de vaste schoonmakers van de long
Alveolaire macrofagen zitten in de kleine luchtzakjes van de longen waar gasuitwisseling plaatsvindt. Ze leven daar jaren, vernieuwen zichzelf en ruimen stilletjes surfactant, dode cellen en losse deeltjes op, terwijl ze onnodige ontsteking vermijden die het kwetsbare weefsel zou beschadigen. De auteurs richtten zich op een eiwit genaamd EI24, eerder gekoppeld aan celstressreacties en cellulaire recycling, maar niet goed begrepen in longimmuniteit. Ze ontdekten dat van de vele soorten weefselmacrofagen in het lichaam juist de alveolaire macrofagen uitzonderlijk hoge niveaus van EI24 tot expressie brengen, wat suggereert dat dit eiwit cruciaal kan zijn voor het leven aan het blootgestelde longoppervlak.
Stabiliteit versus kracht bij longverdedigers
Om te onderzoeken wat EI24 precies doet, fokten de onderzoekers muizen die dit eiwit specifiek in macrofagen misten. Deze dieren ontwikkelden zich normaal en produceerden normale aantallen jonge macrofaagvoorlopers in de long, maar naarmate ze rijpten verdween ongeveer de helft van hun alveolaire macrofagen. De overgebleven cellen toonden duidelijke tekenen van verhoogde celdood aangedreven door een klassieke doodsenzym, caspase-3. Toch waren deze minder talrijke resterende cellen niet zwak: ze vertoonden een meer "on-duty" profiel, met hogere opname van bacteriën in laboratoriumtesten en sterkere productie van ontstekingsmoleculen bij stimulatie. Genetische en chromatine-analyses toonden aan dat honderden genen betrokken bij antigeenpresentatie, celvernietiging en ontstekingsreacties omhoog werden gezet, terwijl regulerende paden die normaal activatie in toom houden werden versoepeld.
Opgepepte stofwisseling met een verborgen prijs
Dieper gravend vonden de onderzoekers dat EI24-deficiënte macrofagen hun metabolisme hadden herbedraad. In plaats van voornamelijk te steunen op een rustige, energiezuinige toestand, lieten ze hogere niveaus zien van zowel suiververbranding (glycolyse) als mitochondriale energieproductie. Deze opgevoerde energiepaden hielpen sterkere ontstekingsreacties en een krachtiger inslikken van microben en kankercellen te voeden. Maar deze metabole overdrive verhoogde ook reactieve zuurstofbijproducten in de mitochondriën, die op hun beurt caspase-3 activeerden en de cellen naar geprogrammeerde dood dreven. Het blokkeren van deze metabole paden of het opruimen van de reactieve moleculen verminderde zowel de overtollige ontsteking als de neiging tot celdood, waarmee het energiegebruik, de dodelijkheid en de levensduur van de cel aan elkaar werden gekoppeld.
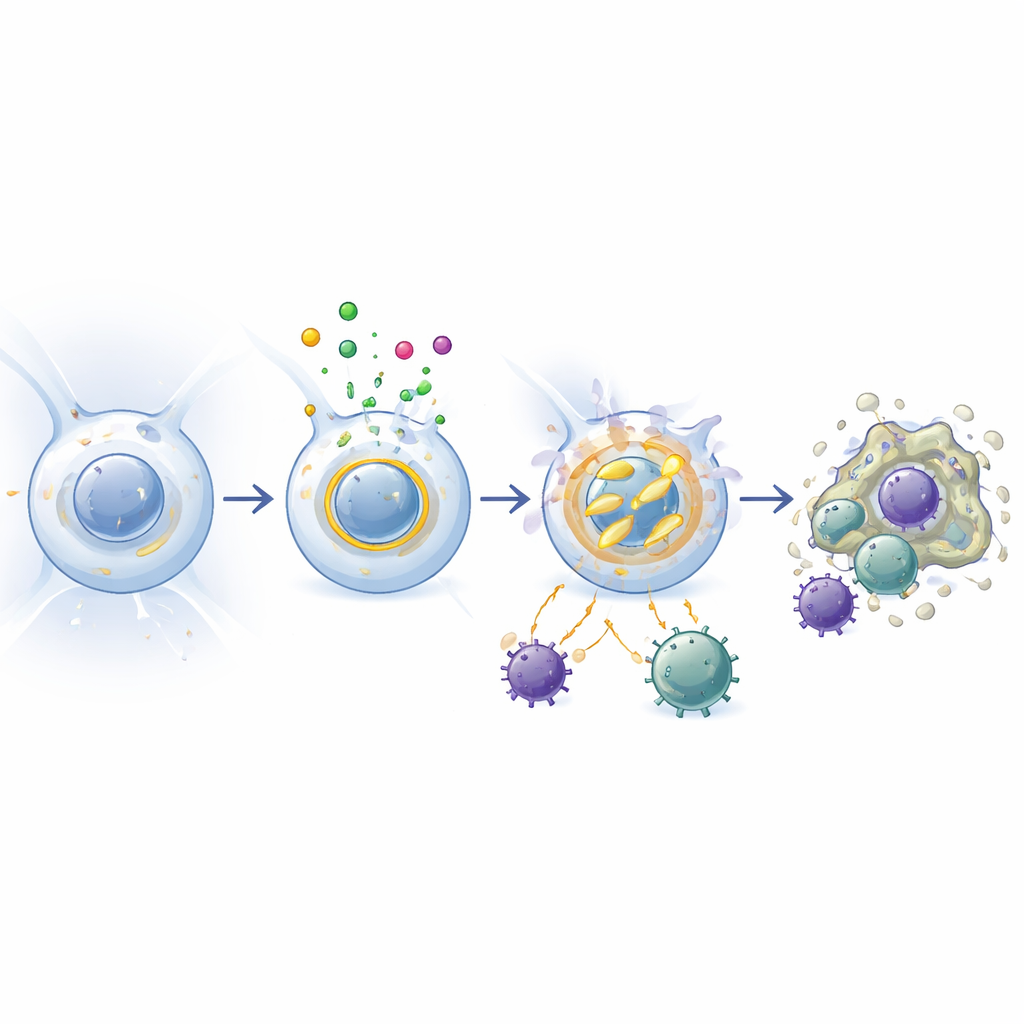
Hoe vriendelijke microben het volume regelen
De long is geen afgesloten kamer; hij komt voortdurend in contact met onschadelijke en gunstige microben uit de lucht en uit de darm. De onderzoekers vergeleken normale muizen met kiemvrije dieren die zonder microben waren opgegroeid. In kiemvrije muizen maakten alveolaire macrofagen veel minder EI24, en het verwijderen van EI24 had weinig invloed op hun aantallen of gedrag. Toen deze kiemvrije muizen later aan normale microben werden blootgesteld, verhoogden hun longmacrofaagjes EI24. Experimenten met microbiale sensorroutes toonden aan dat signalen gedetecteerd door Toll-like receptors 2 en 4—moleculaire "deurbelletjes" voor bacteriële componenten—verantwoordelijk waren voor deze toename. In feite zet de microbiota alveolaire macrofagen in een meer stabiele, minder reactieve staat door EI24 op te voeren, wat helpt de rust te bewaren in een omgeving die anders constante immuunalarmen zou ervaren.
EI24 verlagen om therapie te versterken
Ondanks dat ze minder macrofagen hadden, waren muizen zonder EI24 in deze cellen beter beschermd tegen ernstige influenza-infectie en experimentele longmetastasen van melanoom. Ze ruimden virus efficiënter op, produceerden meer antivirale interferonen in de luchtwegen, en hun macrofagen namen tumorcellen gemakkelijker op. Belangrijk is dat deze dieren geen chronische longschade of verlies van longfunctie ontwikkelden, wat suggereert dat het selectief verwijderen van EI24 de afweer kan versterken zonder duidelijke schade op korte tot middellange termijn. Het team toonde ook aan dat beenmergafgeleide macrofagen die zodanig waren geconstrueerd dat ze EI24 misten effectiever waren wanneer ze in andere muizen werden overgedragen, en normale macrofagen overtroffen in het beperken van zowel virusinfectie als tumorverspreiding in de longen.
Wat dit betekent voor toekomstige behandelingen
Voor een algemeen publiek is de kernboodschap dat onze permanente microben helpen longimmuuncellen in leven en rustig te houden door EI24 aan te zetten—maar dat hetzelfde veiligheidsmechanisme de capaciteit van die cellen om infecties en kanker te bestrijden kan verzwakken. Door EI24 zorgvuldig terug te draaien, kunnen wetenschappers macrofagen in een energieker, agressiever stadium duwen dat virussen en kankercellen beter elimineert, terwijl de algehele longgezondheid in experimentele dieren behouden blijft. Dit werk suggereert dat het richten op EI24, of op de metabole circuits die het regelt, op een dag macrofaaggebaseerde therapieën krachtigere bondgenoten tegen luchtweginfecties en metastatische kanker kan maken.
Bronvermelding: Huang, Y., Su, M., Zhang, Y. et al. Microbiota-induced EI24 improves homeostasis but impedes function of alveolar macrophages via metabolic regulation. Nat Commun 17, 2227 (2026). https://doi.org/10.1038/s41467-026-69000-3
Trefwoorden: alveolaire macrofagen, longimmuniteit, microbiota, macrofaagmetabolisme, kanker- en virusverdediging