Clear Sky Science · nl
Covalente modificatie van een glutaminezuur geïnspireerd op HaloTag-technologie
Proteïne-"ankers" veranderen in medicijndoelen
Veel moderne kankertherapieën werken door zich vast te hechten aan eiwitten in onze cellen. Maar sommige van de meest belangrijke eiwitten bieden geen gemakkelijke "grepen" voor geneesmiddelen. Deze studie introduceert een slimme chemische truc, geïnspireerd op een veelgebruikt laboratoriuminstrument genaamd HaloTag, om zich vast te zetten op een normaal moeilijk bereikbare plek op een eiwit dat groeisignalen relevant voor kanker reguleert. Het werk zou nieuwe wegen kunnen openen naar geneesmiddelen die tumorgedreven routes op een duurzamere manier uitschakelen.
Waarom de meeste covalente middelen op dezelfde plek mikken
In de afgelopen jaren zijn zogenoemde gerichte covalente geneesmiddelen een spannende klasse medicijnen geworden. Ze dragen een licht reactieve chemische groep die een permanente binding vormt met een specifiek aminozuur op een eiwit, waardoor het geneesmiddel op zijn plaats wordt vergrendeld. Bijna al deze middelen richten zich op cysteïne, een relatief zeldzaam maar zeer reactief aminozuur. Daarentegen zijn twee andere aminozuren, aspartaat en glutamaat, veel vaker voorkomend en vaak cruciaal voor de vouwing en functie van een eiwit, maar hun zure "carboxylaat"-groepen zijn veel minder reactief in de waterige omgeving van een cel. Dat maakt selectieve modificatie lastig, en er bestonden maar enkele succesvolle voorbeelden van covalente middelen gericht op glutamaat of aspartaat vóór dit werk.
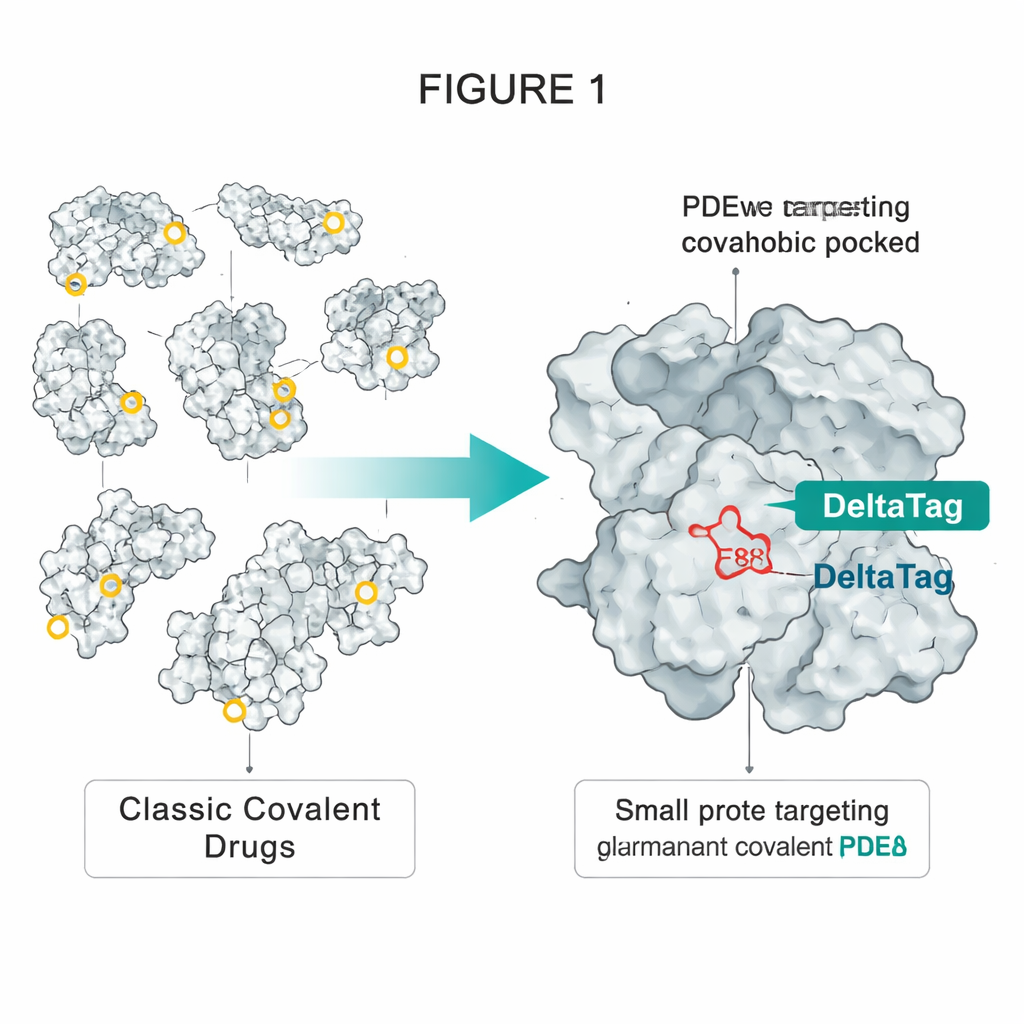
Een truc lenen van HaloTag-technologie
De auteurs lieten zich inspireren door HaloTag, een veelgebruikt gemodificeerd eiwit dat permanent gemerkt kan worden met fluorescente kleurstoffen. In HaloTag reageert een speciaal gepositioneerd aspartaat diep in een hydrofobe pocket met een eenvoudige chloroalkaanketen op de kleurstof en vormt zo een stabiele esterbinding. Het team merkte op dat een ander eiwit, PDEδ, een enigszins vergelijkbare hydrofobe pocket heeft met een enkel toegankelijk glutamaat, E88 genoemd. PDEδ transporteert lipide-gemodificeerde signaalproteïnen zoals het kleine GTPase Rheb door de cel en helpt ze membranen te bereiken waar groeibevorderende complexen zoals mTORC1 worden geactiveerd. Eerdere niet-covalente remmers van PDEδ konden deze shuttle blokkeren, maar hun effect was beperkt omdat een ander eiwit, Arl2, ze na verloop van tijd uit de pocket kan losschudden.
Ontwerpen van DeltaTag om zich aan glutamaat vast te zetten
Om dit "uit-schop"-probleem te omzeilen, begonnen de onderzoekers bij een bekende hoge-affiniteitsremmer van PDEδ en herontwierpen ze een van de zijketens zodat deze een haloalkaan "warhead" droeg, vergelijkbaar met die in HaloTag-liganden. Door meerdere rondes van structurele bijstelling, geleid door eiwitkristalstructuren, kwamen ze uit op een verbinding die DeltaTag heet. De belangrijkste eigenschap is een fenethielbromidegroep die zo is gepositioneerd dat, zodra het molecuul zich in de lipidepocket van PDEδ nestelt, het bromide precies is uitgelijnd om te reageren met E88. Biofysische metingen en hoogresolutie röntgenstructuren bevestigden dat DeltaTag een covalente esterverbinding vormt specifiek met dit glutamaat en dat andere mogelijk reactiever aminozuren op PDEδ ongemoeid blijven. De verbinding is reactief genoeg om het eiwit efficiënt te labelen, maar voldoende stabiel in water en in aanwezigheid van de belangrijkste zwavelhoudende antioxidant van de cel, glutathion, om wijdverspreide, niet-specifieke schade te vermijden.
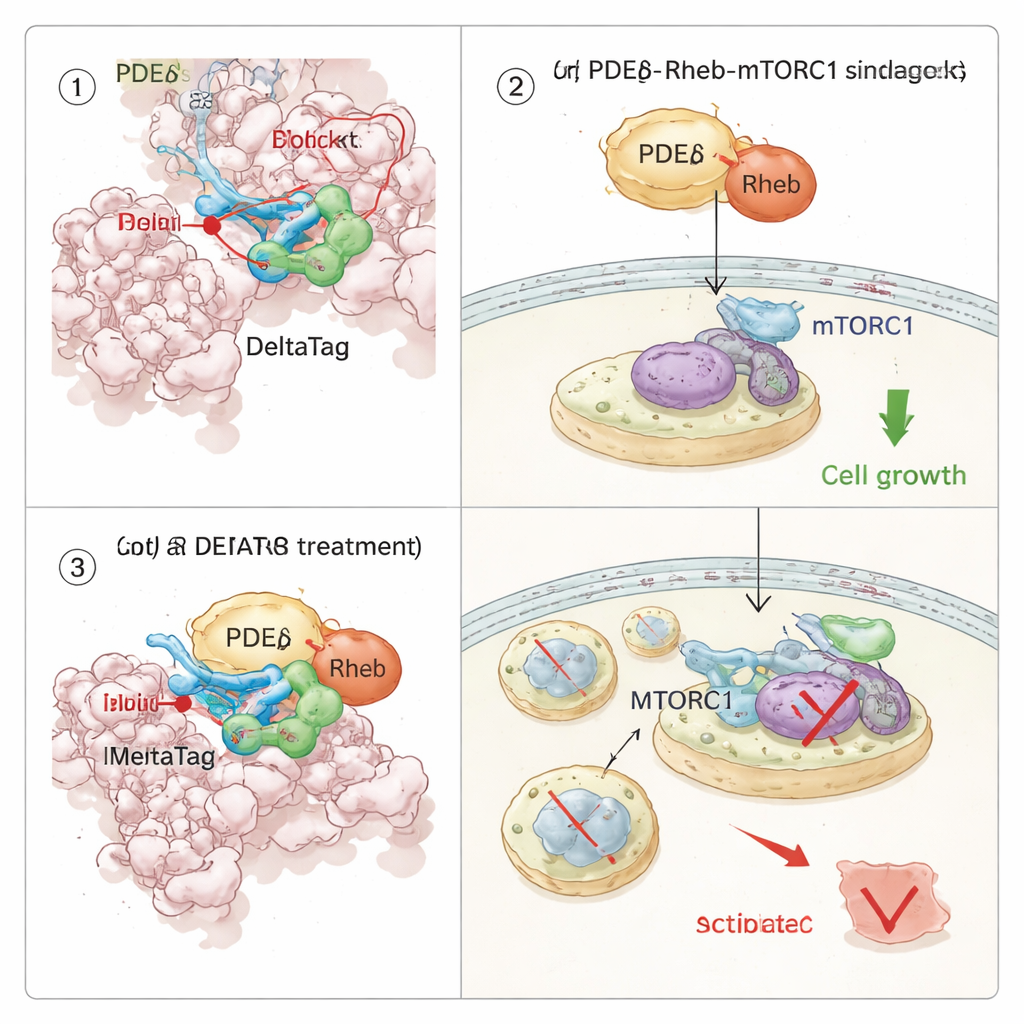
Herschakelen van een groeipad binnen kankercellen
Aangezien PDEδ Rheb chaperonneert, en Rheb op zijn beurt het mTORC1-groeipad inschakelt, onderzochten de onderzoekers hoe covalente remming van PDEδ zich door de signaalroutes van de cel zou verspreiden. Met thermische stabiliteitsprofilering over duizenden eiwitten toonden ze aan dat DeltaTag selectief aan PDEδ bindt in celextracten en eiwitten beïnvloedt die gekoppeld zijn aan de Rheb–mTOR-as. In live-celbeeldvormingsexperimenten veroorzaakte DeltaTag dat Rheb zich verplaatste van een diffuse verdeling in het celinterieur naar meer gebundelde interne membranen, consistent met verstoring van zijn normale shuttling. Globale fosfoproteomica en gerichte Western blots lieten zien dat de activiteit van mTORC1, gevolgd via fosforylering van een ribosomaal eiwit genaamd S6, in de loop van de tijd afnam, terwijl compenserende signalen in verwante paden toenamen. Belangrijk is dat in meerdere menselijke kankercellijnen aangedreven door mutant KRAS en afhankelijk van sterke mTOR-signalen, DeltaTag de celproliferatie effectiever vertraagde dan nauw verwante reversibele remmers, en dat het effect minder sterk was in cellen zonder PDEδ, wat ondersteunt dat de belangrijkste werking on-target is.
Een deur openen naar nieuwe soorten medicijndoelen
Dit werk laat zien dat het mogelijk is kleine moleculen te ontwerpen die een permanente, zeer specifieke binding vormen met één enkel glutamaat dat begraven ligt in een hydrofobe pocket van een eiwit, met behulp van relatief eenvoudige haloalkaanchemie geleend van HaloTag. In het modelstelsel PDEδ levert die covalente verbinding een duurzamere blokkade van een kankergeassocieerd groeipad op dan eerdere reversibele geneesmiddelen. Breder gezien kan dezelfde ontwerplogica worden toegepast op andere eiwitten met hydrofobe holtes die de gebruikelijke "reactieve" aminozuren missen, zolang ze een strategisch geplaatst glutamaat of aspartaat presenteren. Met verdere optimalisatie kunnen glutamaat-gerichte covalente remmers zoals DeltaTag nuttige instrumenten voor chemische biologie worden en uiteindelijk leidende verbindingen voor nieuwe therapieën die momenteel moeilijk te bestrijden eiwitten aanpakken.
Bronvermelding: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
Trefwoorden: covalente remmers, gericht op glutamaat, PDEδ, mTOR-signaaltransductie, ontwerp van kankergeneesmiddelen