Clear Sky Science · nl
Ontwerpen van synthetische cellen met intramembraandomeinen die verschillende tweelaagse asymmetrieën bezitten
Waarom piepkleine synthetische belletjes ertoe doen
Elke levende cel is omgeven door een membraan dat zich gedraagt als een slimme, flexibele huid. Deze huid is niet uniform: de binnen- en buitenzijde, en zelfs verschillende stukken over het oppervlak, kunnen heel verschillende samenstellingen en vormen hebben. Die verschillen helpen cellen signalen te sturen, eiwitten te binden en zich zelfs te delen. Toch is het opvallend moeilijk geweest om eenvoudige, bestuurbare modelmembranen te maken die die complexiteit vangen. Deze studie introduceert een praktische manier om celformaat “synthetische cellen” te maken waarvan de membranen asymmetrisch zijn aan beide zijden en lateraal gepatroneerd in verschillende regio’s—en opent zo een route naar realistischere celimitaties en naar het bestuderen van hoe membraanpatronen budding en deling aansturen. 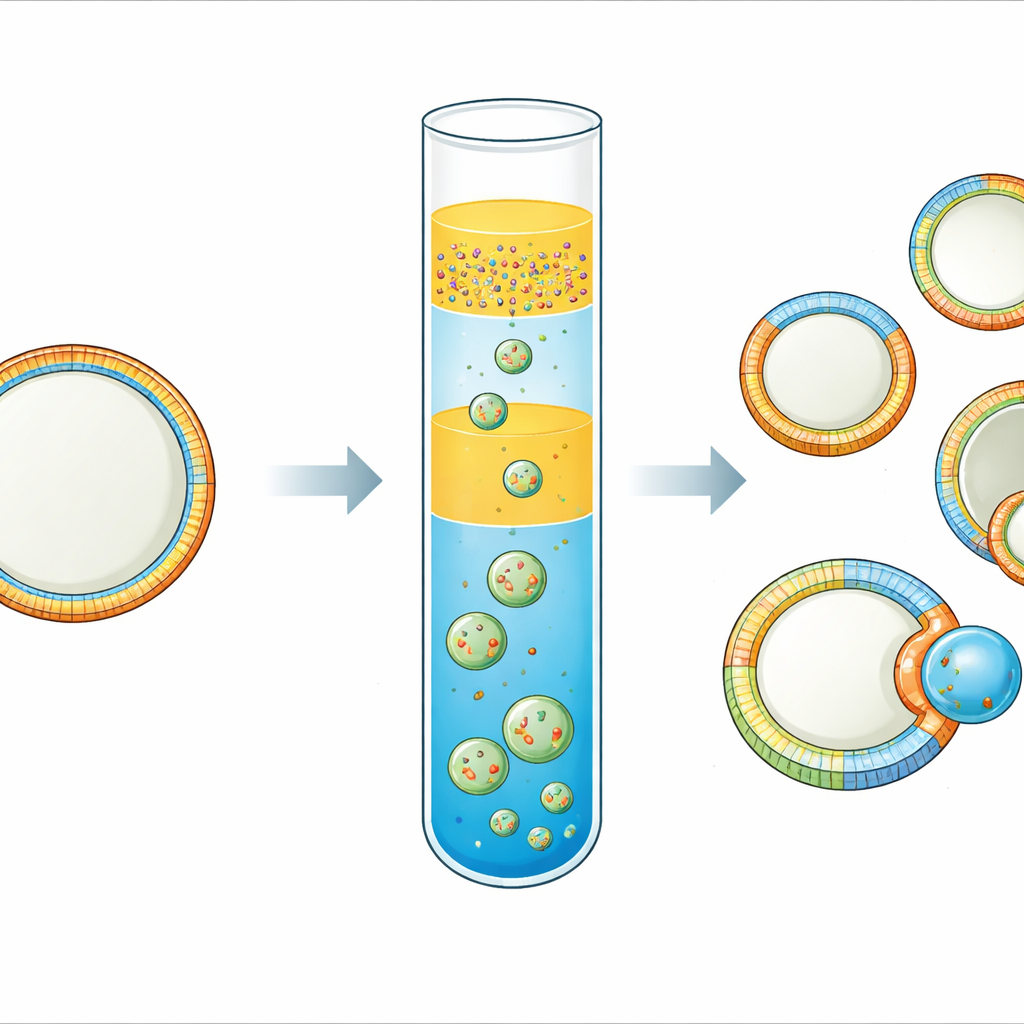
Beter nagemaakte celmodellen bouwen
Werkelijke celmembranen zijn asymmetrisch: de binnenzijde is rijk aan negatief geladen lipiden die signalerende eiwitten aantrekken, terwijl de buitenzijde andere lipiden draagt die cel–celherkenning bemiddelen. Veel laboratoriummethoden kunnen reuzengeslote vesikels maken—holle sferen van vetachtige moleculen—maar hun twee bladen eindigen meestal hetzelfde, en de binnenkant is moeilijk toegankelijk. Andere benaderingen die asymmetrie creëren vereisen vaak complexe apparaten, speciale lipiden of laten de vesikels vastzitten aan een oppervlak. De auteurs wilden vrijstaande, celformaat vesikels maken die hoge encapsulatie van biomoleculen combineren met robuuste, afstelbare asymmetrie die meer lijkt op die van een levende cel.
Een drielaags recept voor asymmetrische membranen
Het team verfijnde een "inverted emulsion"-techniek, waarbij kleine waterdruppels bedekt met lipiden door een olie–waterinterface worden gedreven om vesikels te vormen. Hun belangrijkste innovatie is een drielaagse olielaag. Onderaan bevindt zich een olie met de lipiden bestemd voor het buitenblad van het membraan. Daarboven plaatsen ze een dunne spacer-olie zonder lipiden, en bovenop daarvan een emulsie van waterdruppels omgeven door een tweede olie die de lipiden voor het binnenblad draagt. Tijdens een korte centrifugatiestap vallen de druppels door de spacer en onderste laag, nemen een tweede lipidenlaag op en sluiten tot vesikels. Door twee oliën met verschillende dichtheid te kiezen en de spacer op te nemen, wordt vermenging tussen de lipidenvoorraden sterk beperkt, zodat het binnen- en buitenblad verschillende samenstellingen behouden.
Testen of de twee zijden verschillend blijven
Om te verifiëren dat ze echt verschillende bladen hadden, gebruikten de onderzoekers zowel chemische als eiwitgebaseerde leesmethoden. In één reeks tests voegden ze een fluorescerend lipide alleen aan één blad toe en brachten ze de vesikels vervolgens in contact met een chemische stof in de buitenoplossing die de fluorescentie dooft maar niet door het membraan kan diffunderen. Wanneer het fluorescerende lipide aan de buitenzijde zat, daalde het signaal bijna volledig; wanneer het aan de binnenzijde zat, veranderde het nauwelijks, wat aantoonde dat de meeste gelabelde lipiden bleven waar bedoeld. In een tweede reeks experimenten plaatsten ze lipiden die specifieke eiwitten binden—zoals biotine-getagde lipiden voor streptavidine of speciale kopgroepen voor His-getagd groen fluorescerend eiwit—slechts in één bladzijde. Eiwitten toegevoegd in het tegenovergestelde compartiment (binnen of buiten) binden alleen wanneer hun bijpassende lipide aan dezelfde kant van het membraan zat, waarmee zowel sterke asymmetrie als behoud van eiwitfunctie werd bevestigd.
Riffen creëren en membranen zien budden
Werkelijke celmembranen bevatten ook "riffen": kleine vlekken verrijkt in bepaalde lipiden zoals cholesterol en sphingomyeline, die eiwitten kunnen clusteren en de vorm kunnen beïnvloeden. Het bereiken van dergelijke faseafscheiding met de inverted emulsion-methode was moeilijk omdat cholesterol de neiging had in olie opgelost te blijven in plaats van in het membraan te gaan. Door squalene in de onderste olielaag te gebruiken, die cholesterol minder sterk vasthoudt dan standaard mineraalolie, konden de auteurs reproduceerbaar vesikels vormen waarvan de membranen splitsten in coëxisterende vloeibaar-geordende en vloeibaar-ongorde regio’s, veel zoals riffen. Ze combineerden deze laterale patroonvorming vervolgens met blad-asymmetrie: het ene domein droeg een binnenbladligand die streptavidine binnenin bond, terwijl een ander domein glycolipiden droeg die buiten het cholera-toxine bonden. 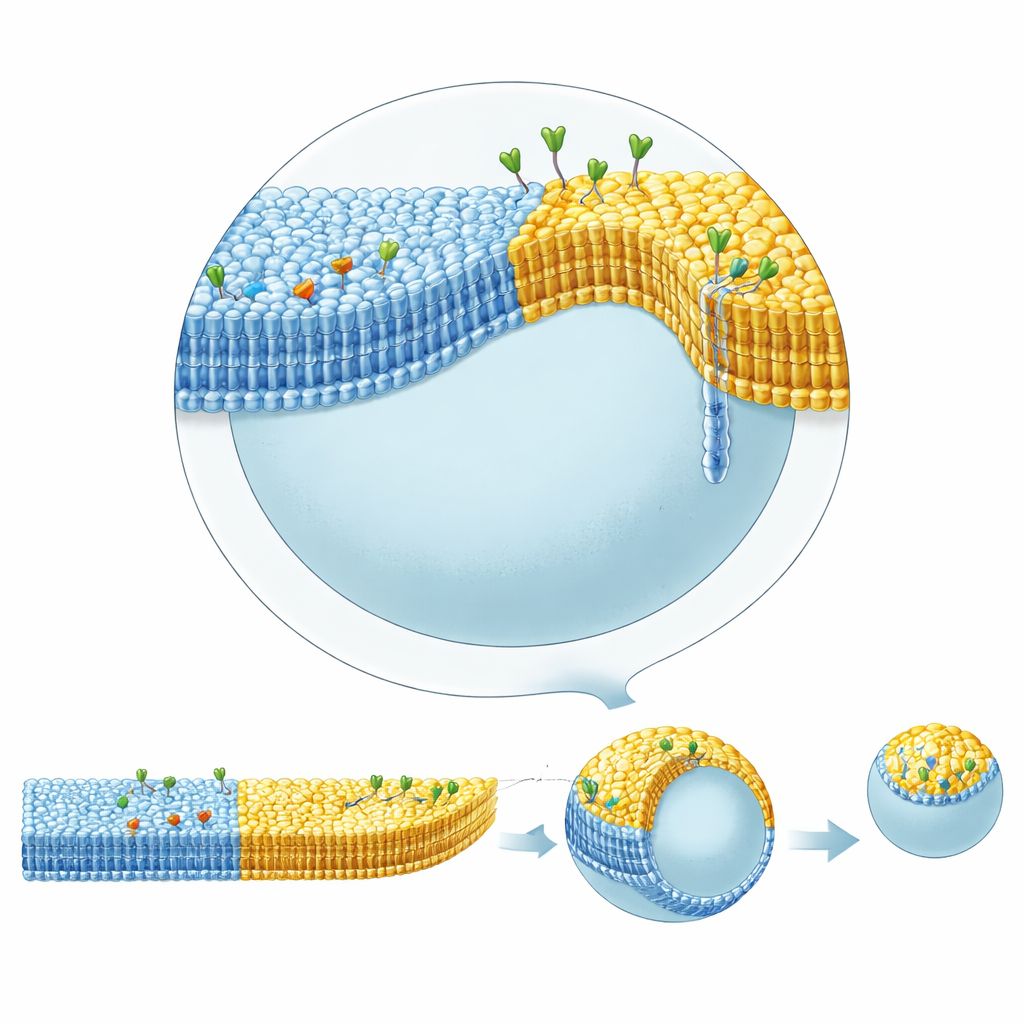
Hoe eiwitten en patronen vormveranderingen aandrijven
Deze complexe vesikels vertoonden opvallende vormdynamiek. Wanneer cholera-toxine aan glycolipiden in het geordende domein aan de buitenzijde bond, bolde dat domein naar buiten uit in een gekromde bud verbonden door een nauwe nek, en bij lichte osmotische deflatie kon het geheel volledig afknijpen als een dochtervesikel. Deze budding vereiste geen energiedragende moleculen zoals ATP of gespecialiseerd delingsapparaat; het ontstond puur door het samenspel van lipidesamenstelling, domeingrenzen en asymmetrische eiwitbinding. Door de hoeveelheid streptavidine gebonden aan de binnenzijde van het ongeordende domein te verhogen, kon het team de naar buiten gerichte buiging van het geordende domein tegenwerken en geleidelijk een meer bolvormige vorm herstellen. Gedetailleerde geometrische analyse van vesikelcontouren toonde aan dat de kromming van het membraan springt bij de grens tussen domeinen, en dat de smalle nekkken die tijdens budding sluiten krachten van ten minste tientallen piconewton moeten weerstaan—waardoor wordt gekwantificeerd hoe domeinstructuur en eiwitopstapeling membranen mechanisch kunnen vormgeven.
Wat dit betekent voor toekomstige synthetische cellen
Simpel gezegd hebben de auteurs een recept ontwikkeld om zachte, celformaat belletjes te maken waarvan de huidjes gepatroneerd en tweezijdig zijn, sterk vergelijkbaar met echte celmembranen. Omdat de methode relatief eenvoudig is, werkt met veel verschillende lipiden en toelaat dat eiwitten en andere grote moleculen worden opgesloten, effent het de weg voor het bouwen van meer levensechte kunstmatige cellen van onderop. Zulke synthetische cellen kunnen wetenschappers helpen ontleden hoe membraanpatronen signalering, transport en deling regelen, en ze zouden uiteindelijk kunnen worden ingezet als slimme medicijndragers die van vorm veranderen of op commando splitsen in het lichaam.
Bronvermelding: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
Trefwoorden: synthetische cellen, lipidenmembranen, membraanasymmetrie, faseafscheiding, membraanbudding