Clear Sky Science · nl
Nanodiscplatform met virale glycoproteïnen voor vaccinevaluatie
Virusproteïnen omzetten in meetbare doelen
Moderne vaccins vertrouwen steeds vaker op nauwkeurig ontworpen versies van de eiwitten die het oppervlak van virussen sieren. Deze eiwitten zijn de belangrijkste doelen voor beschermende antilichamen, maar ze zijn berucht moeilijk te bestuderen in hun natuurlijke, membraangebonden vorm. Dit artikel beschrijft een nieuw laboratoriumplatform dat volledige, langste virusoppervlakte-eiwitten plaatst in kleine, platte lipidedeeltjes die nanodiscs worden genoemd. Deze opstelling stelt onderzoekers in staat te meten hoe goed vaccin-kandidaten echte virussen nabootsen, hoe antilichamen zich eraan hechten, en hoe deze vaccins kunnen worden herontworpen voor betere bescherming.
Waarom het recreëren van het virale oppervlak telt
Veel van de belangrijkste virale eiwitten zitten verankerd in een vetmembraan, precies zoals op een echt virus. Traditionele labmethoden knippen het membraandeel weg om deze eiwitten makkelijker te produceren en te zuiveren in oplossing. Die shortcut verwijdert echter regio’s dicht bij het membraan die juist waardevolle antilichaamdoelen herbergen, waaronder een segment van HIV dat bekendstaat als de membrane-proximal external region (MPER). Deze nabij-membraanregio’s kunnen er anders uitzien en zich anders gedragen wanneer ze niet ingebed zijn in een realistische lipideomgeving, wat betekent dat oplosbare eiwitfragmenten een onvolledig of misleidend beeld kunnen geven van hoe een vaccin in het lichaam zal werken.
Het bouwen van een veelzijdig nanodiscplatform
De onderzoekers ontwikkelden een gestroomlijnde workflow van vijf dagen om volledige virale oppervlakte-eiwitten uit menselijke cellen te winnen, hun natuurlijke membraan-doorlopende segmenten intact te houden en ze opnieuw in een gecontroleerde lipidedisc te plaatsen. Ze brachten eerst ontworpen HIV- en ebolaglycoproteïnen tot expressie op celoppervlakken, haalden die vervolgens voorzichtig los met detergent en vingen ze op een zuiveringsmatrix. Terwijl de eiwitten nog waren bevestigd, voegden ze gedefinieerde lipiden en een ceintuurachtige scaffold-eiwit toe dat zichzelf assembleert tot een kleine, schijfvormige membraan. Toen het detergent werd verwijderd, zakten de virale eiwitten in deze nanodiscs. De resulterende preparaten waren hoogst zuiver, maandenlang stabiel in de koelkast en droegen glycaan (suiker) bedekkingen die sterk overeenkwamen met die op native virale spikes. 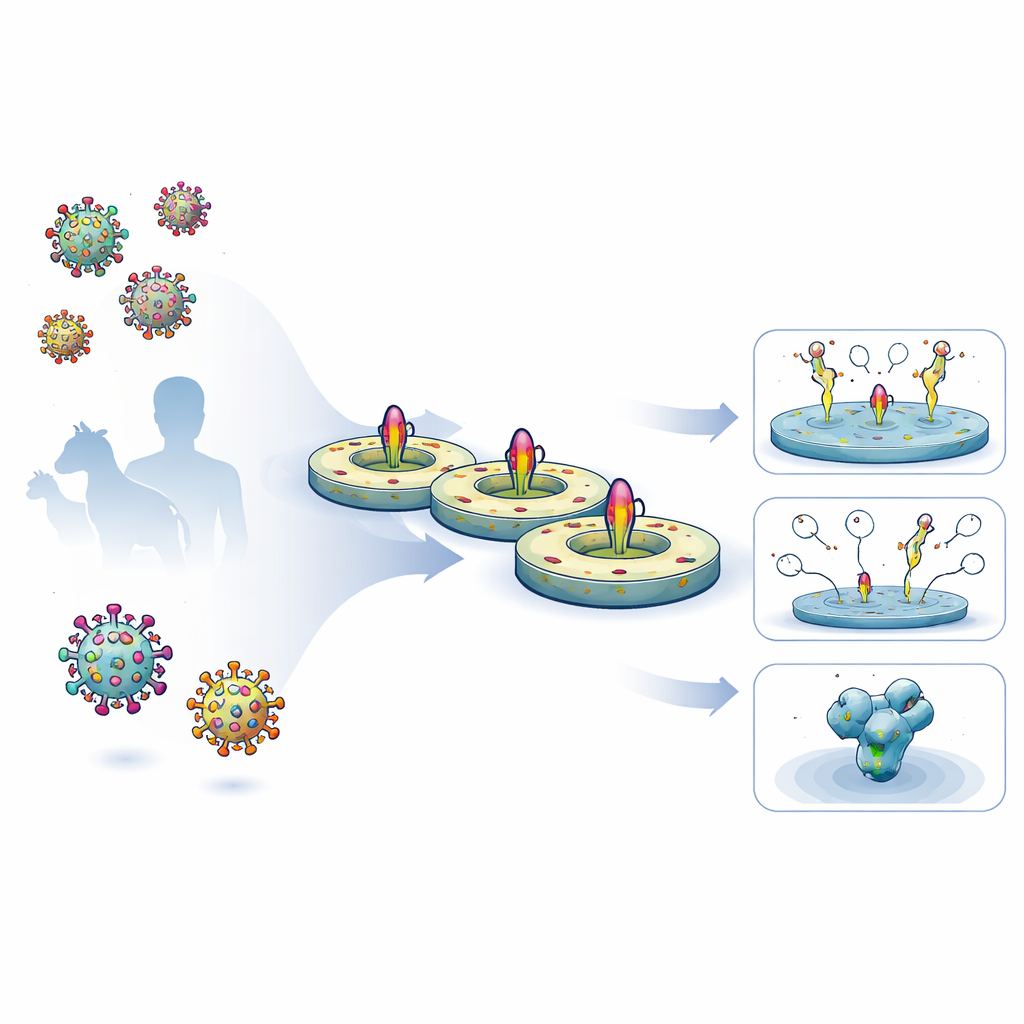
Antistofbinding en immuunreacties uitlezen
Met nanodisc-geïntegreerde eiwitten ter beschikking testte het team hoe goed verschillende antilichamen konden binden in meerdere surface plasmon resonance (SPR)-opstellingen, een techniek die binding in real time volgt. Met HIV-nanodiscs die ontworpen waren om de MPER-regio bloot te leggen, toonden ze aan dat een krachtige breed neutraliserend antilichaam genaamd 10E8 ongeveer 70 keer sterker bond aan het ontworpen construct dan aan een eerdere opzet, voornamelijk omdat het veel langzamer losliet. Controlemutaties die de MPER-regio verstoorden, elimineerden de 10E8-binding volledig, wat bevestigt dat het platform gevoelig rapporteert hoe ontwerpswijzigingen sleutelepitopen beïnvloeden. Dezelfde nanodiscs werkten ook als probes in flowcytometrie, waar ze hielpen B-cellen uit geïmmuniseerde muizen en apen te isoleren die de volledige transmembranairvorm van het HIV-eiwit herkenden, inclusief delen die afwezig zijn in standaard oplosbare probes. 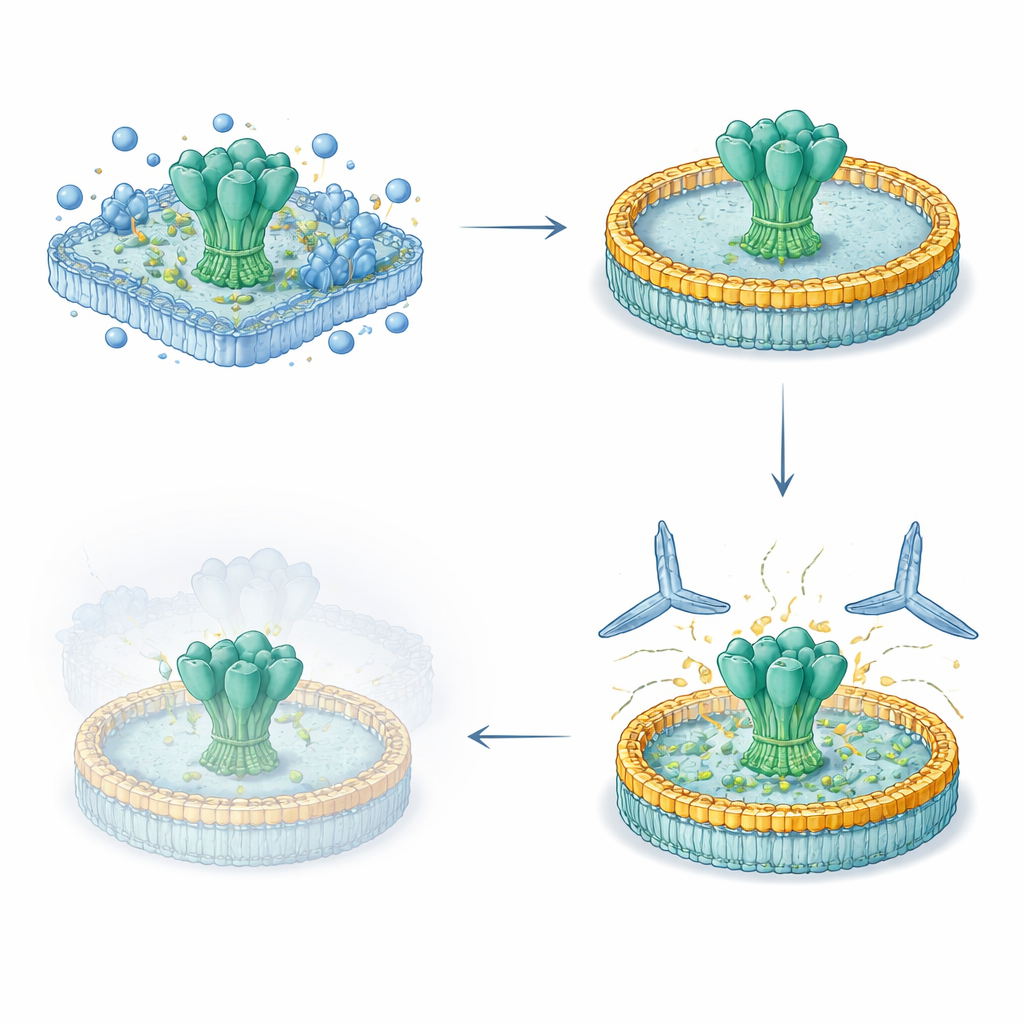
Het volledige doel in atomaire details zien
Om precies te begrijpen hoe antilichamen de MPER in zijn native setting herkennen, gebruikten de auteurs cryogene elektronmicroscopie om de ontworpen HIV-nanodiscs te filmen gebonden aan drie verschillende breed neutraliserende antilichamen. Ze verkregen een structuur van 3,5 angström van één antilichaam, 10E8, terwijl het de MPER-sequentie benaderde terwijl de rest van de HIV-spike verankerd bleef in de lipidedisc. Dit onthulde een doorlopend netwerk van contacten tussen 10E8 en zowel de MPER als nabijgelegen delen van het buitenste eiwit, waaronder een diepe pocket bij de overgang tussen twee subunits. Door deze structuur te vergelijken met eerdere afbeeldingen van 10E8 gebonden alleen aan een kort peptide, toonde het team aan dat de membraanomgeving en de volledige spike extra contacten en dynamische bewegingen mogelijk maken die in eenvoudigere modellen onzichtbaar waren, en dat specifieke aminozuren in het virus sterk bepalen hoe gemakkelijk 10E8 het virus kan neutraliseren.
Brede toepassingen voor slimmere vaccins
In praktische termen biedt dit nanodiscplatform vaccinontwerpers een manier om transmembranair-vaccinkandidaten te evalueren met dezelfde krachtige analytische tools die lange tijd waren voorbehouden aan oplosbare eiwitfragmenten. Het werkt voor verschillende virussen, ondersteunt gedetailleerde bindingsmetingen, maakt precieze sortering en sequencing van vaccin-geïnduceerde B-cellen mogelijk, en levert hoogresolutie-structuren op die realistische membraan-proximale epitopen vastleggen. Voor de niet-specialist is de kernboodschap dat wetenschappers nu een levensechter testplatform hebben voor virale oppervlakte-eiwitten — een platform dat kan laten zien welke vaccinontwerpen echt lijken en gedragen als het echte virus en hoe je ze kunt bijsturen voor sterkere, bredere antilichaamreacties. Dit zou de ontwikkeling van volgende-generatievaccins versnellen, niet alleen tegen HIV maar ook tegen vele andere omhulde virussen.
Bronvermelding: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Trefwoorden: nanodiscs, HIV-vaccins, virale glycoproteïnen, breed neutraliserende antilichamen, cryo-EM