Clear Sky Science · nl
Radicale footprinting in geheel zoogdierbloed
Proteïnen in actie zien in echt bloed
De eiwitten in ons bloed veranderen continu van vorm terwijl ze vitale taken uitvoeren, zoals het bestrijden van infecties, het transporteren van ijzer en het reageren op ziekte. Tot nu toe werkten de meeste instrumenten om deze subtiele vormveranderingen te onderzoeken alleen in vereenvoudigde laboratoriummonsters of geïsoleerde cellen. Deze studie toont voor het eerst aan dat wetenschappers eiwitstructuren rechtstreeks kunnen aflezen in intact zoogdierbloed, wat een route opent om ziekteprocessen te volgen zoals ze daadwerkelijk in het lichaam plaatsvinden.
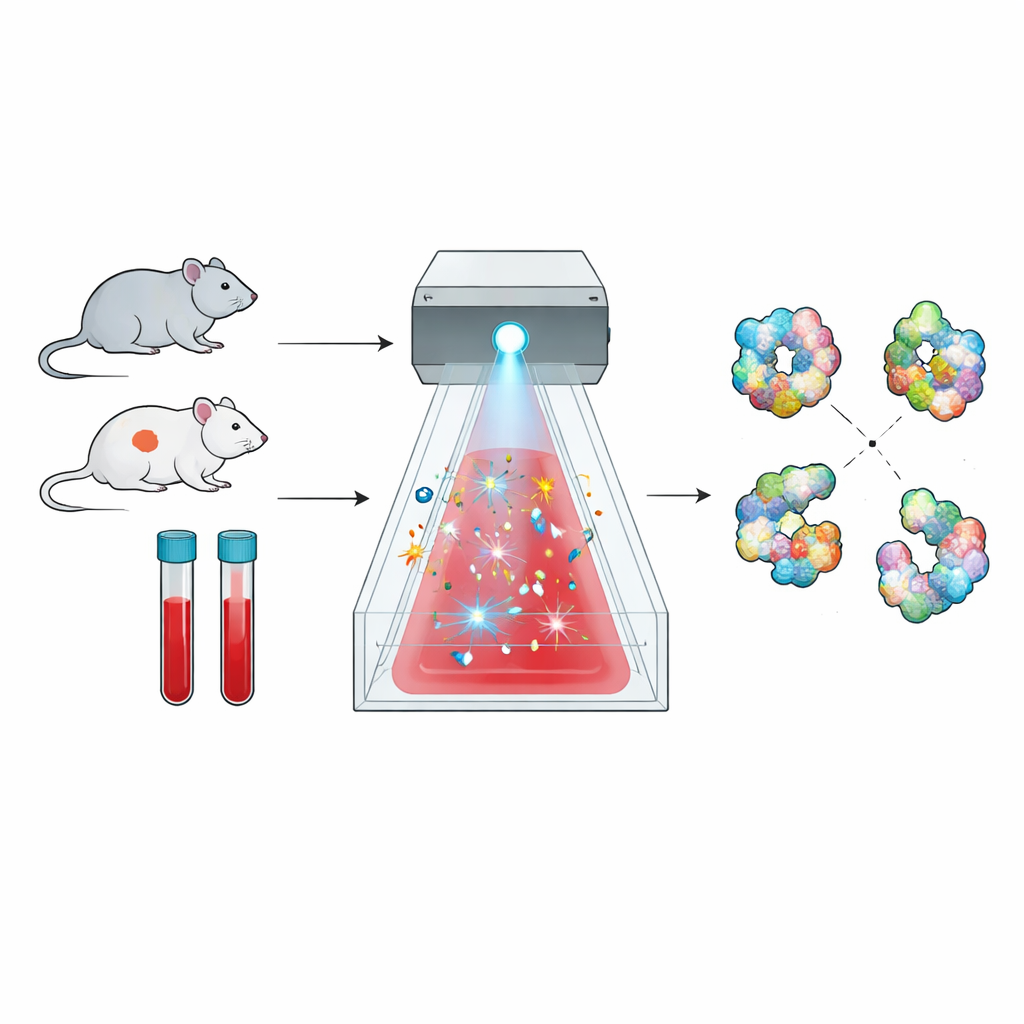
Een nieuwe manier om eiwitvormen in kaart te brengen
Eiwitten zijn geen starre kralen; ze vouwen zich tot ingewikkelde driedimensionale vormen en die vormen bepalen wat ze kunnen doen. De hier onderzochte methode, radicale eiwit-footprinting genoemd, maakt gebruik van dat feit. Korte uitbarstingen van zeer reactieve moleculen werken als een chemische "flits" en treffen alleen de delen van een eiwit die blootgesteld zijn aan de omliggende vloeistof. Later wordt massaspectrometrie gebruikt om te tellen waar die chemische inslagen plaatsvonden, wat een soort oppervlaktemap of voetafdruk van de vorm van elk eiwit oplevert. Veranderingen in die voetafdruk tussen gezonde en zieke toestanden onthullen subtiele verschuivingen in hoe het eiwit gevouwen is of hoe het met partners samenwerkt.
De techniek laten werken in geheel bloed
Het direct toepassen van deze benadering op bloed is een langlopende uitdaging geweest. Bloed absorbeert ultraviolette straling sterk en zit vol enzymen, zoals catalase, die de gebruikelijke radicalengenererende chemicaliën snel vernietigen voordat ze eiwitten kunnen markeren. De onderzoekers losten dit op door over te schakelen op natriumpersulfaat, dat door een felle breedbandflits van licht in krachtige sulfaatradicalen kan worden gesplitst. Met een commercieel systeem genaamd FOX toonden ze aan dat persulfaat betrouwbaar geactiveerd kan worden en dat een ingebouwde dosimetrie-uitlezing kan bijhouden hoeveel radicalen worden geproduceerd, waardoor de "blootstelling" van elk monster nauwkeurig gecontroleerd kan worden.
Cellen beschermen terwijl details worden vastgelegd
Aangezien deze methode bedoeld is om eiwitten in iets dat dichtbij hun natuurlijke staat staat te bestuderen, was het cruciaal dat de bloedcellen zelf niet werden vernietigd. Tests op muizenbloed toonden aan dat toevoeging van geconcentreerd persulfaat slechts kleine, omkeerbare veranderingen in de vorm van rode bloedcellen veroorzaakte en minder dan twee procent celdestructie gaf, vergelijkbaar met eenvoudige zoutoplossingen. Het team ontwikkelde ook een verbeterde "quench"-mix die resterende reactieve soorten snel incorporeert en zo voorkomt dat langzamere nevenreacties na de flits valse schade veroorzaken. Gezamenlijk maakten deze verfijningen het mogelijk om eiwitten in intact muizenbloed te labelen terwijl de celstructuur behouden bleef en de achtergrondruis zeer laag bleef.
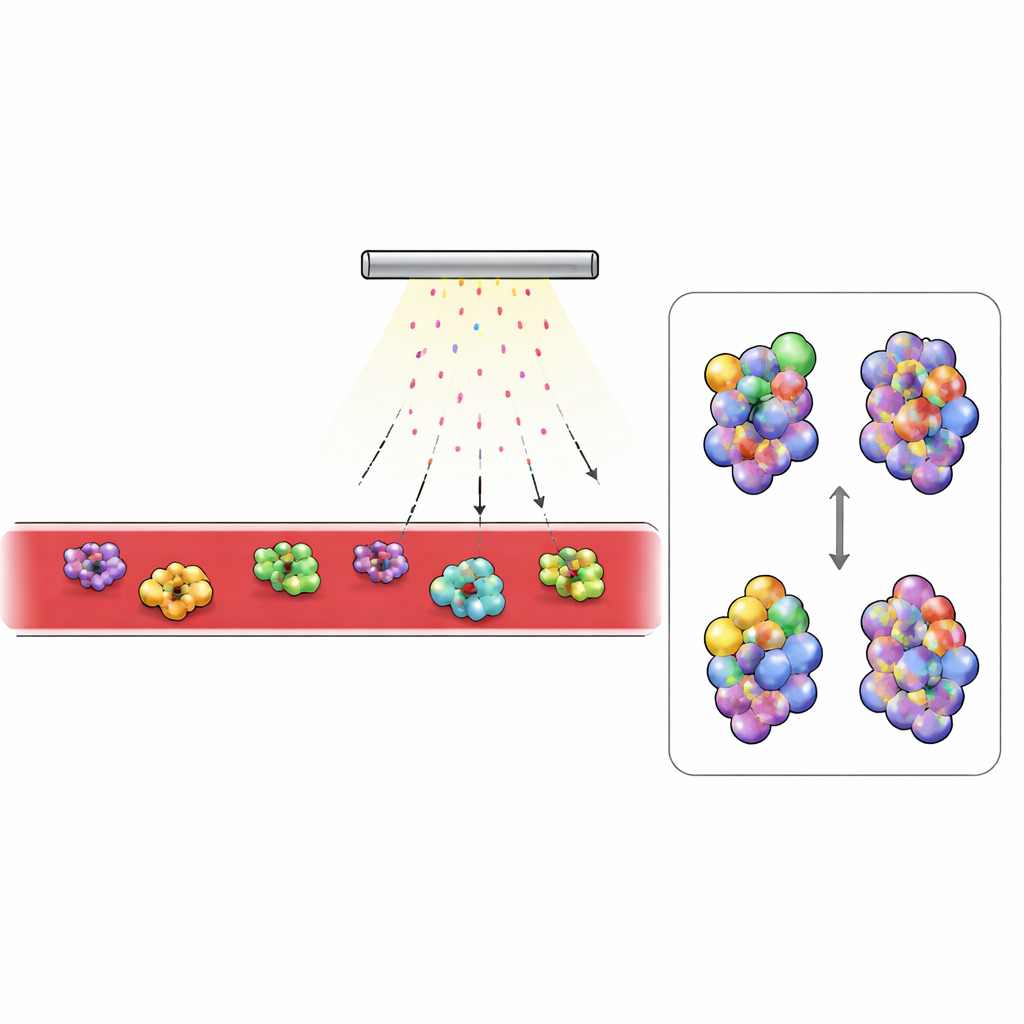
Wat verandert in diabetsch bloed
Met dit platform vergeleken de onderzoekers bloed van gezonde muizen en van een veelgebruikt model van type 2 diabetes. Ze concentreerden zich op de meest voorkomende gedetecteerde eiwitten, vooral die circuleren buiten cellen. Extracellulaire eiwitten toonden veel zwaardere labeling dan die binnen cellen, wat de beperkte penetratie van persulfaat in celinterieurs weerspiegelt. Twee bloedproteïnen staken eruit: complement C3, een sleutelelement van het immuunsysteem, en transferrine, dat ijzer transporteert. Bij diabetische muizen werden regio’s van C3 die verborgen raken wanneer het eiwit in zijn actieve vorm schakelt minder gelabeld, terwijl normaal verborgen gebieden meer blootgelegd waren. Dit patroon kwam overeen met de bekende structurele verandering wanneer C3 wordt omgezet in zijn actieve fragment, C3b, en bloedtests bevestigden dat diabetische dieren veel meer geactiveerd C3 hadden. Bij transferrine waren gebieden nabij de ijzerbindingsplaats beter beschermd in diabetisch bloed, wat consistent is met dat het eiwit meer ijzer draagt. Onafhankelijke metingen toonden hoger serumijzer en een groter aandeel van transferrine verzadigd met ijzer bij diabetische muizen.
Waarom dit belangrijk is voor gezondheid en geneeskunde
Voor de niet-specialist is de kernboodschap dat de auteurs een manier hebben ontwikkeld om de vormen van vele eiwitten tegelijk aan te voelen, direct in echt bloed, en die vormpatronen vervolgens te gebruiken om af te leiden hoe ziekte de chemie van het lichaam verandert. In dit muismodel van type 2 diabetes onthult de methode overactieve complement‑signalering en zwaardere ijzerbelasting van transferrine — veranderingen die klassieke tests mogelijk missen of slechts indirect waarnemen. Omdat de benadering werkt met kleine bloedmonsters en een gestandaardiseerde lichtbron gebruikt, zou het uiteindelijk kunnen helpen vroege structurele waarschuwingssignalen van ziekte te identificeren, de werking van biologische geneesmiddelen in de bloedbaan te volgen en het ontwerp van effectievere behandelingen te sturen.
Bronvermelding: Zhao, M., Tobin, L., Misra, S.K. et al. Radical footprinting in mammalian whole blood. Nat Commun 17, 2470 (2026). https://doi.org/10.1038/s41467-026-68982-4
Trefwoorden: structurele proteomica, bloedproteïnen, type 2 diabetes, complementsysteem, ijzerstofwisseling