Clear Sky Science · nl
Variaties in het C-uiteinde van eiwitten beïnvloeden proteostase
Hoe het staartje van eiwitten gezondheid vormgeeft
Elk eiwit in onze cellen eindigt met een klein "staartje" van slechts een paar bouwstenen. Die staartjes lijken misschien bijzaak, maar deze studie toont aan dat ze stilletjes bepalen welke eiwitten blijven en welke snel worden verwijderd. Omdat eiwitniveaus ten grondslag liggen aan kanker, genetische aandoeningen en hoe cellen reageren op stress, biedt het begrijpen van deze staartjes nieuwe manieren om ziektarisico’s te beoordelen en mogelijk toekomstige behandelingen te ontwerpen.
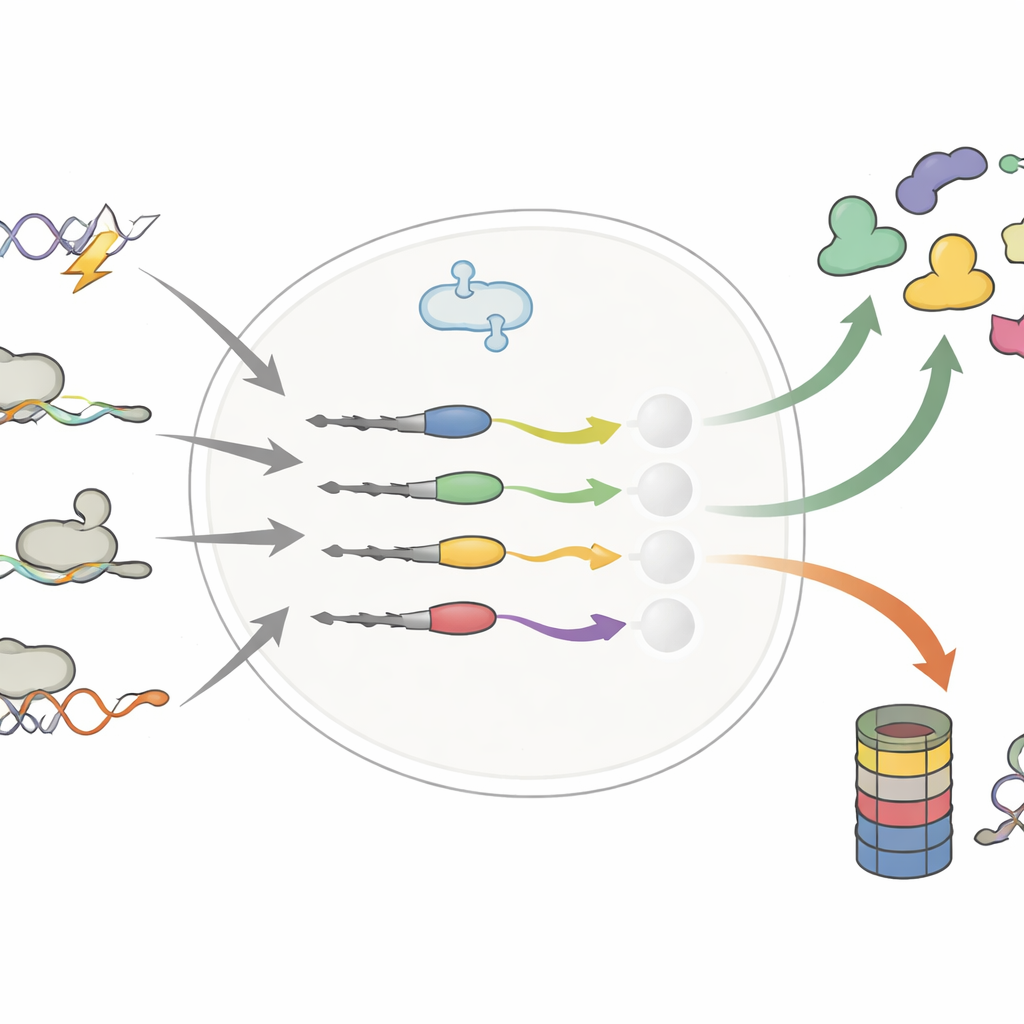
Kleine veranderingen aan het eiwitstaartje, grote verschuivingen in levensduur
De auteurs concentreerden zich op het verre uiteinde van eiwitten — het C-terminus — waar al een paar extra of verwisselde bouwstenen kunnen ontstaan door DNA-mutaties, alternatieve RNA-splicing of doordat ribosomen voorbij het gebruikelijke stopteken lezen. Eerder werk suggereerde dat zulke "foutieve" staartjes vooral als verwijderingslabels fungeren en foutieve eiwitten naar de celversnipperaar sturen. Door systematisch duizenden normale en gewijzigde staartjes te vergelijken, zet deze studie dat eenvoudige beeld op zijn kop. Het team laat zien dat gewijzigde staartjes zowel de levensduur van een eiwit kunnen verkorten als verlengen, soms door kankerbevorderende eiwitten te stabiliseren of tumorremmers te destabiliseren.
Wanneer genetische fouten eiwitten helpen of schaden
Een belangrijke bron van staartveranderingen zijn nonstopmutaties, die een normaal stopsignaal wissen zodat het ribosoom verder leest in een RNA-stuk dat normaal stil blijft. De onderzoekers testten meer dan 3.000 ziektegerelateerde nonstopvarianten met een dual-kleur reporter die meet hoe sterk elk staartje een model-eiwit beschermt of verzwakt. Gemiddeld maakten gemuteerde staartjes eiwitten nog steeds minder stabiel dan hun normale tegenhangers, maar een substantieel deel deed het tegenovergestelde: ongeveer één op de tien nonstopmutaties stabiliseerde eiwitten, terwijl bijna een derde ze destabiliseerde. Deze verschuivingen troffen bekende oncoproteïnen en tumorrepressoren, wat impliceert dat ogenschijnlijk subtiele mutaties daadwerkelijk het evenwicht tussen celgroei en celdood kunnen doen kantelen.
Ingebouwde variatie door splicing en readthrough
Niet alle staartverschillen zijn ongelukjes. Onze genen produceren routinematig meerdere eiwitversies via alternatieve splicing en geprogrammeerde stopcodon-readthrough. Door menselijke genencatalogi te doorzoeken, vonden de auteurs dat bijna twee derde van de genen eiwitten met meer dan één staartontwerp maakt, en veel daarvan verschillen slechts in de laatste paar bouwstenen. Het testen van geselecteerde voorbeelden toonde aan dat deze bijna-identieke versies vaak duidelijk verschillende halfwaardetijden hebben. Sommige door readthrough gegenereerde staartjes maakten eiwitten stabieler, andere minder stabiel. Dit suggereert dat cellen staartvariatie doelbewust gebruiken als een fijnregeling, waarmee ze bepalen hoe lang specifieke eiwitvormen in verschillende weefsels of omstandigheden blijven bestaan.
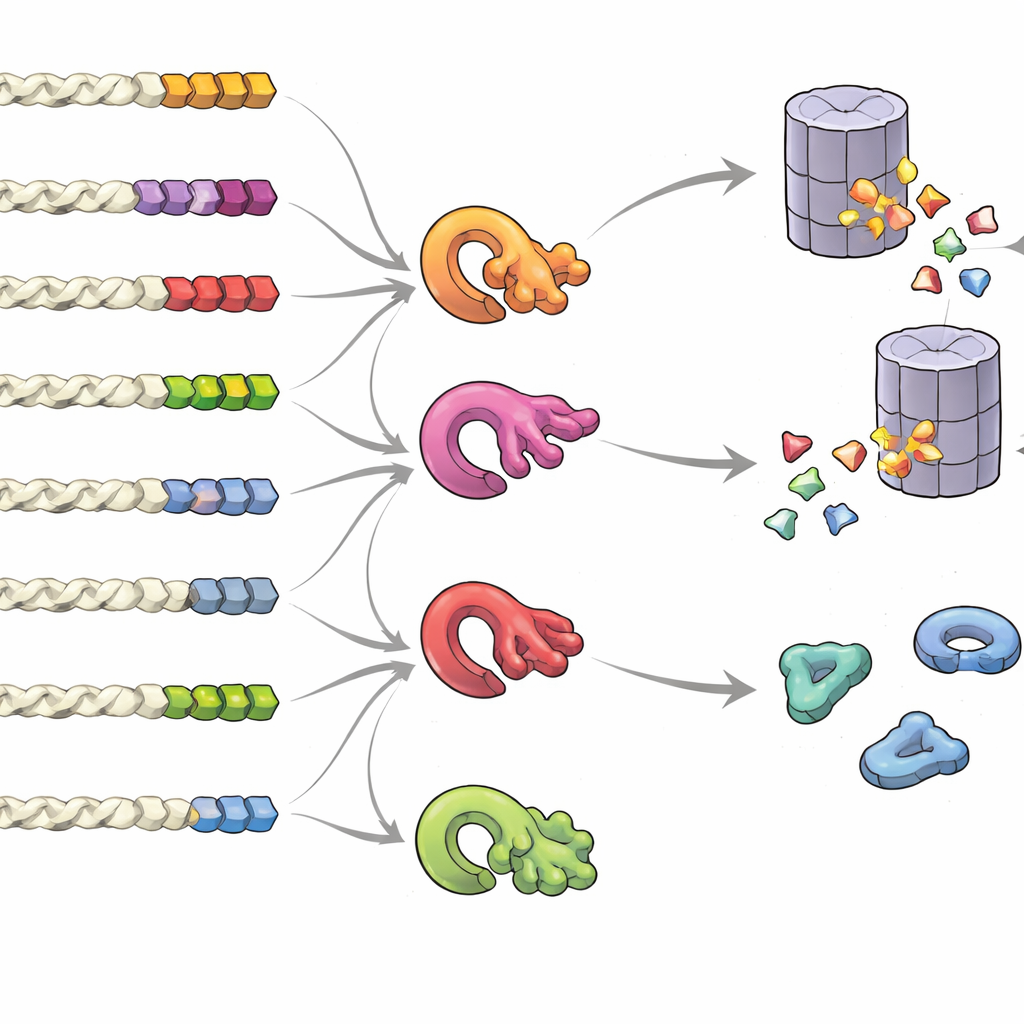
Wat maakt een staart een signaal voor "houd me" of "gooi me weg"
Om te begrijpen welke kenmerken van een staart het lot van een eiwit bepalen, maakte het team bibliotheken met willekeurige staartjes en mat hun impact in bulk. Ze vonden dat het niet één vast "motief" is, maar de algehele samenstelling, positie en clustering van bepaalde bouwstenen die ertoe doen. Staartjes rijk aan kleine of vette (hydrofobe) componenten, of de zeldzamere cysteïne en tryptofaan, nodigden eerder afbraak uit, vooral wanneer deze residuen geclusterd waren. Daarentegen bevorderden staartjes die rijk zijn aan zure (negatief geladen) componenten stabiliteit. Over veel soorten heen toonden normale eiwitstaarten duidelijke tekenen van evolutionaire druk om risicovolle patronen te vermijden, terwijl foutgevoelige readthrough- of frameshift-staartjes een bias hadden richting destabiliserende samenstellingen. De groep ontdekte ook dat meerdere kwaliteitscontrole-enzymen — verschillende ubiquitine-ligases — zich specialiseren in het herkennen van uiteenlopende hydrofobe staartpatronen, waardoor een complex netwerk ontstaat dat beslist welke eiwitten worden afgebroken.
Waarom dit belangrijk is voor geneeskunde en biotechnologie
Het werk herdefinieert eiwitstaarten van passieve eindpunten tot actieve regelaars van eiwithoeveelheden. Voor een leek betekent dit dat veel ziekten mogelijk niet alleen voortkomen uit kapotte eiwitten, maar ook uit subtiele veranderingen in hoelang eiwitten blijven bestaan, aangedreven door kleine verschillen aan hun uiteinden. Het waarschuwt ook dat therapieën die doelbewust readthrough van stopsignalen bevorderen — toegepast bij sommige genetische aandoeningen — onbedoeld de levensduur van veel normale eiwitten kunnen veranderen. Tegelijk suggereren de bevindingen krachtige nieuwe strategieën: door staartsequenties te ontwerpen of cellen aan te zetten bepaalde splicevormen of readthrough-gebeurtenissen te bevoordelen, zouden wetenschappers op den duur eiwitniveaus met opmerkelijke precisie omhoog of omlaag kunnen bijstellen.
Bronvermelding: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Trefwoorden: eiwitstabiliteit, C-uiteinde, eiwitafbraak, genetische mutaties, proteostase