Clear Sky Science · nl
OmiGA voor ultra‑efficiënte mapping van moleculaire kwantitatieve eigenschapslocussen
Waarom dit belangrijk is voor gezondheid en fokkerij
De moderne genetica heeft miljoenen DNA‑verschillen onthuld die eigenschappen zoals ziektegevoeligheid, groei en metabolisme subtiel beïnvloeden. De meeste van deze verschillen werken niet door eiwitten direct te veranderen, maar door de activiteit van genen fijn af te stemmen. Om deze regelgevende laag te begrijpen, koppelen wetenschappers “moleculaire eigenschappen” zoals genexpressie terug aan het genoom. Dit artikel introduceert OmiGA, een nieuwe analysetoolkit die dit soort mapping zowel nauwkeuriger als dramatisch sneller maakt, vooral in populaties waarin veel individuen verwant zijn, zoals boerderijdieren en sommige menselijke families. 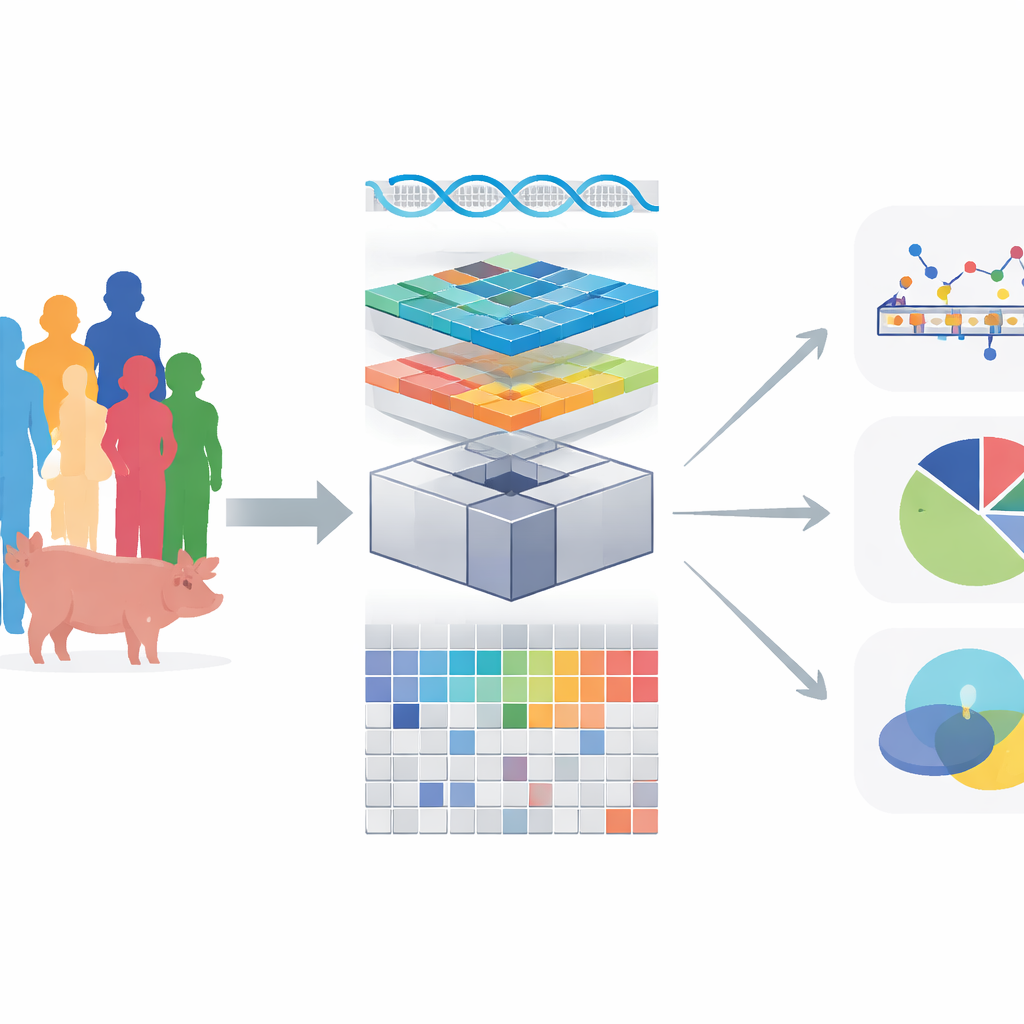
Van DNA naar schakelaars die genen aansturen
In plaats van alleen naar uiterlijke eigenschappen zoals lengte of vetgehalte te kijken, vraagt mapping van moleculaire eigenschappen hoe DNA‑varianten interne meetwaarden veranderen: welke genen omhoog of omlaag worden gezet, hoe RNA wordt gespleten, en vergelijkbare metingen over duizenden genen en weefsels. Plaatsen in het genoom die deze moleculaire metingen beïnvloeden, worden moleculaire kwantitatieve eigenschapslocussen genoemd, of molQTLs. Het vinden ervan helpt wetenschappers een pad te tekenen van DNA‑verandering naar genregulatie tot ziekte‑ of productiviteitskenmerken. Veelgebruikte tools vereenvoudigen de statistiek om de berekeningen behapbaar te houden. Ze negeren vaak hoe nauw verwante individuen zijn, of hoe hele stukken van het genoom samen worden overgeërfd, wat valse signalen kan opleveren en echte effecten kan verbergen.
Waarom verwantschap een statistisch probleem is
In veel dierenrassen en in menselijke familieonderzoeken delen individuen grote DNA‑segmenten vanwege recente gemeenschappelijke voorouders. Deze “complexe verwantschap” kan twee ver verwijderde genetische locaties gekoppeld doen lijken aan dezelfde moleculaire eigenschap, alleen omdat ze samen worden geërfd, niet omdat beide daadwerkelijk het gen reguleren. Standaard lineaire modellen proberen dit te corrigeren door een paar samenvattende afstammingsmaten toe te voegen, maar ze hebben moeite wanneer langafstandscorrelaties in het genoom sterk zijn. Hoe nauwer de verwantschap in de populatie en hoe dichter de genetische data, des te meer blazen deze verkorte methoden de schijnbare signaalsterkte op, wat het aantal valse ontdekkingen doet stijgen.
Een op maat gemaakte motor voor omics‑schaal genetica
OmiGA is gebouwd rond lineaire gemengde modellen, een klasse statistische instrumenten die verwantschap aanpakt door de achtergrondgenetische gelijkenis tussen individuen expliciet te modelleren. De auteurs herontwierpen deze modellen voor omics‑gegevens, waarbij tienduizenden moleculaire eigenschappen worden getest tegen miljoenen DNA‑varianten. Ze introduceren nieuwe algoritmen die de traagste stappen van standaardmethoden vermijden, zware berekeningen hergebruiken over veel eigenschappen heen en op grafische processoren kunnen draaien voor extra snelheid. OmiGA schat ook hoeveel van elke moleculaire eigenschap wordt verklaard door nabijgelegen DNA‑veranderingen, verre regio’s en door niet‑additieve effecten waarbij genkopieën op complexere manieren interageren. Samen maken deze functies van een voorheen omslachtige aanpak een praktisch werkpaard voor grote studies. 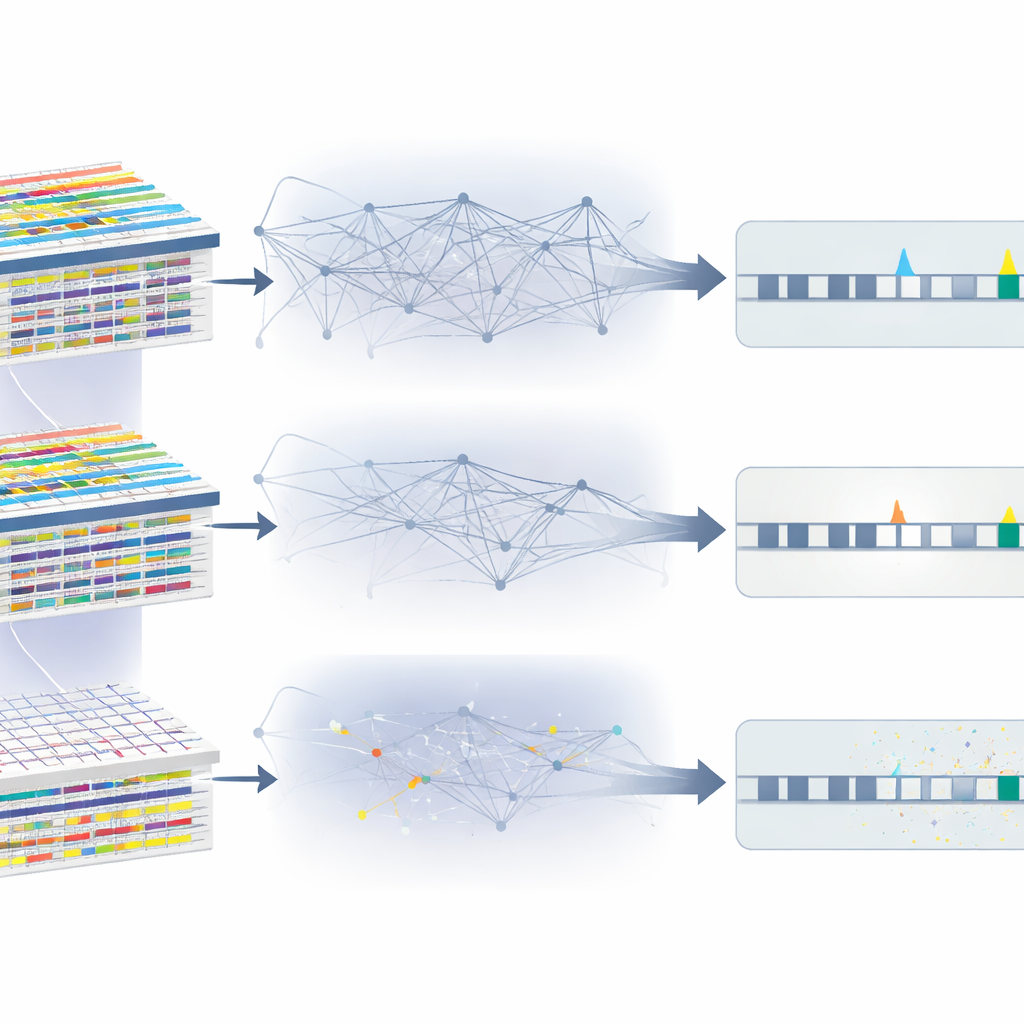
Scherdere signalen in simulaties en echte datasets
Het team vergeleek OmiGA met populaire tools zoals tensorQTL, APEX, GCTA en LDAK met zowel gesimuleerde data als echte metingen van varkens en mensen. In simulaties die nauwe varkenspopulaties en losser verbonden menselijke cohorten nabootsen, hield OmiGA consequent de achtergrondruis onder controle terwijl het het percentage echte ontdekkingen behield of verhoogde. In echte weefseldatasets van varkens identificeerde OmiGA aanzienlijk meer genen waarvan de expressie duidelijk gekoppeld is aan nabijgelegen DNA‑varianten, en deed dat met lagere rekencost. Het leverde ook smallere sets waarschijnlijk causale varianten bij het inzoomen op specifieke regio’s, en toonde sterkere overeenstemming tussen moleculaire signalen en traditionele associatieresultaten, wat suggereert dat het beter is in het aanwijzen van de daadwerkelijke regulatorische veranderingen achter complexe eigenschappen.
Nieuwe inzichten in dominantie en contextuele effecten
Naast standaard “additieve” effecten waarbij elke genkopie onafhankelijk bijdraagt, kan OmiGA dominante effecten modelleren, waarbij de ene kopie de andere kan maskeren of versterken. Toegepast op menselijke celdata vonden de auteurs dat veel genen met klassieke effecten ook verborgen dominante invloeden herbergen, en in sommige gevallen verschijnt dominantie waar additieve effecten dat niet doen. OmiGA detecteert ook contextafhankelijke regulatie, zoals genetische effecten die verschillen met afkomst of omgeving, en splitst erfelijkheid in lokale en verre componenten. Deze mogelijkheden openen de deur naar een rijker beeld van hoe DNA‑variatie moleculaire biologie vormgeeft in diverse populaties.
Wat dit vooruit betekent
Voor niet‑specialisten is de kernboodschap dat OmiGA een betrouwbaarder vergrootglas biedt om te zien hoe DNA‑verschillen de genactiviteit bijsturen, vooral in reële populaties waar verwanten vaak voorkomen. Door valse signalen te verminderen en werkelijk causale varianten te accentueren, helpt het moleculaire veranderingen met meer vertrouwen te koppelen aan eigenschappen zoals ziektegevoeligheid of vleeskwaliteit. Dit kan vervolgexperimenten verscherpen, fokbeslissingen in de landbouw verbeteren en inspanningen versterken om menselijke genetische studies te interpreteren door precies te onthullen welke regelgevende schakelaars in het genoom het belangrijkst zijn.
Bronvermelding: Teng, J., Zhang, W., Gong, W. et al. OmiGA for ultra-efficient molecular quantitative trait loci mapping. Nat Commun 17, 2680 (2026). https://doi.org/10.1038/s41467-026-68978-0
Trefwoorden: mapping van moleculaire QTL, regulatie van genexpressie, lineaire gemengde modellen, genetische verwantschap, omics‑gereedschapskist