Clear Sky Science · nl
VSIG10L is een belangrijke determinant van slokdarmhomeostase en erfelijke aanleg voor Barrett-slokdarm
Waarom dit belangrijk is voor mensen met brandend maagzuur
Chronisch brandend maagzuur komt veel voor, maar slechts een klein deel van de mensen ontwikkelt Barrett-slokdarm, een aandoening die tot slokdarmkanker kan leiden. Deze studie stelt een eenvoudige maar belangrijke vraag: waarom zijn sommige families veel gevoeliger voor Barrett-slokdarm dan andere? Door één gen te volgen en te onderzoeken hoe het de slijmlaag van de slokdarm bij mensen en muizen beïnvloedt, onthullen de onderzoekers een ontbrekende schakel tussen erfelijk risico, refluxschade en het vermogen van het lichaam om de slokdarm gezond te houden.
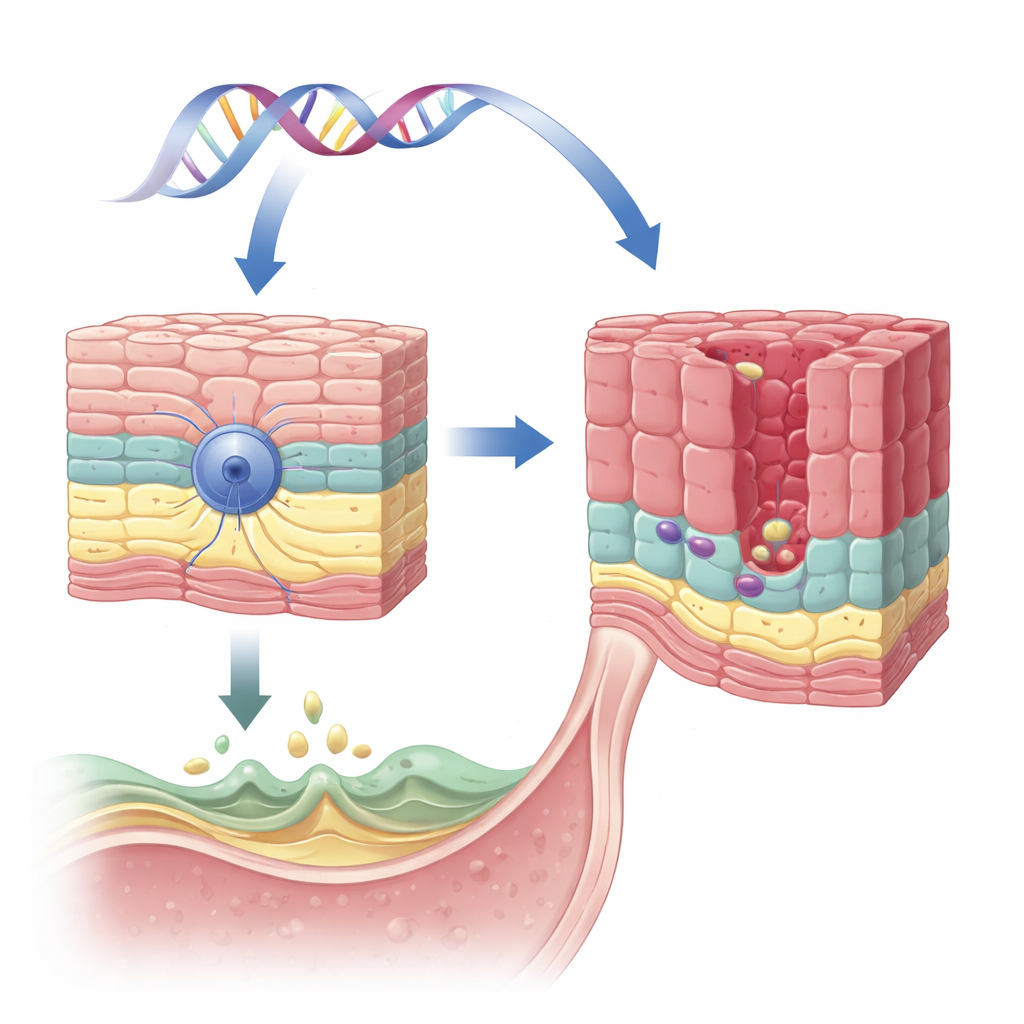
Een beschermend gen in de slokdarmslijmlaag
Het team concentreerde zich op een gen genaamd VSIG10L, eerder opgemerkt in één grote familie met veel leden die getroffen waren door Barrett-slokdarm en aanverwante kankers. VSIG10L is actief in de bovenste lagen van de platte (squameuze) cellen die de slokdarm bekleden, maar niet in de diepere, stamcelachtige basale cellen. Met een gevoelige RNA-detectiemethode in menselijk, varkens- en muismateriaal en driedimensionale kweek van menselijke slokdarmcellen toonden de onderzoekers aan dat VSIG10L consequent alleen wordt aangezet in ‘rijpere’ cellen net boven de basale laag. Dit patroon suggereert dat VSIG10L helpt de squameuze cellen hun laatste rijpingsstappen te voltooien en een stabiele barrière te vormen.
Erfelijke veranderingen die de barrière verzwakken
Door het VSIG10L-gen te sequencen bij 684 mensen uit 302 families met Barrett-slokdarm en slokdarmkanker ontdekten de onderzoekers meerdere zeldzame, schadelijke varianten. Om te testen wat deze varianten doen, maakten ze menselijke, stamcel-afgeleide slokdarmorganoïden van een patiënt die een dergelijke mutatie droeg. Vergeleken met organoïden van een gezonde donor konden de mutantorganoïden niet de normale, gelaagde squameuze structuur opbouwen. In plaats daarvan vormden ze vaak afwijkende, klierachtige cellenbollen die in een basale, onrijpe toestand bleven steken, gemarkeerd door een eiwit genaamd p63. Deze verstoring van normale gelaagdheid en rijping weerspiegelt vroege stappen die men denkt vooraf te gaan aan Barrett-slokdarm bij patiënten.
Muismodellen die menselijke ziekte nabootsen
Om verder te gaan dan kweekcellen creëerde het team muizen die ofwel een nauwkeurige kopie van de menselijke familiaire VSIG10L-mutatie droegen of een volledige uitval van het gen. Bij gezonde muizen is het overeenkomstige Vsig10l-gen opnieuw alleen actief in suprabasale squameuze cellen. Onder de elektronenmicroscoop vertoonden de mutantmuizen een opvallend verlies van desmosomen—de kleine “nagels” die aangrenzende cellen aan elkaar bevestigen—in deze lagen. Genexpressiekaarten van de squameuze forestomach, een muisregio die lijkt op de lagere slokdarm, toonden brede verstoring van structurele en differentiatieprogramma’s. Wanneer de muizen een dieet met het galzuur deoxycholaat kregen, ter nabootsing van chronische reflux, ontwikkelde 70–100% van de Vsig10l-mutante dieren uitgebreide Barrett-achtige mucinerijke plekken bij de overgang tussen squameus en columnair epithelium, terwijl wildtype-muizen slechts kleine, beperkte laesies ontwikkelden.
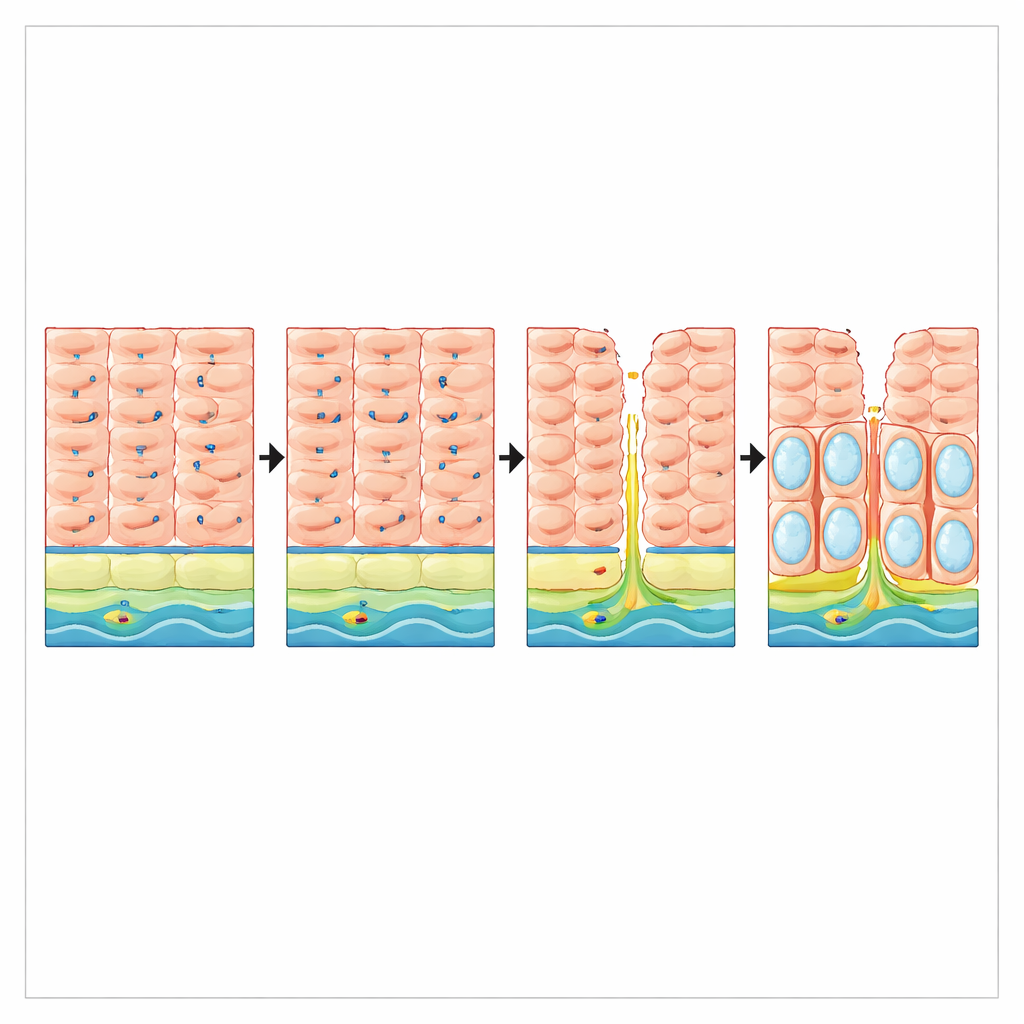
Refluxschade en verlies van bescherming bij patiënten
De onderzoekers onderzochten vervolgens of reflux zelf VSIG10L bij mensen zou kunnen verstoren. In biopten van patiënten met langdurige gastro-oesofageale refluxziekte maar zonder Barrett-slokdarm waren de VSIG10L-RNA-niveaus ongeveer drie keer lager dan bij mensen zonder reflux, hoewel de basale squameuze celmarker TP63 onveranderd bleef. In weefselsecties toonde een gezonde slokdarmbekleding een duidelijke band van VSIG10L-positieve cellen boven een basale laag. Daarentegen vertoonde refluxbeschadigd mucosa een uitbreiding van basale-achtige, p63-rijke cellen en bijna volledig verlies van de VSIG10L-positieve differentiatiegradient. Deze bevindingen suggereren dat chronische reflux niet alleen de fysieke integriteit van de bekleding aantast, maar ook het genprogramma dat de ordelijke vernieuwing ervan onderhoudt.
De onderdelen bij elkaar brengen
Gezamenlijk ondersteunen de resultaten een eenvoudig model: VSIG10L is een sleutelbewaker van de squameuze barrière van de slokdarm. Erfelijke defecten in dit gen, of verworven onderdrukking door chronische reflux, leiden tot gebrekkige rijping van de bekleding, minder cel–cel-ankers en een lekkere oppervlakte. In deze kwetsbare toestand bevordert herhaalde blootstelling aan zuur en gal abnormale, klierachtige genezing in plaats van herstel van de oorspronkelijke squameuze bekleding, wat de basis legt voor Barrett-slokdarm. Voor patiënten en families wijst dit onderzoek op toekomstige genetische tests die degenen met het hoogste risico kunnen aanwijzen en op nieuwe therapieën gericht op het behouden of herstellen van VSIG10L-functie, met als langetermijndoel het voorkomen van Barrett-slokdarm en de progressie naar kanker.
Bronvermelding: Ravillah, D., Singh, S., Katabathula, R.M. et al. VSIG10L is a major determinant of esophageal homeostasis and inherited predisposition to Barrett’s esophagus. Nat Commun 17, 2167 (2026). https://doi.org/10.1038/s41467-026-68975-3
Trefwoorden: Barrett-slokdarm, gastro-oesofageale reflux, genetische aanleg, epitheliale homeostase, risico op slokdarmkanker