Clear Sky Science · nl
Het benutten van allosterie in menselijke fucosyltransferase 8 met een covalente remmer om kernfucosylatie te onderdrukken
Waarom het blokkeren van een klein suikerrestje van belang kan zijn bij kanker
Onze cellen versieren voortdurend eiwitten met korte suikerketens die de werking van die eiwitten fijnregelen. Eén specifieke suikermarkering, kernfucosylatie, helpt tumoren groeien, zich te verspreiden, het immuunsysteem te ontwijken en zelfs weerstand te tonen tegen moderne kankertherapieën. Dit artikel beschrijft hoe onderzoekers een verborgen regelpunt op het menselijke enzym dat deze suiker aanbrengt ontdekten, en een nieuw, weinig toxisch molecuul bouwden dat zich covalent aan dat regelpunt hecht om het enzym uit te schakelen. Hun werk opent een nieuwe weg voor geneesmiddelen die celoppervlak‑suikers subtiel herbedraden in plaats van rechtstreeks DNA of eiwitten aan te vallen.
Hoe cellen suikertags gebruiken om ziekte te vormen
Eiwitten die de cel verlaten passeren een moleculaire ‘afwerkingslijn’ waar suikerketens worden aangebracht en bewerkt. Kernfucosylatie is zo’n afwerkingsstap, uitgevoerd door een enzym genaamd FUT8, dat een enkele fucose suikereenheid toevoegt op een sleutelpositie van veel door eiwitten verbonden glycans. Wanneer FUT8-niveaus stijgen, wordt dit suikermerk gebruikelijker op moleculen die celgroei, -beweging en immuunherkenning regelen. Studies koppelen hoge FUT8-activiteit aan agressieve melanoom, triple-negatieve borstkanker, longkanker en resistentie tegen gerichte middelen en sommige antilichaamtherapieën. Het blokkeren van FUT8 kan bepaalde immuunremmende eiwitten, zoals PD-1, van het celoppervlak verwijderen en tumoren beter zichtbaar maken voor het immuunsysteem, waardoor FUT8 een aantrekkelijk doelwit is voor kankerimmunotherapie en voor het verbeteren van biologische geneesmiddelen.
De behoefte aan slimmere, meer selectieve blokkers
Het ontwerpen van geneesmiddelen tegen FUT8 is lastig geweest omdat veel verwante enzymen dezelfde basis suikervoorziening gebruiken. Eerdere remmers bootsten vaak die suikertoevoer na, wat leidde tot brede, niet-selectieve blokkade van vele fucosylatiepaden en ongewenste bijwerkingen, waaronder stollingsproblemen die een klinische proef stillegden. De auteurs redeneerden dat een betere strategie zou zijn het drukke hoofdactieve centrum te vermijden en in plaats daarvan te zoeken naar een uniek ‘op afstand’ gelegen site op FUT8 die als controleschakelaar zou kunnen dienen. Met behulp van een high-throughput screeningsassay die de enzymactiviteit monitorde, doorploegden ze meer dan zesduizend verbindingen en identificeerden enkele ketenvormige moleculen die FUT8 vertraagden en tegelijkertijd de invasie van kankercellen in kweek verminderden.
Het ontdekken van een verborgen regelvak
Met behulp van röntgendiffractie loste het team de driedimensionale structuren van FUT8 gebonden aan twee van deze remmers op. Tot hun verrassing bevond geen van beide verbindingen zich op de gebruikelijke plek waar de suikerdonor en -acceptor binden. In plaats daarvan nestelden beide zich in een lange, kanaalachtige pocket tussen twee hoofdlobben van het enzym, dicht bij maar onderscheidbaar van het actieve centrum. Binding op deze plaats duwde bepaalde lusstructuren en sleutelaminozuren uit positie, met name elementen die normaal helpen de suikerdonor vast te houden. Computersimulaties toonden aan dat wanneer de pocket gevuld was, de algehele beweging en energielandschap van FUT8 verschoof naar conformaties die slecht zijn in het katalyseren van de reactie. Met andere woorden: de remmers werkten allosterisch: ze activeerden een verre knop die de werkende delen van het enzym uit lijn bracht.
Een hitmolecuul omzetten in een precies covalent hulpmiddel
Gewapend met deze structurele kaart zochten de onderzoekers naar moleculen die niet alleen de pocket konden bezetten, maar ook een permanente binding konden vormen met een nabijgelegen lysine‑residu (K216) dat van nature naar het kanaal toe beweegt. Ze vonden dat een reagens genaamd SSO, dat een reactieve N‑hydroxysuccinimide‑ester draagt, in dezelfde groef bond en een covalente verbinding met K216 vormde, waarmee het enzym in een inactieve toestand werd vergrendeld. Gebaseerd op gedeelde kenmerken van SSO en hun eerdere hit NH125, voegden ze fragmenten van beide samen om een nieuw molecuul te creëren dat CAIF werd genoemd. Kristalstructuren bevestigden dat CAIF door het kanaal loopt, strak past tussen hydrofobe residuen en een covalente binding met K216 aangaat. Dit ontwerp versterkte de FUT8-remming meerdere malen vergeleken met de oudermoleculen, terwijl verwante enzymen gespaard bleven, wat de unieke vorm van FUT8’s allosterische pocket benadrukt.
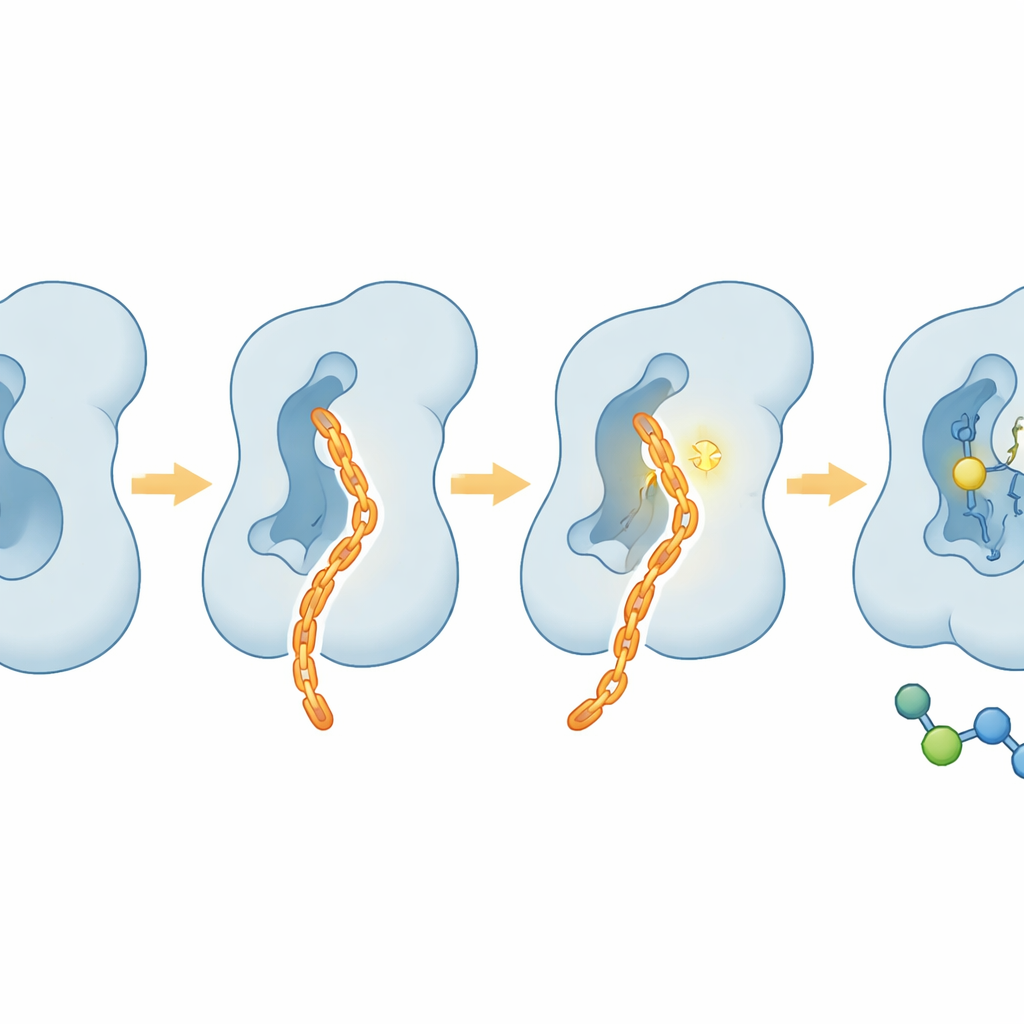
Zacht voor cellen, hard voor tumorgedrag
Buiten proefbuizen onderzocht het team hoe CAIF zich in levende cellen gedraagt. In meerdere humane cellijnen toonde CAIF minimale toxiciteit, zelfs bij hoge concentraties, wat aangeeft dat het niet breed de celmachinerie vergiftigt. Toch verminderde het duidelijk de kernfucosylatie aan het celoppervlak, aangetoond met suikerbindende kleurstoffen, en deed dat met veel betere selectiviteit voor FUT8 dan eerdere pan‑remmers. In invasieassays voor kankercellen overtrof CAIF een veelgebruikte suikergebaseerde remmer in het beperken van het vermogen van tumorcellen om door een matrix te migreren, een kenmerk van metastatische potentie. Deze effecten sluiten aan bij de bekende rol van FUT8 bij het bevorderen van invasie en immuonevasi e in plaats van het direct stimuleren van celdeling.
Wat dit betekent voor toekomstige kankerbehandelingen
Deze studie beweert niet dat CAIF zelf klaar is als geneesmiddel. In plaats daarvan toont het aan dat FUT8 een eerder onbekende, druggabele allosterische pocket bevat die kan worden gericht met zorgvuldig gevormde moleculen die een duurzame binding aan één lysine vormen. Door deze site te benutten, kunnen onderzoekers selectief een suikermodificerend enzym terugschakelen dat op het kruispunt ligt van kankerprogressie, immuunontwijking en geneesmiddelresistentie, terwijl verwante enzymen grotendeels ongemoeid blijven. Het werk biedt een blauwdruk voor het ontwerpen van volgende‑generatie remmers die ziekte‑relevante suikerpatronen op eiwitten hervormen en mogelijk het arsenaal voor kankerimmunotherapie en verbeterde antilichaamgeneesmiddelen uitbreiden.
Bronvermelding: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
Trefwoorden: FUT8-remming, kernfucosylatie, covalente allosterische remmers, kankerglycosylering, ontwerp van glycosyltransferase-geneesmiddelen