Clear Sky Science · nl
FANCD2 remt vorkvoortgang en voorkomt fragiliteit bij vroege oorsprongen tijdens her-replicatie
Als DNA-kopieën een beetje van het script afwijken
Elke keer dat een cel deelt, moet ze haar volledige DNA-bibliotheek precies één keer kopiëren. Als delen van die bibliotheek tweemaal worden gekopieerd, of op een gehaaste en slordige manier, kan dat leiden tot gebroken chromosomen en mutaties die kanker aanjagen. Deze studie onderzoekt wat er gebeurt wanneer de waarborgen van de cel tegen extra kopieerrondes beginnen te falen, en onthult hoe een reparatie-eiwit genaamd FANCD2 ingrijpt om licht afwijkende cellen te behoeden voor het afglijden naar volledige genoomchaos.
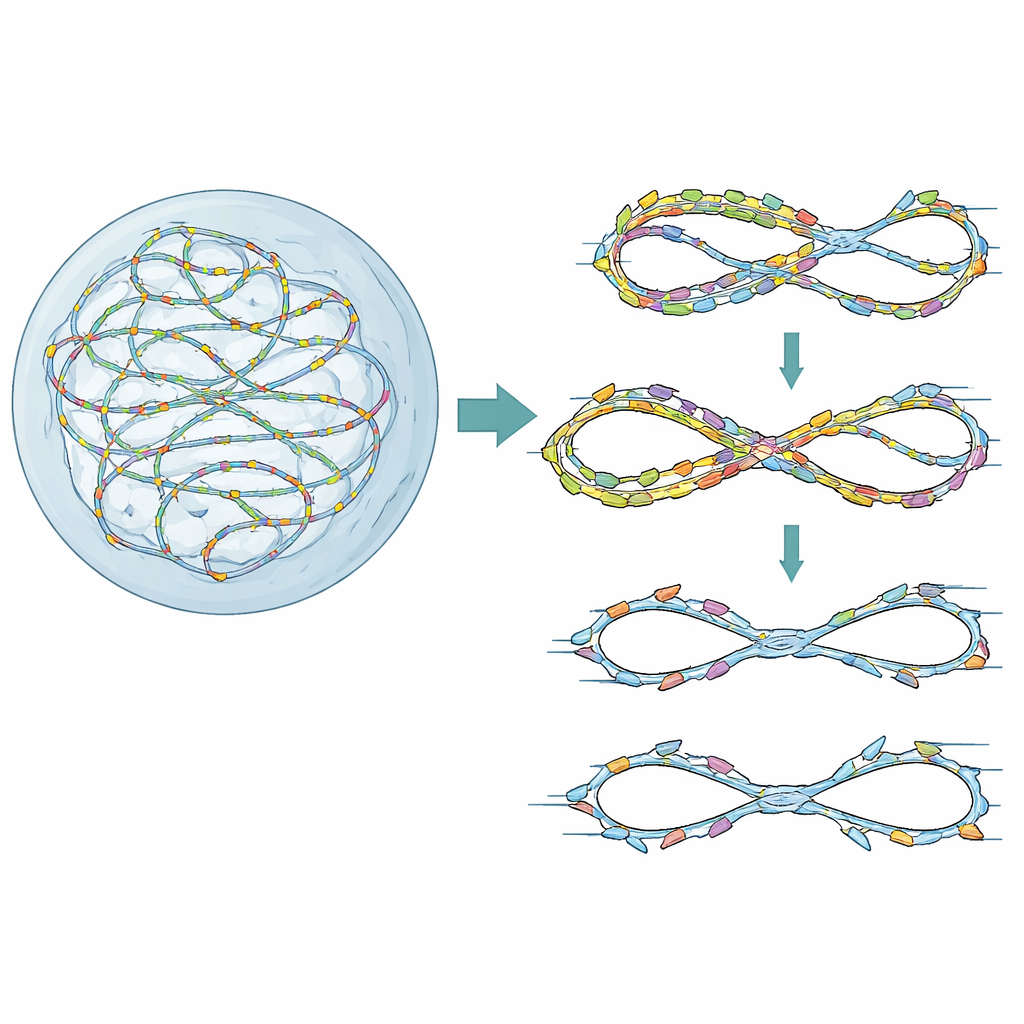
Leuningen voor één schone kopie
Onze chromosomen worden verdubbeld vanaf duizenden startpunten, of “oorsprongen”, die eerst worden geactiveerd (gelicentieerd) en vervolgens in een zorgvuldig getimede volgorde afgevuurd. Een klein eiwitje met de naam Geminin helpt normaal gesproken voorkomen dat elk oorsprong meer dan één keer per celdeling vuren. Wanneer Geminin verloren gaat of verzwakt, kunnen sommige oorsprongen opnieuw afvuren op reeds gekopieerd DNA — een situatie die bekendstaat als her-replicatie. Kankercellen, die vaak te veel licentiefactoren produceren, zijn bijzonder vatbaar voor dit probleem. De auteurs gebruikten eerst een grootschalige genetische screen in humane cellen die waren voorbereid op laag-niveau her-replicatie door Geminin-depletie. Ze vroegen welke DNA-reparatie- en checkpointgenen cruciaal worden in deze gestreste toestand en vonden dat FANCD2, vooral bekend van het repareren van DNA-kruisverbindingen in Fanconi-anemie, naar voren kwam als een sleutelbeschermer van celsurvival en genoomintegriteit.
Een eerstehulpverlener bij overbelaste kopieermachines
Het team volgde vervolgens waar en wanneer FANCD2 verschijnt in cellen die her-repliceren. Kort nadat Geminin is verwijderd, hoopt FANCD2 zich snel op chromatin en vormt heldere nucleaire focale punten, ruim voordat wijdverspreide DNA-breuken detecteerbaar zijn. Met labeling van nieuwgesynthetiseerd DNA en nabijheidsassays toonden ze aan dat FANCD2 rechtstreeks wordt aangetrokken naar actieve replicatiemechanismen, vooral in cellen waarvan het DNA al een tweede keer gekopieerd wordt. In gesynchroniseerde cellen die werden vrijgegeven naar de volgende celdelingscyclus, verscheen een duidelijke populatie met een diffuse, over-replicatie DNA-patroon. Deze cellen vertoonden sterke FANCD2- en RPA-signalen, wat wijst op aanhoudend replicatiestress, en werden door een actieve checkpoint op de grens voor mitose vastgehouden, wat suggereert dat FANCD2 deel uitmaakt van een vroege respons die gestreste vorken stabiliseert in plaats van alleen te reageren op gebroken DNA.
Het beteugelen van weglopende vorken en verborgen gaten
Om te testen hoe FANCD2 het DNA-kopiëren beïnvloedt, combineerden de onderzoekers Gemininverlies met FANCD2-depletie. Verrassend genoeg verhoogde het verwijderen van FANCD2 niet het aandeel cellen met duidelijk her-gerepliceerde genomen. In plaats daarvan onthulden enkelmolecuul DNA-fiberassays dat replicatievorken verder reisden en asymmetrischer werden, een teken van oneven en instabiele voortgang. Deze snellere vorken lieten meer enkelstrengige gaten achter in het nieuw gevormde DNA, zichtbaar als intense RPA- en native BrdU-foci en bevestigd door de gevoeligheid van gelabelde segmenten voor een enzym dat enkelstrengige regio’s knipt. Cellen die zowel Geminin als FANCD2 misten, toonden een toename van chromosoombreuken, fragmenten, nucleaire lichaampjes en micronuclei — allemaal kenmerken van ernstige genoominstabiliteit. Het blokkeren van PARP, een factor die normaal helpt bij het omgaan met zulke gaten, imiteerde en verergerde deze defecten, wat benadrukt dat ongecontroleerde gatvorming centraal staat in de schade.
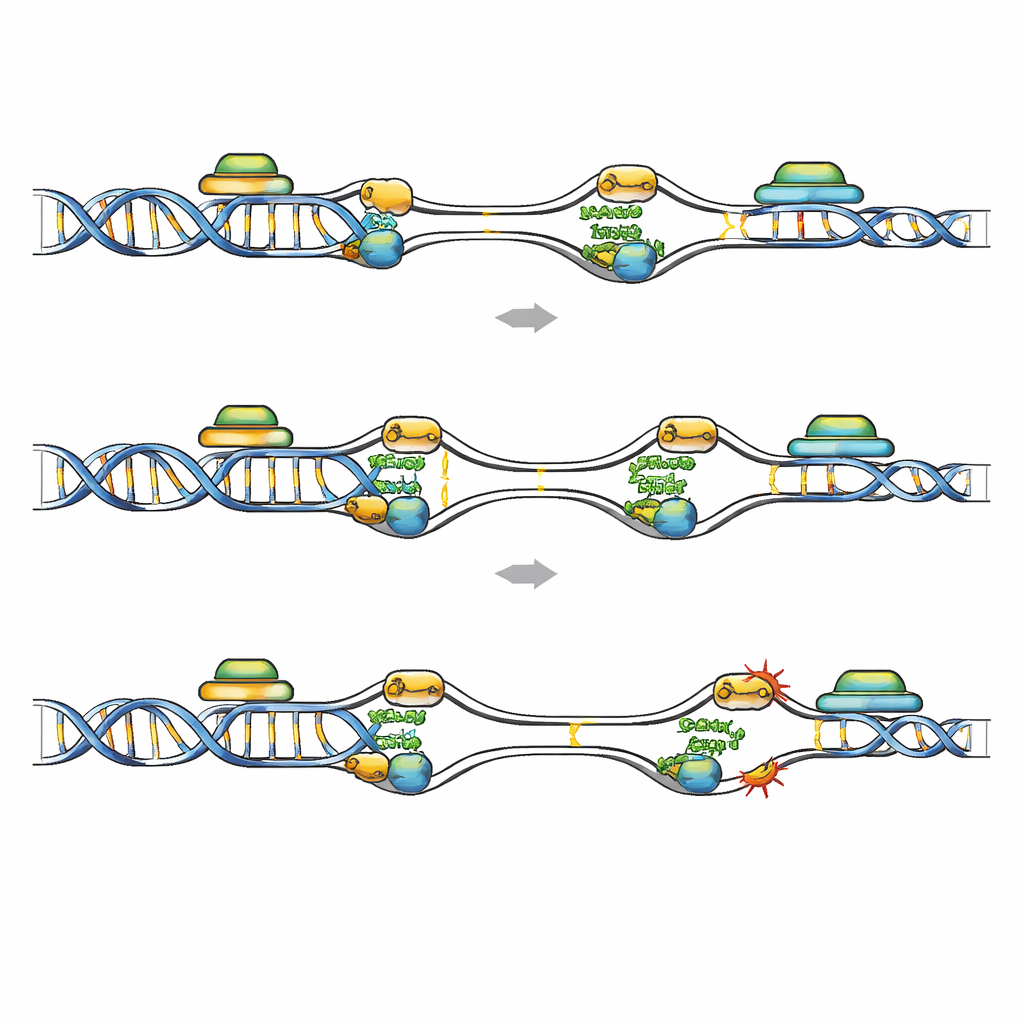
Fragiele hotspots waar kopiëren en aflezen botsen
Genoomwijde kaartlegging van FANCD2-binding gaf inzicht in waar her-replicatie het gevaarlijkst is. In leukemische cellen met Geminin-depletie verschoof FANCD2 van klassieke common fragile sites naar vroeg-afvurende replicatieoorsprongen ingebed in korte, GC-rijke, sterk getranscribeerde genen. Deze gebieden dragen kenmerken van actieve transcriptie en zijn gevoelig voor R-lussen, waarbij nieuw gevormde RNA-hybriden met het DNA-template binden en zo replicatie kunnen blokkeren. Publieke datasets toonden meer DNA-schade en verhoogde RNA–DNA-hybride signalen in FANCD2-verrijkte genen na Gemininverlies, en deze regio’s overlappen met zogenoemde vroeg-replicerende fragiele sites. Wanneer transcriptie breed werd gedempt met een middel, of wanneer R-lussen specifiek werden verwijderd door overexpressie van RNase H1, daalde het aantal FANCD2-, RPA- en DNA-schadefoci in Geminin-deficiënte cellen sterk. Dit wijst erop dat botsingen tussen opnieuw afgevuurde oorsprongen en actieve transcriptie-eenheden, versterkt door R-lussen, fragiele hotspots creëren die FANCD2 moet beschermen.
Fijn afgestelde bescherming via chemische tags
FANCD2 wordt deels geactiveerd door het aanhechten van een kleine ubiquitine-achtige tag. Door FANCA, een kerncomponent van het taggingsapparaat, te depleteren en door gebruik van cellen die een FANCD2-mutant uitdrukken die resistent is tegen deze modificatie, toonden de auteurs aan dat mono-ubiquitinylering het overleven van her-replicerende cellen verbetert maar niet absoluut noodzakelijk is. Zelfs niet-getagde FANCD2 bood gedeeltelijke bescherming, wat consistent is met verschillende rollen in zowel het detecteren als het stabiliseren van gestreste vorken. Het algemene beeld is dat FANCD2 helpt de replicatie bij kwetsbare vroege oorsprongen te vertragen en te organiseren en beperkt hoeveel en hoe groot de enkelstrengige gaten worden.
Waarom dit belangrijk is voor kankerbehandeling
Voor niet-specialisten is de kernboodschap dat niet alle replicatiefouten vanaf het begin catastrofaal zijn. Milde her-replicatie, zoals voorkomt in sommige tumoren, kan worden verdragen als beschermende systemen zoals FANCD2 weglopende DNA-kopieën in toom houden en voorkomen dat fragiele gaten veranderen in gebroken chromosomen. Wanneer deze beveiliging wordt verwijderd of overweldigd, escaleren dezelfde kleinschalige licentiefouten snel tot genoomvernietiging. Aangezien Gemininverlies en defecten in replicatielicentiëring verrijkt zijn in kankercellen, en veel tumoren al zwaktes in het Fanconi/BRCA-netwerk dragen, suggereren de hier blootgelegde kwetsbaarheden therapeutische strategieën: het combineren van remmers die kankecellen naar her-replicatie duwen met geneesmiddelen die gataccumulatie verergeren, zoals PARP-remmers, zou selectief kwaadaardige cellen voorbij hun tolerantiegrens kunnen duwen terwijl normale cellen met intacte bescherming worden gespaard.
Bronvermelding: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
Trefwoorden: DNA-replicatiestress, FANCD2, Geminin, her-replicatie, genoominstabiliteit