Clear Sky Science · nl
Associatie-geïnduceerde vouwing bepaalt de assemblage van de surrogate light chain en het pre-B‑celreceptorcore
Hoe ons lichaam nieuwe antilichamen proefdraait
Voordat een jonge B‑cel in het beenmerg mag toetreden tot het immuunsysteem, moet zij een zware proef doorstaan: kan zij een werkend antilichaam‑core bouwen? Dit artikel onderzoekt hoe een speciale ‘oefen’versie van een deel van het antilichaam, de surrogate light chain genoemd, bij deze test helpt. Door te volgen hoe deze eiwitten vouwen en in elkaar passen, onthullen de auteurs een verborgen kwaliteitscontrolesysteem dat beslist welke toekomstige antilichamen goed genoeg zijn om te behouden — en welke worden afgekeurd.
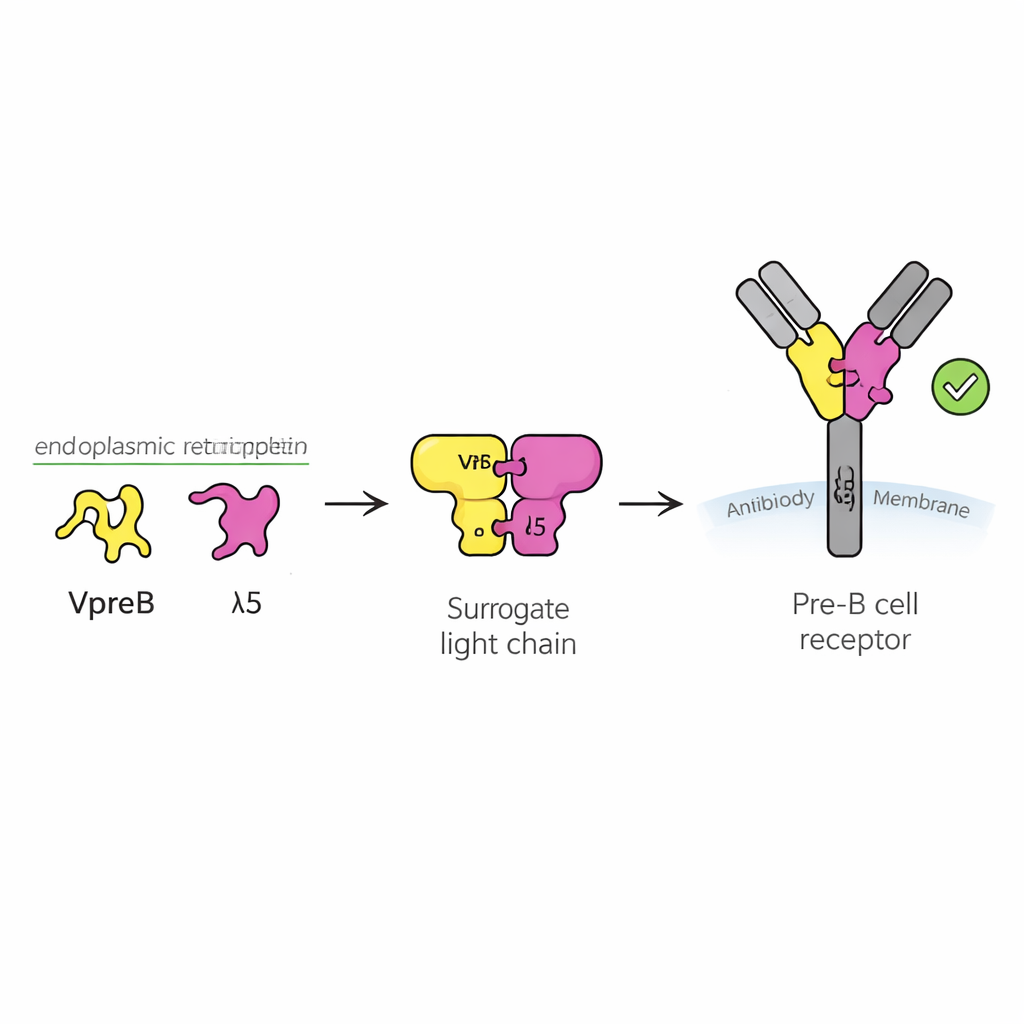
Een veiligheidscontrolepunt voor jonge immuuncellen
Antilichamen zijn Y‑vormige eiwitten die indringers herkennen. Ze bestaan uit twee hoofdonderdelen: zware ketens en lichte ketens. Tijdens de B‑celontwikkeling wordt eerst de zware keten gemaakt, en de cel moet bepalen of deze nieuwe zware keten bruikbaar is voordat hij energie steekt in het maken van een matchende lichte keten. Hiervoor gebruikt de cel een tijdelijke plaatsvervanger, de surrogate light chain, die bestaat uit twee eiwitten genaamd VpreB en λ5. Samen met de zware keten vormen zij het pre‑B‑celreceptor, een sensor op het celoppervlak die een “doorgaan” of “stop” signaal uitzendt. Ongeveer de helft van de pasherstructureerde zware ketens faalt voor deze test, dus begrijpen hoe de surrogate light chain werkt is essentieel om te snappen hoe een gezond antilichaam‑repertoire wordt opgebouwd.
Vouwing door associatie: een onstabiele partner helpen
De auteurs ontdekten dat één component, VpreB, grotendeels niet‑gevouwen en onstabiel is wanneer hij op zichzelf staat. Met behulp van biofysische technieken toonden zij aan dat VpreB pas in zijn juiste driedimensionale vorm schiet wanneer het bindt aan λ5. Een korte streek van λ5, gevormd als een β‑streng, schuift in VpreB en voltooit diens structuur, als het inzetten van een ontbrekende tand in een tandwiel. Deze “associatie‑geïnduceerde vouwing” stabiliseert niet alleen VpreB, ze creëert ook een zeer sterke verbinding tussen de twee eiwitten, met een affiniteit in het lage nanomolaire bereik. In cellen ontsnappen VpreB en λ5 pas aan vasthouding in het endoplasmatisch reticulum en worden zij gesecreteerd of verder vervoerd wanneer ze tot deze surrogate light chain assembleren, wat benadrukt hoe vouwing en kwaliteitscontrole nauw verweven zijn.
De zware keten afwerken en de inspectie doorstaan
Het verhaal eindigt niet bij VpreB en λ5. Een cruciale regio van de zware keten, CH1 genaamd, is aanvankelijk ongestructureerd en wordt binnen de cel gehouden. De onderzoekers lieten zien dat λ5, enigszins als een chaperonne, CH1 kan aanzetten om te vouwen wanneer ze binden. Deze tweede associatie‑geïnduceerde vouwing is essentieel voor het bouwen van het volledige pre‑B‑celreceptor en om het te laten vertrekken uit het endoplasmatisch reticulum naar het celoppervlak. Interessant is dat beide delen van de surrogate light chain — VpreB en λ5 — contact kunnen maken met de zware keten, maar alleen λ5 in staat is CH1 naar zijn afgewerkte, vouwing‑competente staat te brengen. Wanneer dit niet gebeurt, wordt het gedeeltelijke receptorcomplex tegengehouden en verwierp de cel feitelijk die zware keten.
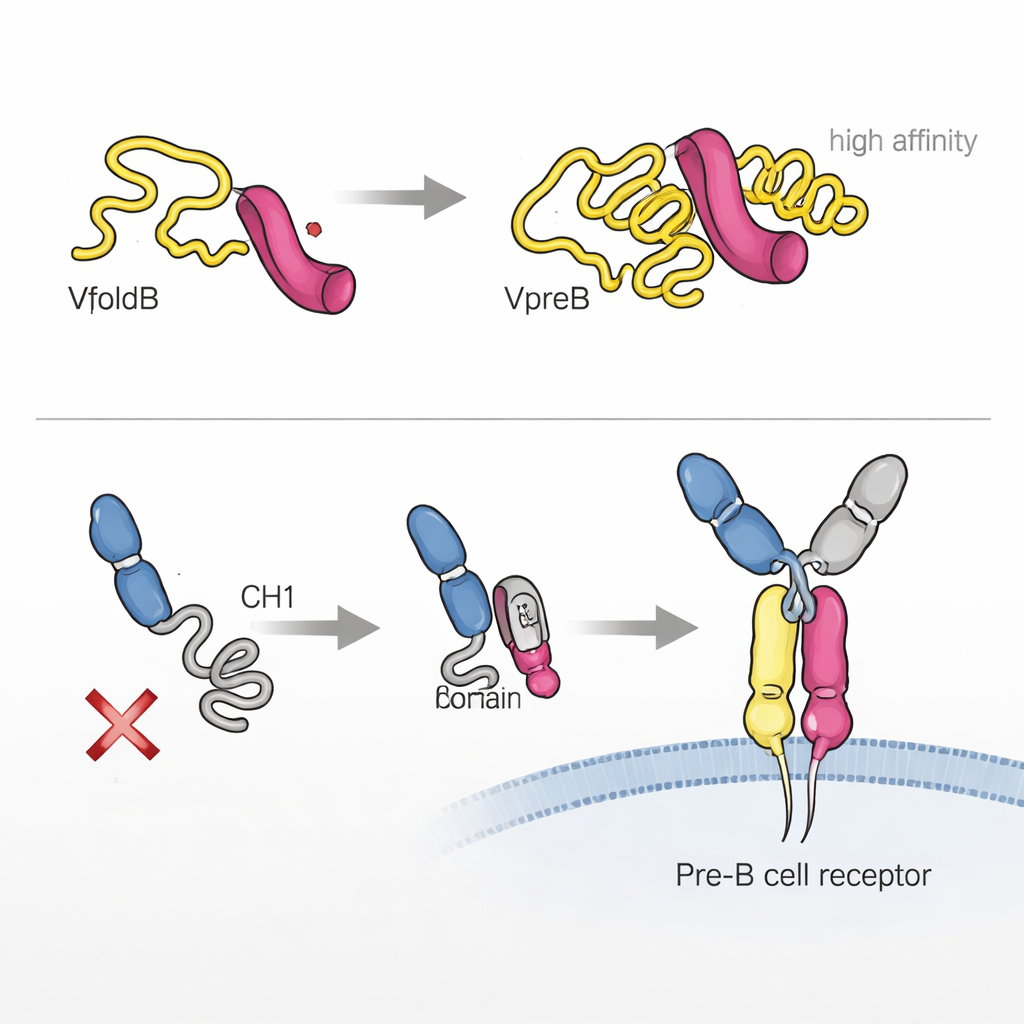
Flexibele staarten die binding en signalering fijnregelen
Zowel VpreB als λ5 dragen slappe, ongestructureerde segmenten die unieke regio’s worden genoemd en geen gelijkenis vertonen met bekende eiwitsequenties. Hoewel deze staarten niet strikt noodzakelijk zijn om de twee eiwitten in een reageerbuis te laten assembleren, vonden de onderzoekers dat ze sterk beïnvloeden hoe snel de surrogate light chain vormt, hoe stabiel deze is en hoe goed hij bindt aan segmenten van de zware keten. In cellen verminderde het weghalen van deze regio’s de efficiëntie waarmee de geassembleerde complexen werden gesecreteerd. De λ5‑staart bleek in het bijzonder multifunctioneel: zij versnelt de assemblage, is essentieel voor bepaalde contacten met het variabele deel van de zware keten en levert belangrijke bijdragen aan hoe het pre‑B‑celreceptor antigenen en andere liganden aangaat. In sommige gevallen benaderde de antigeenbindsterkte van een combinatie van surrogate light chain en zware keten die van een normaal antilichaamfragment.
Waarom dit belangrijk is voor antilichaamdiversiteit
Door deze stapsgewijze vouwing‑ en assemblagegebeurtenissen in kaart te brengen, stellen de auteurs dat de surrogate light chain meer doet dan alleen de zware keten op zijn plaats houden. Hij fungeert als een dynamische inspecteur, die met zijn gestructureerde kern en flexibele staarten voelt of een zware keten correct kan vouwen en productief kan interageren met potentiële doelen. Succesvolle combinaties worden gevouwen, gestabiliseerd en mogen het celoppervlak bereiken, waar ze signalen uitzenden die de B‑cel laten doorgroeien. Defecte combinaties worden vastgehouden en uiteindelijk verwijderd. De kernboodschap voor niet‑deskundigen is dat je immuunsysteem een geraffineerde ‘testbank’ voor toekomstige antilichamen draaiende houdt, opgebouwd uit eiwitten die elkaar letterlijk in vorm vouwen, zodat alleen goed‑functionerende antilichaam‑cores verder mogen om je te verdedigen.
Bronvermelding: König, J., Sarmiento Alam, N.C., He, R. et al. Association-induced folding governs surrogate light chain and pre-B cell receptor core assembly. Nat Commun 17, 1202 (2026). https://doi.org/10.1038/s41467-026-68965-5
Trefwoorden: B‑celontwikkeling, antilichaamvouwing, surrogaatlichte keten, eiwitkwaliteitscontrole, pre‑B‑celreceptor