Clear Sky Science · nl
Enzymatische deracemisatie van structureel diverse allenen ontsluiten met ontworpen photo-enzymen
Waarom het combineren van moleculen ertoe doet
Veel geneesmiddelen werken alleen wanneer hun atomen op een heel specifieke driedimensionale manier zijn gerangschikt, vergelijkbaar met hoe een linkerhand in een linkse handschoen past maar niet in een rechtse. Chemici kunnen deze "éénhandige" moleculen vaak maken, maar het is moeilijk dit schoon te doen wanneer de bouwstenen complex zijn. Dit artikel pakt die uitdaging aan voor een lastige klasse gedraaide structuren, allenen genaamd, door gebruik te maken van speciaal ontworpen lichtgestuurde enzymen. Het werk laat zien hoe biologie en fotochemie gecombineerd kunnen worden om de gewenste moleculaire "hand" uit een verwarrend mengsel te halen, wat snellere en schonere routes naar toekomstige geneesmiddelen en materialen belooft.
Gedraaide bouwstenen met grote opbrengst
Allenen zijn lineaire ketens van drie koolstofatomen met twee aangrenzende dubbele bindingen, maar deze eenvoudige rangschikking draait de ruimte zodanig dat het volledige molecuul een handigheid krijgt. Deze axiale draaiingen komen voor in natuurlijke producten, gewasbeschermingsmiddelen en geavanceerde katalysatoren. Helaas zijn traditionele methoden om chirale allenen te maken vaak sterk gespecialiseerd: een katalysator die uitstekend werkt voor de ene allene faalt vaak voor een andere met kleine structurele veranderingen. Zelfs recent ontwikkelde lichtgestuurde chemische katalysatoren worstelen met dit probleem. Als gevolg daarvan moeten chemici bij het verkennen van nieuwe allenen herhaaldelijk katalysatoren van nul af aan herontwerpen, wat de ontdekking vertraagt en afval vergroot.
De selectiviteit van de natuur lenen en licht toevoegen
Enzymen in levende systemen blinken uit in het herkennen en omzetten van specifieke vormen met opmerkelijke precisie, maar ze zijn geëvolueerd voor natuurlijke doelen, niet voor kunstmatig gemaakte allenen. De auteurs streefden ernaar een "photo-enzym" te creëren dat enzymachtige selectiviteit combineert met het vermogen om licht als energiebron te gebruiken. Ze begonnen met een eiwitraamwerk genaamd CTB10 en herprogrammeerden het genetisch om een niet-natuurlijk aminozuur te dragen dat zich gedraagt als een ingebouwd lichtantennetje. Wanneer deze speciale bouwsteen ultraviolet licht absorbeert, kan hij energie doorgeven aan een nabijgelegen allene, die tijdelijk geëxciteerd raakt en waardoor zijn draaiing kan worden herschikt. Door dit proces vele keren te herhalen, kan het enzym selectief één hand uit een 50:50-mengsel verwijderen en voornamelijk de andere hand achterlaten. 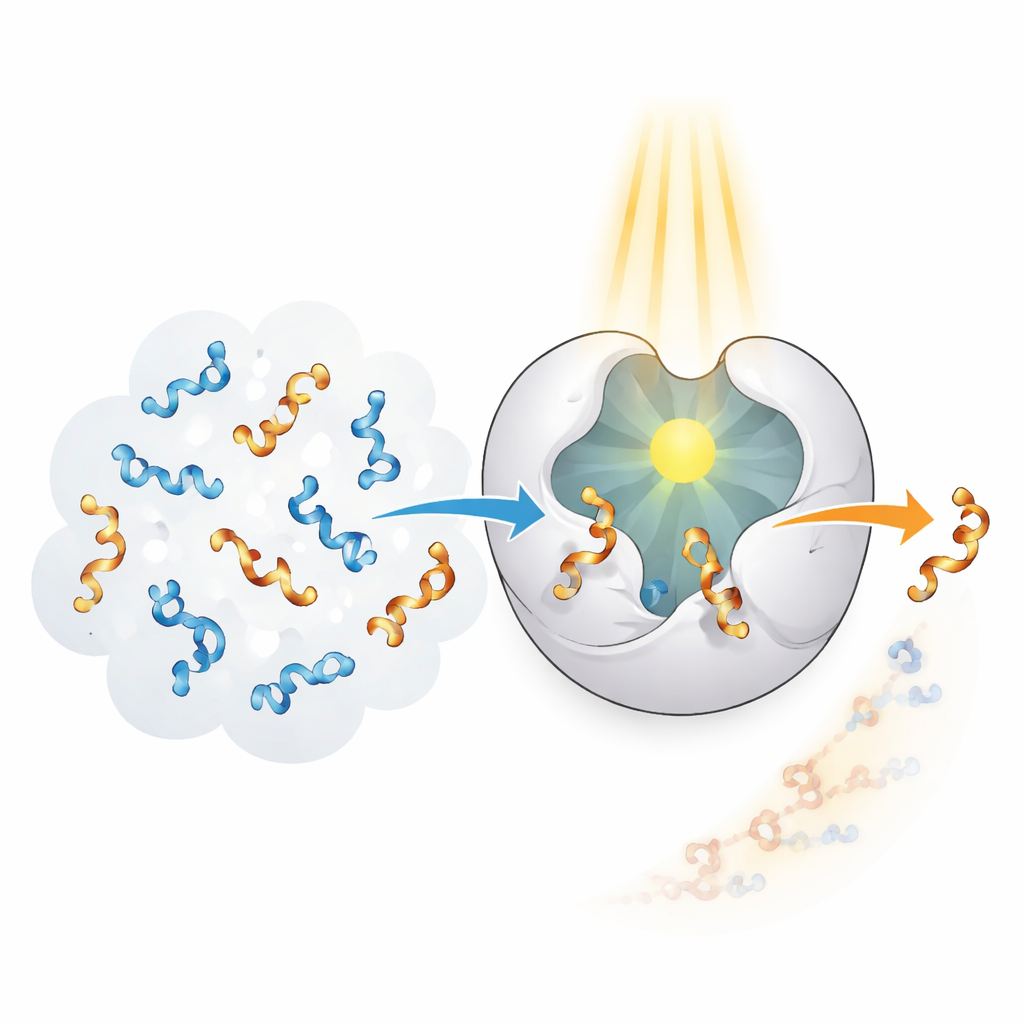
Strakke pocketen uithollen voor vele verschillende gasten
Het ontwerpen van zo'n systeem is niet zo simpel als het schijnen van licht op een eiwit. Het team gebruikte computermodellering, strategische mutaties en röntgendiffractiebeelden om meerdere varianten van het photo-enzym te vormen, elk met een iets andere interne pocket. Deze pockets houden de allene in een gedefinieerde houding naast het lichtantennetje en stabiliseren sleutelpunten van het molecuul via waterstofbruggen en subtiele vouwinteracties. Stap voor stap verbeterden de onderzoekers zowel de bindingssterkte als de uitlijning tussen enzym en allene, die cruciaal zijn voor efficiënte energieoverdracht. De uiteindelijke varianten toonden indrukwekkende prestaties: ze zetten allene-carbonzuren, esters en amiden om in eenhandige producten met zeer hoge zuiverheid, vaak boven 99% van één handigheid, en deden dit in aanwezigheid van lucht zonder dat delicate omstandigheden nodig waren.
Het mechanisme op atomair niveau bekijken
Om te begrijpen waarom de nieuwe photo-enzymen de ene hand boven de andere prefereren, kristalliseerden de auteurs enzym–subtraatparen en onderzochten die op atomair niveau. Ze vonden dat de bevoordeelde allene-hand dichter bij de lichtopvangende groep zit en meerdere licht verschillende vormen kan aannemen, die allemaal compatibel zijn met efficiënte energieoverdracht. De ongunstige hand bindt ofwel zwak of ligt verder weg, waardoor excitatie veel minder waarschijnlijk is. Aanvullende experimenten met zuivere rechts- en linkshandige beginnende materialen bevestigden deze voorkeur: het enzym zet de geprefereerde hand snel om in een reactief intermediair, dat vervolgens in oplossing ontspant naar een mengsel waarin de tegenovergestelde hand zich ophoopt. In wezen gedraagt het eiwit zich als een moleculaire draaiklok, die herhaaldelijk één hand exciteert en consumeert terwijl de andere zich opeenstapelt. 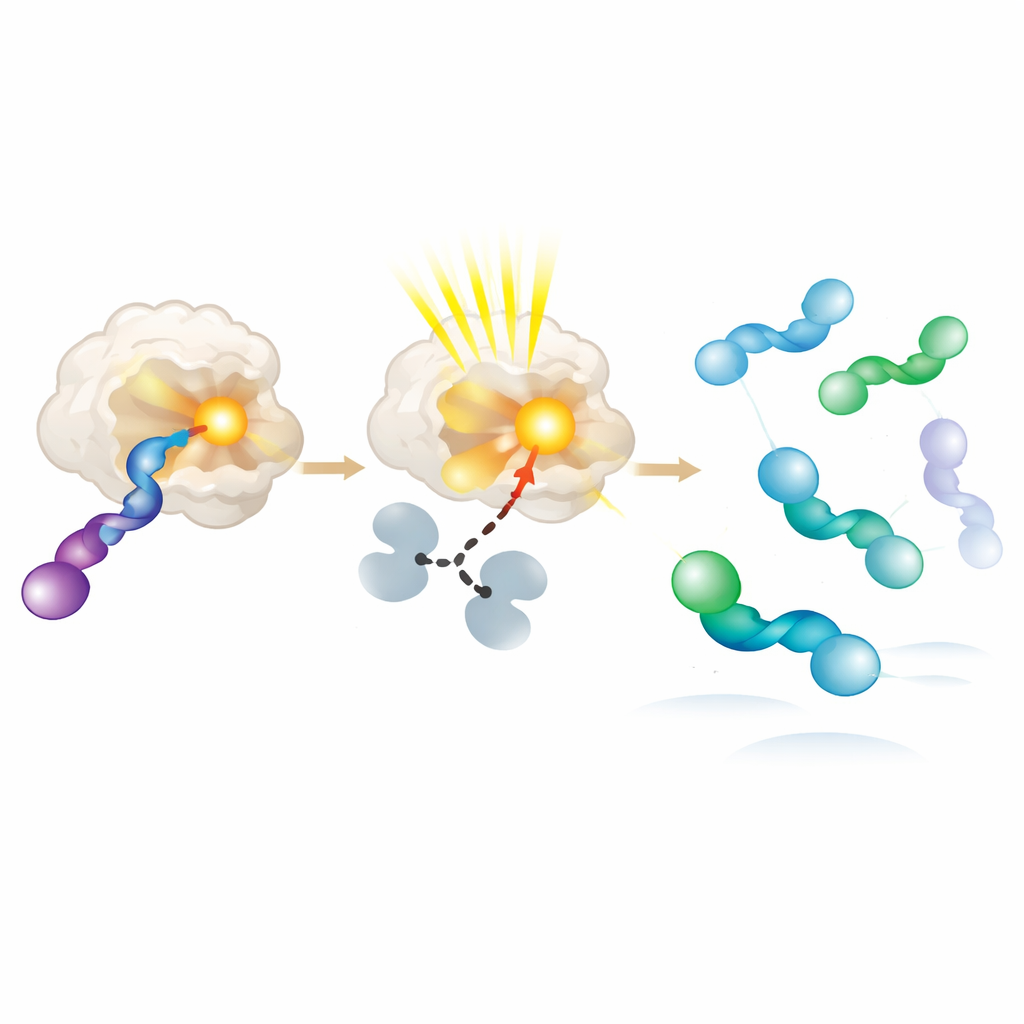
Wat dit betekent voor toekomstige chemie
Voor niet‑specialisten is de belangrijkste boodschap dat het team een programmeerbare eiwitmachine heeft gecreëerd die licht gebruikt om gedraaide moleculen met ongekende veelzijdigheid te sorteren en te upgraden. In plaats van voor elk doel een gloednieuwe chemische katalysator te ontwerpen, kunnen onderzoekers nu beginnen vanaf dit photo-enzymplatform en de interne pocket afstemmen om vele verschillende allenen te accepteren. Deze aanpak verkleint de kloof tussen de voortreffelijke controle van de natuur en de behoefte van de chemische industrie aan brede, robuuste methoden. Op lange termijn zouden dergelijke lichtgedreven enzymen chemici kunnen helpen om complexe, eenhandige bouwstenen voor geneesmiddelen en materialen efficiënter te bereiden, met minder stappen en minder afval.
Bronvermelding: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
Trefwoorden: photo-enzym, deracemisatie, chirale allene, biokatalyse, triplet-energieoverdracht